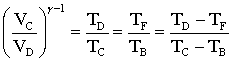|
|
|||
|
|||
|
On considère que le carburant utilisé est assimilable à de l'octane de formule brute C8H18 de masse volumique r= 720 kgm-3.
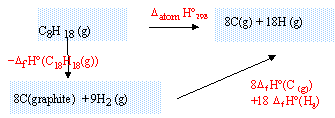
Le pouvoir calorifique Q de l'octane est la chaleur libérée par la combustion d'une unité de volume d'octane. Donner sa valeur en kJ cm-3. corrigé C8H18(g) +12,5 O2(g) --> 8 CO2(g) + 9H2O (g) Enthalpie de formation de l'octane à 298 K: On réalise un cycle thermodynamique, faisant intervenir la réaction d'atomisation de l'octane ( toutes les liaisons sont rompues, réactifs et produits étant à l'état gazeux)
DatomH0 = 7 DliaisonH0 (C-C) + 18DliaisonH0 (C-H) DatomH0 =7*345+18*415=2415+7470=9885 kJ/mol. 8DfH0(C(g)) + 18DfH0(H(g)) = 8*716,7+18*218 = 5733,6+3924=9657,6 kJ/mol DfH0 (octane(g)) = 9657,6 -9885 = -227,4 kJ/mol. enthalpie standart de combustion de l'octane : C8H18(g) +12,5 O2(g) --> 8 CO2(g) + 9H2O (g) DcombH0 = -DfH0 (octane(g)) -12,5DfH0 (O2(g)) + 8DfH0 (CO2(g))+ 9 DfH0 (H2O(g)) DcombH0 = -(-227,4)-12,5* 0 + 8*(-393,5)+9*(-241,8)= -5,1 103 kJ/mol. Chaleur libérée par la combustion d'un cm3 d'octane : masse d'1 cm3 d'octane : 0,72 g masse molaire octane : 8*12+18 = 114 g/mol Qté de matière d'octane dans 1 cm3 : 0,72/114 = 6,31 10-3 mol. Q = 6,31 10-3 *5,1 103 = 32,2 kJ cm-3.
|
|||
|
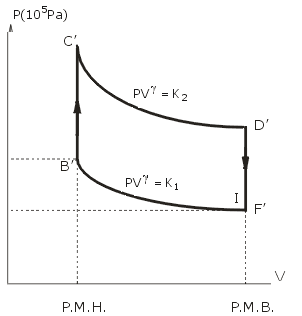
Les scooters de cylindrée inférieure à 50 cm3 sont équipés d'un moteur à explosion à deux temps. Celui-ci existe sous plusieurs formes. Le type le plus répandu ( surtout dans le domaine des petites puissances ) est celui qui comporte trois lumières ; celles-ci sont destinées à assurer l'aspiration, l'échappement et la communication entre le carter et le cylindre. Le mélange carburé ( air - essence - huile ) provenant du carburateur pénètre dans le carter pendant le mouvement du piston du P.M.B (point mort bas) au P.M.H (point mort haut). Au cours de la descente, cet air est comprimé et dirigé vers le cylindre par le canal de transfert. La légère compression du mélange carburé permet l'évacuation du gaz de combustion. Le graissage des parties mobiles, assuré par de l'huile que l'on mélange à l'essence, permet de réduire les frottements. 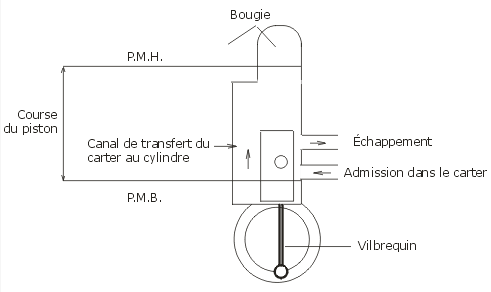 Il est rappelé que les quatre phases ( admission, compression, combustion et détente ), qui sont réparties sur deux tours du vilebrequin dans un quatre temps (deux allers et deux retour - menus du piston) se succèdent dans un deux temps sur un seul tour du vilebrequin (un aller et un retour - menu du piston). Cela est possible parce que les phases échappement et admission ont lieu très rapidement et sensiblement au moment où le piston se trouve au point mort bas (P.M.B). Pratiquement le diagramme de Watt ( pression en ordonnées, volume en abscisses ) a l'allure représentée sur la figure ci-dessous. On y distingue les deux temps : - 1er temps : compression du mélange carburé (FB), combustion (BC). - 2ème temps : détente (CD), échappement des gaz de combustion et admission d'une nouvelle charge de mélange carburé (DHF). 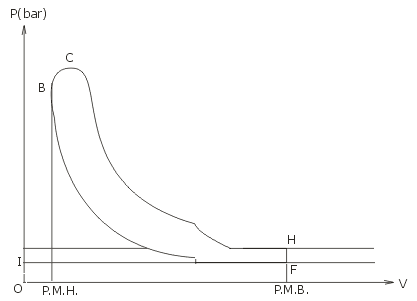 Le diagramme théorique (B'C'D'F') s'identifie au cycle de Beau de Rochas. Il est établi avec les hypothèses suivantes : - la combustion (B'C') est instantanée et se produit lorsque le volume du cylindre vaut VC (piston au point mort haut). - la détente (C'D') et la compression (F'B') du mélange sont adiabatiques réversibles. - lors de l'échappement et de l'admission (D'F') quasi instantanées, le volume du cylindre est considéré constant égal à VD . La cylindrée du moteur est VD-VC . Le taux de compression est égal au rapport volumétrique a= VD / VC . Dans la notice technique d'un scooter (Spacer 50 Kymco), on lit les indications suivantes : vitesse maximale : 45 km.h-1. régime de puissance maximale : 7000 tours.min-1. (vitesse angulaire de vilebrequin) puissance maximale : 4,40 kW cylindrée : 49,5 cm3. course du piston : 39,2 mm. On donne : * la constante des gaz parfaits : R = 8,31 J.mol-1 .K-1. * la température et la pression du point F' : TF =300 K ; PF = 105 Pa. On fera d'autre part l'approximation suivante : l'air étant en grand excès par rapport au mélange ( huile + carburant ), on assimilera le mélange carburé à un gaz parfait unique, de coefficient g=1,4( g = Cp / Cv rapport de capacités thermiques molaires à pression constante et à volume constant), de masse molaire 29 g.mol-1 . On rappelle que le pouvoir calorifique, noté q, supposé indépendant de la température, est la chaleur libérée par la combustion d'une unité de volume d'essence. On prendra q= 30 kJ.cm-3 . détermination de la consommation d'essence du scooter :
|
|||
|
vitesse moyenne du piston sur un cycle : Un tour de vilebrequin correspond à un cycle thermodynamique. 7000 tours éffectués en 60 s soit 1 tour effectué en 60 / 7000 = 8,57 10-3s =8,57 ms, durée d'un cycle. Un cycle correspond à un aller-retour - menu soit 2 * 39,2 10-3 = 7,84 10-2 m. v moy = 7,84 10-2 / 8,57 10-3 = 9,14 m/s. vitesse moyenne quadratique des molécules :
(3 *1,38
10-23 *300 / 4,81 10-26
)½ =508
m/s
valeur très supérieure à la vitesse du
piston. La transformation est quasi-statique et on peut la
considérer comme réversible.
S'il n'y a pas d'échange de chaleur lors des transformations C'D' et F'B', celles-ci peuvent être modélisée par des adiabatiques réversibles. PVg =Cte pour un gaz parfait et pour une transformation adiabatique réversible. dans une transformation adiabatique, il n'y a pas déchange de chaleur donc l'entropie échangée est nulle. si la transformation est en plus réversible, l'entropie crée est nulle. la variation d'entropie est donc nulle : transformation isentropique. Ce
résultat est indépendant de la nature du
système (gaz parfait, gaz de Van der Waals )
la détente C'D' est adiabatique réversible donc WC'D'= DU = n Cv mDT= n Cv m(TD -TC) la compression F'B' est adiabatique réversible donc WF'B'= DU = n Cv mDTn = Cv m(TB -TF) Wcycle = n Cv m(TD -TC+TB -TF) or nCv m = nR / (g-1) et PFVD = nRTF. Wcycle
= PFVD / ((g-1)TF)
(TD -TC+TB
-TF)
pour la transformation B'C' ( W=0) et DU = Qchaud = n Cv mDT= n Cv m(TC -TB) Qchaud
= PFVD / ((g-1)TF)
(TC -TB)
h = travail fourni à l'extérieur / chaleur libérée par la combustion h = -W cycle / Q chaud = (-TD +TC-TB +TF) / (TC -TB) h = 1 - (TD-TF ) / (TC -TB) or pour une adiabatique réversible PVg = Cte et PV / T = Cte1 d'où TV(g-1) = constante
h =
1 - 1/ a(g-1)
travail W = h Qchaud =0,4 Qchaud et la durée d'un cycle est : 8,57 10-3 s 4 400 =
0,4
Qchaud / 8,57 10-3 soit Qchaud
= 94,2
J/ s.
vitesse 45 /3,6 = 12,5 m/s durée de parcours : 105 / 12,5 = 8000 s. nombre de cycle : 8000 / 8,57 10-3 = 9,33 105. énergie mise en jeu : 9,33 105*94,2 = 8,8 107 J pouvoir calorifique q = 3 104 J.cm-3 consommation : 8,8107 / 3 104 = 2900 cm3 = 2,9 L. le pouvoir
calorifique de l'essence est grand, alors la consommation
reste faible.
Mais l'admission et l'échappement se déroulent en même temps, le travail récupérable est en réalité plus faible car les gaz frais se mélangent partiellement aux gaz brûlés.
retour - menu |
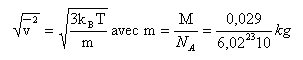 =
4,81 10-26 kg
=
4,81 10-26 kg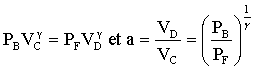 =
61 / 1,4 = 3,59.
=
61 / 1,4 = 3,59.