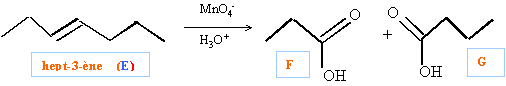|
|
|||
|
|||
|
synthèse |
Par oxydation d'un carbure éthylénique E, on obtient 2 composés F et G. F donne avec l'alcool éthylique une réaction d'équilibre au cours de laquelle il se forme du propanoate d'éthyle. G peut être obtenu par hydrolyse du produit d'addition de l'anhydride carbonique sur le bromure de propyl-magnésium.
corrigé |
||
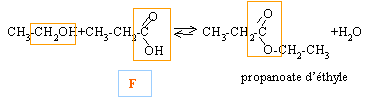
CH3-CH2-CH2-MgBr + CO2 conduit à CH3-CH2-CH2-COOH acide butanoïque (G)
|
|||
|
à partir du but-1-ène |
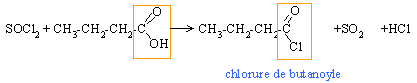
Le but-1-ène traité par du bromure d'hydrogène en présence d'un peroxyde organique donne un corps A. A est transformé par une solution diluée d'hydroxyde de sodium en B qui, par oxydation par le dichromate de potassium en milieu acide à 70°C donne C. C traité par le chlorure de thionyle SOCl2 donne D.
corrigé |
||
|
CH3-CH2-CH=CH2 + HBr donne CH3-CH2-CH2-CH2Br 1-bromobutane (A) (A) +HO- donne CH3-CH2-CH2-CH2-OH butan-1-ol (B) 2{ Cr2O72- +6 e- + 14H+ --> 2Cr3+ + 14H2O } réduction 3{ C3H7CH2OH + H2O --> C3H7COOH + 4 e- + 4H+ } oxydation 2Cr2O72- + 3C3H7CH2OH + 16H+ --> 4 Cr3+ + 3C3H7COOH + 11H2O acide butanoïque (C) (C) + SOCl2 donne SO2 +HCl +CH3-CH2-CH2-CO
|
|||
|
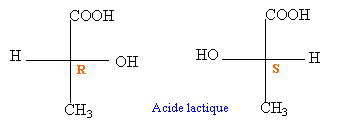
acide lactique |
On utilise l'éthanal comme réactif organique de base et tous les produits minéraux utiles.
|
||
|
puis en présence H3O+ à : CH3-CHOH-COOH On obtient un mélange racémique : 50% de R et 50% de S
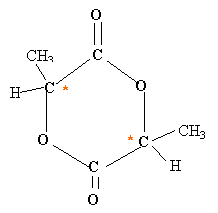
La déshydratation intramoléculaire de l'acide 3-hydroxybutanoïque donne l'acide but-2-ènoïque. CH3-CHOH-CH2-COOH donne CH3-CH=CH-COOH (configurations Z et E) L'estérification entre 2 molécules d'acide lactique donne un lactide.
2 C * asymétriques donc 4 isomères. |
|||
|
|
|||
|
à partir de l'acide monochloroacétique |
|
||
|
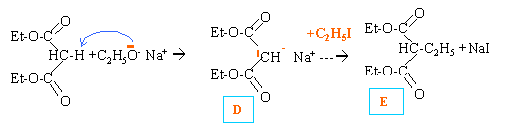
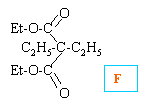
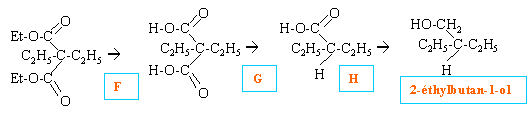
Cl-CH2-COOH donne NC-CH2-COOH acide 2-cyanoéthanoïque (A) l'hydrolyse acide conduit à HOOC-CH2-COOH acide propanedioïque (B) estérification en présence d'éthanol propanedioate d'éthyle (C) C2H5-OOC-CH2-COO-C2H5
suivi ensuite par des réactions analogues à la fixation d'un second groupe ethyle.
|