| |
les phéromones chez les insectes (France bac juin 99)
|
||||||
|
|
stéréochimie |
La communication, c’est-à-dire le transfert d’informations, chez les insectes se fait principalement par voie chimique grâce à des substances appelées phéromones. Certaines sont des signaux d’alarme, d’autres permettent le marquage d’une piste ou sont destinées à attirer les insectes de sexe opposé en vue de la reproduction.On se propose d’étudier deux exemples de phéromones.
Etude de la molécule A.
Etude de la molécule B.
Malcool :88 g /mol; M acide =60 g/mol ; MB =130 g/mol.
|
|||||
| |
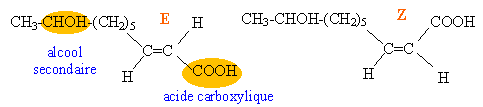
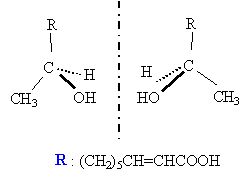
Le carbone porteur de la fonction alcool est tétraédrique et porte 4 groupes différents. C'est un carbone asymètrique
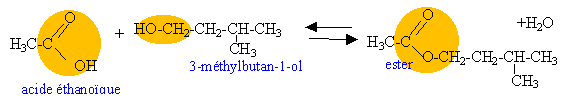
Quantités de matière des réactifs : acide éthanoïque :10/60= 0,166 mol alcool : 10 /88 =0,1136 mol l'alcool est en défaut, c'est le réactif limitant. On peut théoriquement obtenir 0,1136 mol d'ester soit : 0,1136* 130= 14,77 g rendement : masse expérimentale *100 / masse théorique 10,7*100/14,77 = 72 %.
|
||||||
|
|
|