|
|
||||||
|
||||||
|
|
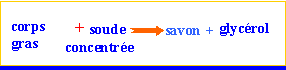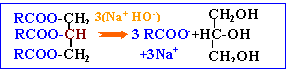
Depuis très longtemps, la réaction de saponification des triglycérides (triesters du glycérol) par la soude (solution aqueuse d.hydroxyde de sodium) permet la fabrication du savon, les triglycérides utilisés étant des mélanges de graisses et d'huiles. Ce procédé est encore utilisé et 90 000 tonnes de savon sont ainsi fabriqués en France chaque année. Les triglycérides ont une formule développée de la forme :
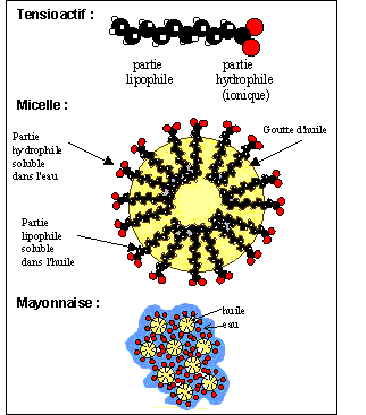
- que les graisses et les huiles sont non miscibles (insolubles) dans l'eau ; - que dans l'eau, les micelles sont des agglomérats d.ions carboxylate.
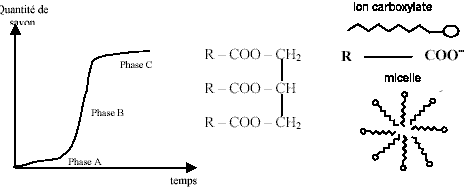
Soit R -COO- l'ion carboxylate formé. R est la partie hydrophobe et COO- est la partie hydrophile. la vitesse est égale au coefficient directeur de la tangente à la courbe à la date t donnée. Au cours de la phase de démarrage, la courbe n'est pas très inclinée donc la vitesse de la réaction n'est pas très grande. Lors de la phase de saponification rapide, la courbe croît de façon beaucoup plus importante au cours du temps, on en déduit donc que la vitesse est plus grande. Enfin au cours de la phase de fin de saponification, la courbe tend vers une asymptote horizontale ce qui signifie que la vitesse tend vers 0. Phase A : il est rappelé au début du sujet que les graisses et les huiles sont insolubles dans l'eau. Or la réaction de saponification met en jeu des triglycérides et de la soude, deux substances insolubles. Pour maintenir l'émulsion de deux substances non miscibles, il est nécessaire d'agiter. Phase B : les ions carboxylate vont se lier : - par leur partie l'eau contenue dans la solution de soude ; - par leur partie hydrophobe aux molécules de triglycéride Il y aura ainsi formation de micelles.
disperser la graisse dans l'eau, permet de faciliter la « rencontre entre les molécules de triglycérides et les ions hydroxyde. Au fur et à
mesure que la réaction de saponification a lieu, les concentrations des
réactifs diminuent ; ceci entraîne la diminution de la vitesse de la
réaction lors de la troisième phase.
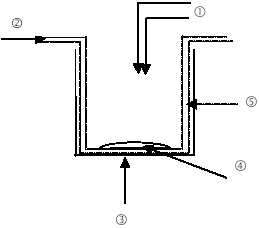
2. La vapeur d.eau 3. La cuve 4. Le fond de savon 5. Le serpentin Le savon, en rendant miscibles les deux réactifs, augmente la vitesse de la réaction. La vapeur d'eau qui circule au fond de la cuve dans un serpentin, permet de porter le mélange à ébullition. Une température élevée augmente la vitesse de la réaction.
|
|||||
|