|
chimiste français (1786-1889) |
||||||
|
||||||
|
|
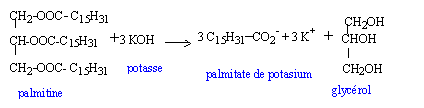
document : Au début de la vie professionnelle de Chevreul, l'industrie textile était le moteur de l'innovation scientifique et technologique en chimie. Dans ce contexte il eut à analyser un savon mou... Ce savon était obtenu par chauffage d'un mélange de graisse de porc et de potasse. Chevreul traite cette combinaison par un acide fort ( acide chlorhydrique). Il en retire une substance nacrée. Cette substance possède des propriétés acides. Il l'appelera acide margarinique. Son nom définitif d'acide palmitique lui viendra de Frémy qui l'a isolé dans l'huile de palme. L'acide palmitique fond à 63°C, il est insoluble dans l'eau. Masse molaire en g/mol : palmitine 806 ; potasse : 56 ; palmitate de sodium 294. Questions :
CH3-(CH2)14-COO- ion palmitate, base conjuguée
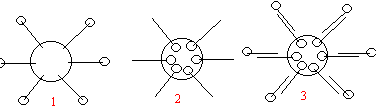
234000 / 294 = 79,6 mol de palmitate de potassium soit 79,6 / 3 = 26,53 mol de palmitine. 16,53 * 806 = 21,38 kg palmitine. en tenant compte du rendement : 21,38 / 0,8 = 26,72 kg. % palmitine dans la graisse de porc : 26,72 / 100 *100 = 26,7%. CO2- constitue la partie hydrophile ; CH3-(CH2)14- constitue le groupe lipophile. la micelle est le schéma (1), chaine carbonée fixée sur la graisse et groupe CO2- du coté de l'eau. CH3-(CH2)14-COO- + H3O+ --> CH3-(CH2)14-COOH + H2O l'acide palmitique est très peu soluble dans l'eau, l'extrémité hydrophile n'existe plus. Un savon est donc peu efficace en milieu acide.
|
|||||
|