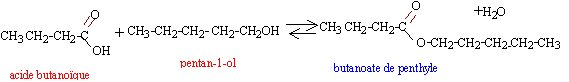|
Amérique du Nord 06/01 |
|||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||
|
|
préparation d'un ester : Le butanoate de pentyle de formule brute C9H18O2 est un ester dont l'odeur rappelle celle de l'abricot.
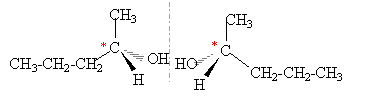
stéréochimie : L'alcool B peut être préparé par hydratation d'un alcène le pent-1-ène. On obtient en même temps que l'alcool B un autre alcool B' : le pentan-2-ol. - Donner la formule semi-développée de cet alcool B' et préciser sa classe. - Qu'est ce qu'un atome de carbone asymétrique ? - Des deux molécules d'alcool laquelle possède un atome de carbone asymétrique ? repèrer sur la formule semi-développée le carbone asymétrique par un astérisque. - Comment qualifie-t-on cette molécule ? - Schématiser les deux énantiomères en représentation conventionnelle.
l'alcool, le pentan-1-ol est un alcool primaire. l'acide est l'acide butanoïque
température, concentration des réactifs et catalyseur sont des facteurs cinétiques. expérience 1 : la température est plus élevée (70°C au lieu de 50°C) la vitesse de la réaction est d'autant plus grande que la température est élevée. expérience 2 : la température est plus élevée (80°C au lieu de 50°C) et présence d'un catalyseur, l'acide sulfurique. la vitesse de la réaction est encore plus grande, car deux facteurs cinétiques favorables interviennent. expérience 3 : la température est plus élevée (70°C au lieu de 50°C) et présence d'un catalyseur, l'acide sulfurique. la vitesse de la réaction est plus grande, car deux facteurs cinétiques favorables interviennent. expérience 4 : la température est plus élevée (70°C au lieu de 50°C) et présence d'un excès de l'un des réactifs, l'alcool. la vitesse de la
réaction est plus grande, car deux facteurs cinétiques favorables
interviennent.
un carbone asymétrique est un atome de carbone tétragonal lié à 4 groupes d'atomes différents. la molécule de pentan-2-ol est chirale représentation des deux énantiomères :
|
||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||
|