|
bac Amérique du sud 11/2000.
|
||||||||||
|
||||||||||
|
|
On trouve dans le commerce des produits liquides servant à déboucher les canalisations obstruées. On peut lire sur l'étiquette " danger, produit corrosif; contient de l'hydroxyde de sodium( soude caustique solution 20%". On se propose de vérifier cette teneur en soude par dosage avec une solution connue d'acide chlorhydrique. préparation d'une solution diluée : Le produit commercial est trop concentré pour pouvoir être dosé directement. On prépare doc 500 mL d'une solution diluée 50 fois (solution S)
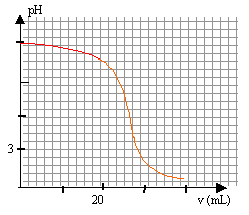
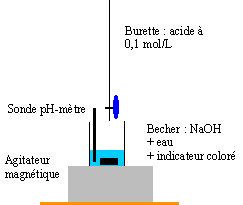
dosage pH-métrique : IOn souhaite doser 20 mL de la solution diluée avec une solution d'acide chlorhydrique de concnetration Ca = 0,1 mol/L, en utilisant un pH-mètre.
masse atomique (g/mol) : H=1 ; O=16 ; C=12 ; Na=23.
|
|||||||||
|
le rapport des volumes de la fiole jaugée et de la pipette est égal à 50 . volume fiole jaugée = 500 mL volume pipette = 500 / 50 = 10 mL. matériel nécessaire : fiole jaugée 500 mL; pipette 10 mL+ pipeteur se munir de gants et de lunette de
protection pour manipuler la solution commerciale corrosive.
L'eau n'apporte quasiment pas d'ion hydroxyde, le résultat du dosage n'est pas faussé.
H3O+ + HO- --> 2H2O totale, exothermique à l'équivalence les quantités de matière d'acide et de base sont stoéchiométriques. Avant l'équivalence la base est en excés, après l'équivalence l'acide est en excès.
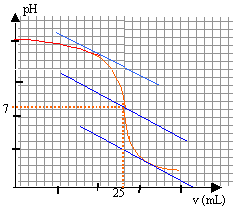
CsVs = CaVa Cs= 0,1*25/20=0,125 mol/L C= 50 Cs = 6,25 mol/L. la zone de virage de l'indicateur coloré doit contenir le pH du point équivalent (pH=7 dans ce cas) donc bleu de bromothymol
masse de soude dans la solution du commerce : 6,5*40 = 250 g masse de 1L de ce produit commercial : 1208 g pourcentage massique de soude : 250/1208 *100 = 20,7 % écart relatif : (20,7 - 20 )/ 20 *100 = 3,5%
|
||||||||||
|