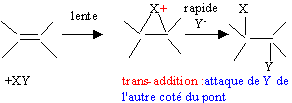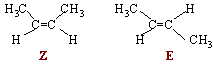|
|
||
|
||
|
Dans un premier temps le but-1-ène est hydraté à froid en milieu acide sulfurique dilué. On obtient majoritairement un produit A.
CH3-CH2-CH=CH2 + H2O = CH3-CH2-CHOH-CH3 : butan-2-ol mécanisme réactionnel de la réaction en justifiant la formation majoritaire de A:
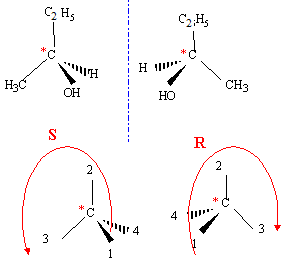
La règle de Markovnikov permet de prévoir sur quel atome de carbone se fixe l'hydrogène de l'hydracide ( ou de H2O) : l'atome d'hydrogène se fixe sur l'atome de carbone le moins substitué. Le produit A possède des stéréoisomères ; représentation de Cram et nomenclature RS.
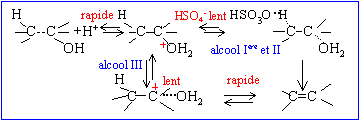
Le composé A est maintenant déshydraté en milieu acide sulfurique concentré à 150 °C. équation bilan de la réaction précédente : CH3-CH2-CHOH-CH3 =
CH3-CH=CH-CH3 + H2O Dans le cas ou plusieurs atomes de carbone sont porteurs d'hydrogènes pouvant être éliminés, l'alcène le plus substitué se forme.
Le but-2-ène présente une stéréoisomérie de type Z E :
|
||
|
|