|
Imagerie par émission de positons d'après IMRT 05 |
||||||
|
||||||
|
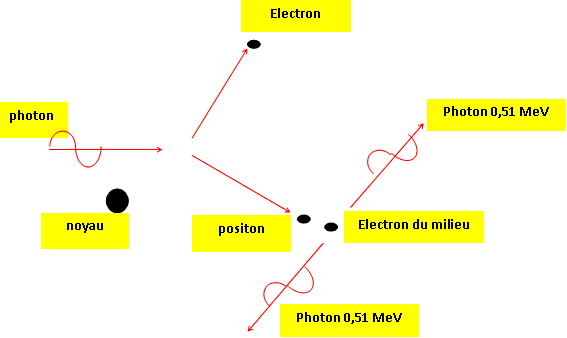
Les protons de 16 MeV sont produits dans un cyclotron. La période du fluor 18 est T= 2 heures. Données : 1 eV = 1,6 10-19 C ; unité d'activité 1 Ci = 37 GBq = 3,7 1010 Bq c= 3,0 108 m/s ; masse du proton mP= 1,67 10-27 kg. Le fluor 18 qui marque un dérivé du glucose est préparé par l'interaction d'un proton 11p d'énergie 16 MeV avec un atome d'oxygène 18 18O. Ecrire l'équation de cette réaction nucléaire. Enoncer les lois appliquées. 188O + 11p ---> 189F + 10n (neutron) Conservation de la charge : 8+1 = 9 ; conservation du nombre de nucléons : 18+1 = 18+1 Le fluor 18 est émetteur bâta+. Ecrire la réaction de désintégration. 189F ---> 188O + 01e + neutrino. Le chemin suivi par le positon est très court, il est freiné par la matière et s'annihile en fin de course avec un électron du milieu.
Après 2 heures de tir de protons de 16 MeV sur 1 mL d'eau enrichie de 95% en oxygène 18 et une synthèse du 18FDG qui dure environ 1 h, on obtient à 6 h du matin une solution de 18FDG d'activité A0 = 110 GBq. L'activité volumique maximum autorisée étant av=250 MBq mL-1, on procède à une dilution, afin d'avoir à cette heure là, un volume Vi de solution ayant juste cette activité volumique maximum autorisée. Calculer ce volume Vi. 110 GBq = 110 000 MBq ; A0 / av= 110 000/250 = 440 Il faut diluer 440 fois la solution de 1 mL ; le volume final est 440 mL.
A partir de cette solution, on prépare à 6 h du matin des lots dont l'activité doit être de Ainj = 10 mCi au moment de l'injection. Calculer Ainj en MBq. unité d'activité 1 Ci = 37 GBq = 3,7 1010 Bq ; 1 mCi = 3,7 107 Bq 10 mCi = 3,7 108 Bq = 3,7 102 MBq. La période du fluor 18 est T=2 h. Calculer sa constante radioactive l. lT = ln2 ; l = ln2 / T = ln2 / 2 = 0,347 h-1 = 9,63 10-5 s-1.
|
||||||
|
|