|
Radioactivitť.
Il existe trois type de dťsintťgrations radioactives : a, Ŗ+ et Ŗ-.
Quel est
le type des particules ťmises dans chacune de ces dťsintťgrations
?
alpha : noyau d'hťlium 42He ; Ŗ+
: ťlectron 0-1e ; Ŗ- : positon
01e.
Le potassium 4019K
est radioactif et se dťsintŤgre en donnant de l'argon 4018Ag.
Donner
l'ťquation de sa dťsintťgration en rappelant les
rŤgles de conservation utilisťes. De quel type de
dťsintťgration s'agit-il ?
4019K ---> 4018Ag + AZX.
Conservation de la charge : 19 = 18 + Z d'oý Z = 1
Conservation du nombre de nuclťons : 40 = 40 + A d'oý A = 0.
4019K
---> 4018Ag
+ 01e
( positon).
La radioactivitť est de type bťta + ( Ŗ+).
Dťfinir la demi-vie
radioactive notťe tĹ.
Durťe au
boutde laquelle la moitiť des noyaux initiaux se sont dťsintťgrťs ;
durťe au bout de laquelle l'activitť initiale est divisťe par
deux.
La demi vie radioactive du potassium 40 est tĹ =1,3 109
ans.
Donner la
valeur de la constante radioactive l.
l
tĹ =
ln 2 ; l = ln 2 / tĹ = ln 2 /1,3 109 =5,332 10-10
an-1 ~5,3 10-10 an-1.
|
|
Dans certaines roches volcaniques on dťcŤle la
prťsence de potasium 4019K radioactif. Lors
d'une ťruption volcanique, tout l'argon sťvapore sous l'effet des
conditions de tempťrature et de pression / on dit que la lave se
dťgaze. A cette date, considťrťe comme instant initial t=0, la lave
volcanique se solidifie et ne contient pas d'argon. Plus tard, ŗ
l'instant t, on effectue un prťlevement de roche sur le site volcanique
ancien. Un spectrographe dťtermine la composition massique de ce
prťlevement , qui contient, entre autre : mK= 1,57 mg de 4019K
et mAr= 82,0 mg de 4018Ar.
M(K) voisin M(Ar) = 40,0 g/mol ; NA= 6,02 1023 mol-1.
|
Dťterminer
le nombre d'atomes de potassium 40 ( NK) et le nombre
d'atomes d'argon 40 ( NAr) ŗ la date t.
nombre d'atomes de potassium 40 ( NK) et le nombre
d'atomes d'argon 40 ( NAr) ŗ la date t :
NK= mK /M(K) * NA=1,57 10-3
/ 40 *6,02 1023 = 2,36 1019 atomes
NAr= mAr /M(Ar) * NA=82 10-6
/ 40 *6,02 1023 = 1,23 1018 atomes
On note N0 le nombre d'atomes de potassium 40
contenus ŗ la date t=0 dans la roche prťlevťe ŗ la date t.
Justifier
la realtion N0= NK+NAr.
ŗ t=0 : N0= NK(t=0)
Chaque fois qu'un noyau de potassium 40 se dťsintŤgre il se
forme un noyau d'argon 40 : ŗ la date t, N0-NK
atomes de potassium 40 ont disparu ;
il s'est formť NAr =N0-NK atomes
d'argon 40. D'oý : N0 =NAr +NK.
Exprimer le
nombre d'atome NK(t) de potassium 40 en fonction de t, N0,
l
Loi de dťcroissance radioactive : NK(t) = N0
e(-lt) soit
ln(NK(t) / N0 ) = l t.
Dťterminer
la date approximative de l'ťruption.
t = -1/l ln(NK(t) / N0
) =-1/5,33 10-10 ln(2,36 1019 / 2,48 1019)
= 9,5 107 ans.
Spectrophotomťtrie.
A l'aide d'un
spectrophotomŤtre, on rťalise une sťrie de mesures d'absorbance A de
solutions de violet cristallisť, ŗla longueur d'onde
l= 580 nm. La cuve a une ťpaisseur l =1 cm. On obtient les
rťsultats suivants en fonction de la concentration massique r des solutions :
|
r gL-1
|
0,6 10-3
|
1,5 10-3
|
2,4 10-3
|
3 10-3
|
4,5 10-3
|
6 10-3
|
|
A
|
0,075
|
0,25
|
0,42
|
0,515
|
0,775
|
1,04
|
Donnťes : violet cristallisť C25H30N3
; M=408,19 g/mol
Dťfinir la
transmittance T et l'absorbance A d'une solution.
La transmission T est dťfinie comme le rapport de l'intensitť
transmise I ŗ l'intensitť incidente I 0.
T = I / I0
; log T= -A.
Enoncer
la loi de Berr-Lambert; expliciter tous ces termes et donner leurs
unitťs.
A= log (I0/I) = elc ( A est l'absorbance ou densitť optique)
oý e est un coefficient caractťristique de la
substance appelť coefficient d'absorbance ( L
mol-1 cm-1), l est l'ťpaisseur de la cuve ( cm) et c la
concentration de la solution ( mol/L).
Quel
est le critŤre de choix de la longueur d'onde ŗ laquelle s'effectue les
mesures ? Pourquoi ?
Les solutions colorťes prťsentent une longueur d’onde lumineuse oý
l’absorption est maximale. Cette longueur d’onde maximale l max ne dťpend pas de la
concentration, c’est une grandeur caractťristique de l’ion absorbant.
Elle est utilisťe pour effectuer les mesures photomťtriques sur des
solutions de diffťrentes concentrations.
Montrer
que la loi de Berr est vťrifiťe pour cette sťrie de solution.
|
r gL-1
|
0,6 10-3
|
1,5 10-3
|
2,4 10-3
|
3 10-3
|
4,5 10-3
|
6 10-3
|
|
A
|
0,075
|
0,25
|
0,42
|
0,515
|
0,775
|
1,04
|
|
r /A gL-1
|
8 10-3
|
6 10-3
|
5,7 10-3
|
5,8 10-3
|
5,8 10-3
|
5,76 10-3
|
r /A ťtant ŗ peu prŤs constant,
la loi de Beer est vťrifiťe.
r /A = 5,8 10-3 g L-1.
Dťterminer
la valeur du coefficient d'absorption molaire du violet cristallisť.
C/A=5,8 10-3 / masse molaire (g/mol) = 5,8 10-3
/408,19 =1,42 10-5 mol/L = 1,42 10-2 mol m-3.
r /A = 1 /(el)
avec largeur l = 10-2 m ;
1,42 10-2 = 1/(10-2 e ) = 100 / e soit e = 100 /1,42 10-2 = 104
/1,42 =7042 m2 mol-1.
ou bien : 1,42 10-5= 1/(1* e ) soit e = 1/1,42
10-5=70420 Lmol-1
cm-1.
La mesure de l'absorbance d'une solution de violet
cristallisť de concentration inconnue, rťalisťe dans ces conditions,
donne A= 0,631. Dťterminer
la concentration molaire c et la concentration massique r de cette solution.
si A= 0,631 alors C/A= 1,42 10-5 mol/L soit
C= 0,631*1,42 10-5 = 8,96 10-6 mol/L
r = 8,96 10-6*408,19
=3,66
10-3 g/L.
|
|
|
Structure cristalline :
Donnťes : masse molaire du calcium M(Ca) = 40,1 g/mol ; NA = 6,02 1023 mol-1 ;
rayon atomique du calcium ra = 0,197 nm.
Le calcium est un mťtal blanc argentť qui cristallise dans le rťseau cubique ŗ faces centrťes.
Reprťsenter une maille du cristal mťtallique.
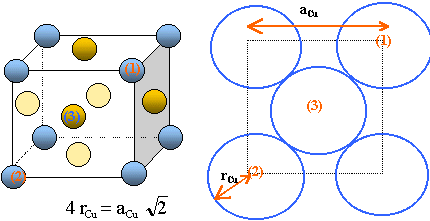
Dťterminer le nombre x d'atomes de calcium dans la maille.
Les atomes des sommets apartiennent ŗ 8 mailles et comptent pour 1/8 ;
les atomes aux centres des faces appartiennent ŗ 2 mailles et comptent pour Ĺ.
x = 8(1/8) + 6(1/2) = 4.
On appelle a la longueur de l'arÍte d'une maille cristalline.
Dťterminer l'expression littťrale de a en fonction du rayon atomique ra du calcium, puis calculer a.
Les atomes tangents sont situťs sur la diagonale
de chaque face.
4 ra = a 2Ĺ ; a = 4 ra / 2Ĺ ; a = 4 * 0,197 / 1,414 = 0,557 nm.
Exprimer la masse volumique r du calcium en fonction de x, a, NA et M(Ca).
volume du cube : a3 ; masse = x fois masse d'un atome de calcium = x MCa / NA
masse volumique :
r = x MCa / (NAa3)
Quel est le produit ( nom et formule) de la calcination du carbonate de calcium ?
Oxyde de calcium ou chaux vive CaO.
|
|
