|
fermentation alcoolique des jus sucrés concours chimie Capes 2007. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Dans la fabrication de la bière on utilise le malt ( orge germée et séchée) comme matière première. Au cours du brassage, le malt est broyé puis mis en suspension dans l'eau. L'amidon, principal constituant du malt, subit une transformation chimique et l'on obtient le moût. Le moût est ensuite soumis à la fermentation alcoolique. L'amidon est transformé en sucres, maltose puis glucose, par les enzymes développées lors du maltage, au cours du brassage. La fermentation : cette étape consiste à ensemencer le moût avec des levures ; celles-ci transforment les sucres présents en alcool et en CO2. On s'intéresse à la première étape de la fermentation alcoolique qui fait intervenir une enzyme E1 : G + ATP = GPh + ADP ( R1) catalysée par E1. on note G : glucose ; ATP : adénosine triphosphate ; ADP: adénosine diphosphate ; GPh : glucose phosphate ; E1 : hexokinase. Cette réaction peut être décomposée en trois étapes élémentaires : E1 + G =E1G (R2) équilibre rapide de constante thermodynamique K2. E1G + ATP --> GPh + E1 + ADP (R3) étape limitante, non inversable de constante de vitesse k3. GPh + E1 = GPhE1 (R4) équilibre rapide de constante thermodynamique K4. La réaction (R4) traduit l'inhibition de l'enzyme E1 par le produit de la réaction R3, c'est à dire GPh. Les activités seront assimilées aux concentrations. On note [E1]0 la concentration initiale de l'enzyme E1. Bilan de matière sur l'enzyme
E1 : [E1]0
=[E1]
+ [E1G]
+ [GPhE1]
v1 = k3[E1G][ATP]
Lors d'une campagne expérimentale, on a pu mesurer la vitesse initiale v1,0 dans les conditions suivantes : [E1]0 =1 10-6 mol/L ; [ATP]0 =5 10-2 mol/L ; [ADP]0 =0 mol/L ; Les concentrations initiales et les résultats obtenus sont consignés dans le tableau suivant :
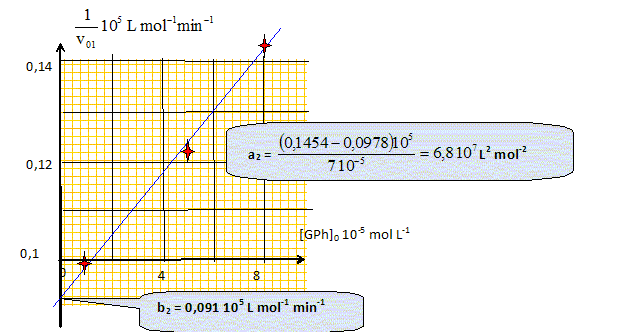
Exploitation des 4 premières expériences. Montrer que 1/v1,0 et 1/ [G]0 sont liées par une relation affine du type : 1/v1,0 = b1 + a1 * 1/ [G]0. Préciser les unités et les valeurs des constantes a1 et b1.
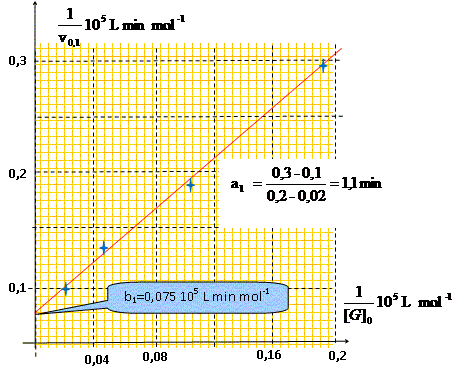
Utiliser la constante b1 pour trouver k3 en précisant son unité. à t=0, [GPh]0 = 10-5 mol/L = constante ; K4[GPh]0 est constant.
k3 =1/(7,5 103 *10-6*5 10-2 )=2,7 103 L min-1 mol-1.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|