|
Corrosion du fer, machine frigorifique, capteur de température, Bts FEE 2009 |
|||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||
|
On recueille les eaux de ruissellement dans une cuve en acier (alliage de fer). Elle contient un volume d'eau : Veau = 10 m3. Donnée : constante d'autoprotolyse de l'eau : [H3O+][HO-]= 10-14 à 25°C.. L'eau de la cuve a un pH de 5,2. Calculer la concentration molaire en ions H3O+ et HO-. [H3O+] = 10-pH = 10-5,2 =6,3 10-6 mol/L. [HO-]= 10-14/[H3O+] =10-14/10-5,2 =10-8,8 =1,6 10-9 mol/L. Calculer la quantité de matière d'ions H3O+ présents dans l'eau. 10 m3 = 104 L ; n = Veau * [H3O+] =104 * 6,3 10-6 = 6,3 10-2 mol. On souhaite neutraliser l'eau de la cuve en ajoutant de la soude. Quelle est la valeur du pH de l'eau après neutralisation ? Dosage acide fort base forte : à l'équivalence le pH est égal à 7 à 25°C. Ecrire l'équation de la réaction de neutralisation entre les ions H3O+ et HO- . H3O+ aq+ HO- aq = 2 H2O (l). La cuve est à l'air libre et se corrode. Citer un agent responsable de la corrosion du fer. Le dioxygène de l'air. Ecrire la demi-équation électronique du couple Fe2+/ Fe. Fe2+aq+ 2e- = Fe(s) L'eau de la cuve contient du dioxygène dissous. La demi-équation électronique du couple O2 aq / H2O(l) s'écrit : O2 aq + 4H+aq + 4e- =2 H2O(l) Donner l'équation chimique de la réaction entre le dioxygène dissous dans l'eau et le fer. O2 aq + 4H+aq + 4e- =2 H2O(l) 2 Fe(s) = 2Fe2+aq+ 4e- Citer une méthode de protection de la cuve contre la corrosion. Recouvrir le fer d'une epinture antirouille ; relié le fer à une anode sacrificielle en magnésium. Le fluide frigorigène subit les
transformations réversibles suivantes : - en A, (entrée du compresseur ) la
vapeur saturée, est à la
température T1 = 243 K et
à la pression p1 =1,51 bar. Elle
est comprimée adiabatiquement jusqu'à
la pression p2 =5,67 bar (trajet A-B :
compresseur). On note T2 la
température du fluide en B. - La vapeur sèche subit une
transformation isobare dans le condenseur
jusqu'à liquéfaction totale (trajet
B-C). - En C, le fluide est à l'état de
liquide saturé à la
température T3 = 293 K . Il est
détendu de manière isenthalpique
jusqu'à la pression p1. (trajet
C-D). - Enfin, le fluide entre dans
l'évaporateur où le liquide restant
se transforme en vapeur saturée à la
température T1 = 243 K (trajet
D-A). Données : le fluide dans son
état gazeux se comporte comme un gaz
parfait. Rapport des chaleurs massiques : g=
cP/cV =1,2 ; cP =
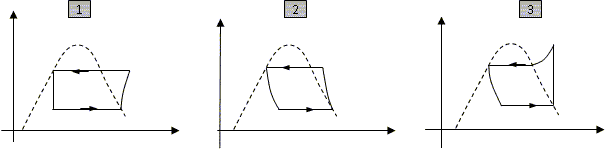
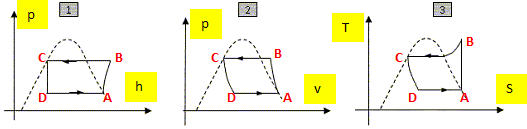
480 J kg-1 K-1. Sur la figure du document annexe (à rendre avec la copie), choisir les couples de grandeurs (p, v) ; (p, h) et (T, s) adaptés à chaque graphe et placer les grandeurs sur les axes correspondants. Placer les points A, B, C et D sur chacun des trois graphes. Dans une machine frigorifique, le cycle est décrit dans le sens anti-horaire. Dans le diagramme (T s ) la compression adiabatique A --> B, correspond à un segment vertical. La température augmente de T1 à T2. Dans le diagramme (p h ) la détente isenthalpe C --> D, correspond à un segment vertical. Dans le diagramme (p v ) la transformation isobare B --> C, correspond à un segment horizontal.
La pression de la vapeur sèche à la sortie du compresseur est p2 = 5,67 bar . Montrer que la température T2 du fluide en fin de compression est égale à 303 K. Transformation adiabatique réversible A--> B : PVg = cste. Loi des gaz parfaits PV = nRT ; V = nRT/P d'où : P1-g Tg = cste ; P(1-g) / g T = cste. P1(1-g) / g T1 =P2(1-g) / g T2 ; T2 =T1 [P1 / P2](1-g) / g T2 =243 [1,51/5,67]-0,2/ 1,2 =243*1,246 =303 K. En utilisant le premier principe de la thermodynamique, établir l'expression du travail massique fourni par le compresseur au fluide (travail de transvasement) en fonction de cP , des températures T1 et T2 puis faire l'application numérique. DhAB = WAB + QAB avec QAB = 0 ( adiabatique) et DhAB =cp ( T2-T1) WAB =cp ( T2-T1) = 480 (303-243) =28,8 103 ~ 29 kJ kg-1.
En déduire la valeur de l'enthalpie massique du fluide au point B. DhAB =hB-hA ; hB = hA + DhAB =338 + 28,8 = 366,8 ~ 3,7 102 kJ kg-1. Exprimer littéralement la quantité de chaleur massique cédée par le fluide, entre les points B et C, en fonction de cP , T2,T3 et L (chaleur latente de liquéfaction à la température T3 ). Faire l'application numérique en prenant L = -143 kJ kg-1. Transformation isobare dans le condenseur : QBC = DhBC + L = cp(T3-T2) + L. QBC = 480 (293-303) -143 103 = (-4,8 -143)103 = -147,8 kJ kg-1 ~ 1,48 102 kJ kg-1. On donne l'enthalpie massique du liquide saturé à la pression p1=1,51 bar et à la température T1 =243 K ; hliq =173 kJ kg-1. Déterminer l'enthalpie massique du fluide au point D. "isenthalpique jusqu'à la pression p1. (trajet C-D)" DhCD =0 ; hD-hC = 0 ; hD=hC =219 kJ kg-1. Déterminer le titre vapeur xv en ce point. xV = (hD-hliq) / (hA-hliq) =(219-173) / (338-173) = 0,279 ( 28 %). Exprimer l'efficacité de ce système réfrigérant en fonction des enthalpies massiques hA, hB et hD. Faire l'application numérique. Chaleur retitée à la source chaude / travail investi = QDA / WAB = (hA-hD) / WAB. efficacité = (338-219) / 28,8 = 4,1.
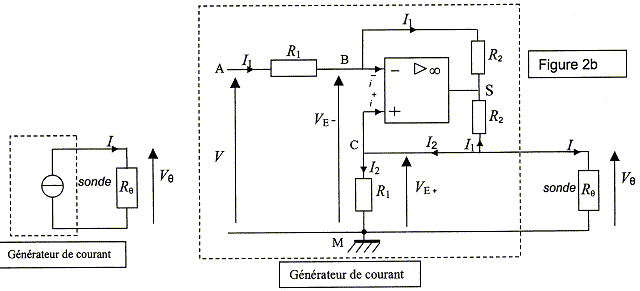
Le capteur de température est constitué par une résistance Rq alimentée par un générateur de courant.
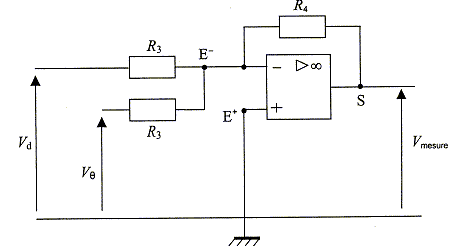
Pour des températures q comprises entre -50°C et +100°C , la résistance du capteur est donnée par la relation Rq =R0(1+a q ) avec R0=100 ohms et a=4,0 10-3°C-1. Dans tout le problème, les amplificateurs opérationnels sont parfaits, ils fonctionnent en régime linéaire ; ainsi : VE+=VE-=Vq ; i+ = i- =0 ; Vsat+ = + 15 V ; Vsat- = -15 V. Etude du générateur de courant. Le capteur est traversé par un courant d'intensité I constante, produit par un générateur de courant. On donne R1 =1,0 kW, R2 =10,0 kW et V = 1,0 V. Les deux résistances R2 sont traversées par des courants ayant la même intensité (représentée par I1 sur le schéma). Exprimer I1 en fonction de V, VE+ et R1. V = R1 I1 + VE+ ; I1 = (V-VE+ ) / R1. Exprimer I2 en fonction de VE+ et R1. VE+ = R1I2 ; I2 = VE+ / R1. En déduire que l'intensité I du courant dans la sonde a pour expression : I = -V/R1. Calculer sa valeur numérique. Loi des noeuds : I1 + I2 +I = 0 ; I = -I1 - I2 =[- (V-VE+) -VE+ ] / R1 = -V/R1 = - 1,0 / 1,0 103 = -1,0 10-3 A. Quel est l'intérêt de maintenir l'intensité I constante dans la résistance ? Vq = RqI ; si I est constante, la tension aux bornes du capteur est proportionnelle à Rq ; Rq - R0 est de plus proportionnelle à la température. Montrer que la tension Vq aux bornes du capteur peut s'écrire : Vq =-0,10 -4,0 10-4 q. En déduire les valeurs de Vq pour q= 0°C et pour q= 100°C. Vq = RqI = -RqV / R1 =-R0(1+a q )V / R1 = -100(1+4,0 10-3q )*1,0 / 1,0 103 = -0,10 - 4,0 10-4q. V0 = -0,10 V ; V100 = -0,14 V.
|
|||||||||||||||||||||||||||
|
|