|
|
||||||||
|
||||||||
|
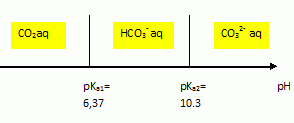
Elťment calcium. Le symbole chimique du calcium ťtant 4020Ca, justifier la forme stable Ca2+ de cet ťlťment ŗ partir de sa structure ťlectronique. L'atome de calcium compte 20 ťlectrons : 1s2 2s2 2p6 3s2 3p6 4s2. L'ion calcium compte 18 ťlectrons : 1s2 2s2 2p6 3s2 3p6. La couche ťlectronique externe de l'ion Ca2+ est complŤte ŗ 8 ťlectrons : cet ion est donc stable. Le numťro atomique du carbone ťtant 6, celui de l'oxygŤne ťtant 8, donner la formule de Lewis de la molťcule de dioxyde de carbone. Donner sa gťomťtrie. La molťcule de dioxyde de carbone est linťaire. 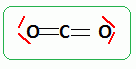 L'ťlťment calcium est essentiellement prťsent sur Terre sous forme de carbonate de calcium ( calcaire). Le carbonate de calcium est utilisť pour la fabrication de la chaux (CaO) par calcination. La transformation correspond ŗ l'ťquilibre chimique dťcrit par l'ťquation chimique suivante : CaCO3(s) = CaO(s) + CO2(g). Proposer un moyen simple de dťplacer l'ťquilibre en faveur de la production de chaux. En ťliminant l'un des produits ( ici le dioxyde de carbone gazeux ) au fur et ŗ mesure qu'il se forme, on dťplace l'ťquilibre dans le sens direct, formation de chaux. Les eaux souterraines. De l'eau initialement pure dans une rťgion volcanique se retrouve dans une cavitť calcaire profonde. La tempťrature y est de 25 įC et la pression partielle du dioxyde de carbone PCO2 est constante et ťgale ŗ 0,35 bar. Le calcaire se dissout partiellement dans cette eau de mÍme que du dioxyde de carbone. Le calcaire sera assimilť ŗ du carbonate de calcium CaCO3(s) ; le terme concentration dťsigne la concentration molaire ; on ne considŤrera que les transformations chimiques dťcrites par les ťquations chimiques suivantes et leurs constantes d'ťquilibre ŗ 25įC indťpendantes de la pression. CaCO3(s) = Ca2+aq + CO32-aq ; Ks =[Ca2+aq] [CO32-aq] = 4,47 10-9. CO2(g) = CO2 aq ; PCO2 = 30,1 [CO2 aq] CO2 aq + 2H2O(l) =HCO3-aq + H3O+aq ; Ka1 = [H3O+aq][HCO3-aq] / [CO2 aq] = 4,25 10-7. HCO3-aq + H2O(l) =CO32-aq+ H3O+aq ; Ka2 = [H3O+aq][CO32-aq] / [HCO3-aq] = 5,61 10-11.
Ka1 = [H3O+aq][HCO3-aq] / [CO2 aq] et PCO2 = 30,1 [CO2 aq] Ka1 = 30,1[H3O+aq][HCO3-aq] / PCO2. [HCO3-aq] = Ka1PCO2 / (30,1[H3O+aq]). Dťterminer
l'expression littťrale de [Ca2+aq ] ŗ l'ťquilibre en fonction de Ka1,
Ka2, Ks,
PCO2 et [H3O+aq
]. Les ťquations trouvťes donnent : [Ca2+aq] =1,61 1010[H3O+aq]2 et [Ca2+aq]= 2,47 10-9 / [H3O+aq]. Calculer
[Ca2+aq]
et [H3O+aq] ŗ l'ťquilibre. Dťterminer
le pH et la concentration en ion carbonate.
Cette mÍme eau est pompťe jusqu'ŗ la surface oý la pression partielle de dioxyde de carbone est plus faible et ťgale ŗ 3,5 10-4 bar. La tempťrature reste ŗ 25 įC. Justifier l'apparition de bulles dans l'eau lorsque celle-ci arrive en surface. Si la pression partielle PCO2 diminue, alors [CO2 aq] diminue et l'ťquilibre CO2(g) = CO2 aq est dťplacť dans le sens indirect, formation de CO2(g). Pendant le pompage, le pH de l'eau augmente jusqu' ŗ une valeur proche de 8. Expliquer pourquoi la rťponse prťcťdente est cohťrente avec l'augmentation du pH. [CO2 aq] diminue : l'ťquilibre CO2 aq + 2H2O(l) =HCO3-aq + H3O+aq est dťplacť dans le sens indirect : diminution de [HCO3-aq] et de [H3O+aq]. [HCO3-aq] diminue : l'ťquilibre HCO3-aq + H2O(l) =CO32-aq+ H3O+aq est dťplacť dans le sens indirect : diminution de [CO32-aq] et de [H3O+aq]. La concentration [H3O+aq] diminue et en consťquence, le pH augmente. Pendant le pompage, la concentration en ion calcium passe de 4,6 10-3 mol/L en profondeur ŗ 3,6 10-3 mol/L en surface. Une partie des ions calcium prŤcipite sous forme de calcaire qui entartrera les canalisations. Dťterminer la masse de calcaire CaCO 3 ( M = 100 g/mol) qui se dťpose pour un volume V = 1000 L d'eau puisťe. Diffťrence de quantitť de matiŤre par litre d'eau : 4,6 10-3 -3,6 10-3 =1,0 10-3 mol Soit pour 1000 L d'eau : 1,0 mol ou 100 g de calcaire. Le produit de solubilitť de l'hydroxyde de calcium Ca(OH)2 est K's = [Ca2+aq][HO-aq]2= 8,0 10-6. Calculer le pH de prťcipitation de l'hydroxyde de calcium si [Ca2+aq] = 3,6 10-3 mol/L en surface. [HO-aq]= ([K's / [Ca2+aq])Ĺ =([8,0 10-6/ 3,6 10-3)Ĺ =4,71 10-2 mol/L pOH = -log (4,71 10-2 )=1,33 d'oý pH = 14-pOH =14-1,33 =12,7 ~ 13. L'hydroxyde de calcium ne prťcipite pas en surface car le pH de l'eau est bien infťrieure ŗ la limite du pH de prťcipitation.
Dťtecteur thermostatique. Le dťtecteur comporte une thermistance dont la caractťristique est donnťe : 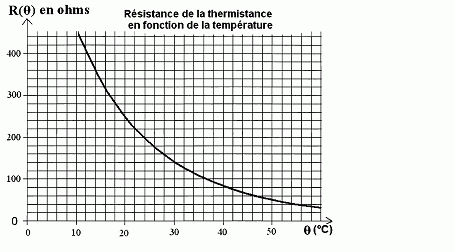 Dťterminer la sensibilitť "s" de la thermistance ( variation de sa rťsistance en ohm par degrť celsius ŗ la tempťrature q = 32 įC. Tracer la tangente ŗ la courbe ŗ q = 32 įC et dťterminer son coefficient directeur. 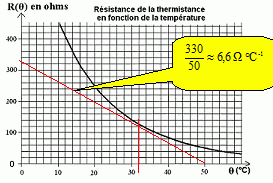 Cette thermistance de rťsistance R(q) et un conducteur ohmique de rťsistance R' rťglable sont insťrťs dans le montage suivant : 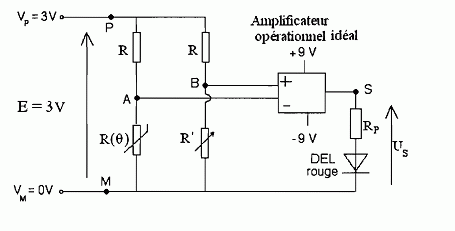 Quelle est l'utilitť du conducteur ohmique RP ? Protection de la diode contre une surintensitť. A quelle condition, sur les tensions US et UAB la diode considťrťe comme idťale est allumťe ? US doit Ítre positive ( + 9 V) : l'AO, fonctionnant en comparateur, doit Ítre saturť ŗ l'ťtat haut. Le potentiel de l'entrťe B doit Ítre supťrieur ŗ celui de l'entrťe A : VB-VA = UBA >0. La tension UAB doit donc Ítre nťgative. La diffťrence de potentiel entre les points A et B a pour expression :  On veut que la diode s'allume dŤs que la tempťrature est supťrieure ŗ 22 įC. Dťterminer la valeur de R'. 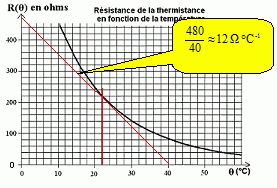 UAB < 0 ou nul ; R(q) - R'< ou nul ; R(q) = R' ; R' = R(22įC) = 12*22 ~2,6 102 ohms. |
||||||||
| |
||||||||
|
|