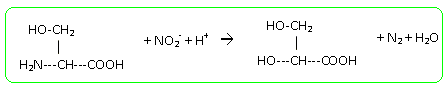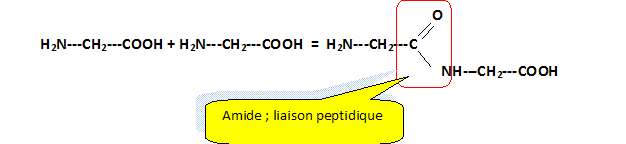|
Autour d'acide a-aminťs naturels : sťrine et glycine, synthŤse de l'anthranilate de mťthyle ( bac Stl chimie de laboratoire 2009) |
|||||||||||||||||||||||
|
|||||||||||||||||||||||
La sťrine a une masse molaire de 105 g/mol ; sa composition centťsimale massique est : % C = 34,3 ; % H = 6,7 ; % O = 45,7 ; % N = 13,3. Montrer que la formule brute de la sťrine est C3H7NO3. La formule brute est de la forme Cx Hy Oz Nt avec x, y, z et t entiers.
D'oý x = 1,05*34,3 / 12 = 3 ; y = 1,05 *6,7 = 7 ; z = 1,05*45,7 / 16 = 3 ; t = 1,05*13,3 / 14 = 1. sachant que la sťrine possŤde une fonction alcoolprimaire, en dťduire sa formule semi-dťveloppťe. Nommer la sťrine selon la nomenclature officielle.
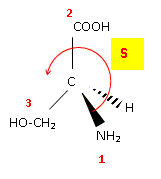
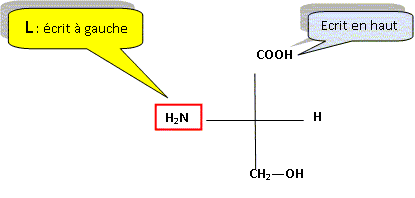
Dessiner un des ťnantiomŤres de la sťrine en reprťsentation de Cram puis dťterminer sa configuration absolue en justifiant soigneusement.
numťroter de faÁon dťcroissante chacun des quatre substituants selon son numťro atomique. NH2 (1) ; COOH (2) ; CH2OH (3) ; H (4). On place alors l'atome (ou le groupement) de numťro le plus ťlevť derriŤre. On regarde dans quel sens, sens horaire ou trigonomťtrique, on passe du numťro 1, au 2, au 3. - Si le sens de rotation est le sens horaire (ou anti-trigonomťtrique), le carbone est Rectus (R), - Si le sens de rotation est le sens trigonomťtrique (ou anti-horaire), le carbone est Sinister (S).
Ecrire l'ťquation de la rťaction dťcrite et nommer le produit B obtenu.
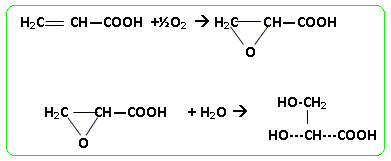
B : acide-2,3-dihydroxypropanoÔque. Le composť B peut Ítre ťgalement obtenu par l'ťpoxydation de l'acide propŤnoÔque, suivie de l'hydrolyse acide de l'ťpoxyde obtenu. Donner la formule semi-dťveloppťe de l'acide propŤnoÔque. Ecrire la formule semi-dťveloppťe de l'ťpoxyde intermťdiaire. Ecrire l'ťquation de la rťaction d'hydrolyse de l'ťpoxyde, conduisant ŗ B.
La glycine. Le nom officiel de la glycine est : acide 2-aminoťthanoÔque. Donner la formule semi-dťveloppťe de ce composť, ainsi que sa formule brute. H2N-CH2-COOH ; formule brute : C2H5O2N. Prťciser les propriťtťs acido-basiques des deux fonctions chimiques prťsentes dans la glycine. Donner la formule semi-dťveloppťe de l'espŤce prťpondťrante de la glycine en milieu trŤs acide, puis en milieu trŤs basique. La fonction amine -NH2 est une base ; la fonction acide carboxylique -COOH est un acide. En milieu trŤs acide, la forme H3N+-CH2-COOH prťdomine ; en milieu trŤs basique, la forme H2N-CH2-COO- prťdomine. La glycine peut rťagir avec elle mÍme pour donner un composť C, de formule brute C4H8N2O3. Ecrire l'ťquation de la rťaction mise en jeu, en utilisant d'abord les formules brutes. Indiquer la formule semi-dťveloppťe de C ainsi que le nom de la fonction chimique formťe lors de cette rťaction. C2H5O2N + C2H5O2N = C4H8N2O3 + H2O.
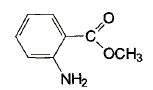
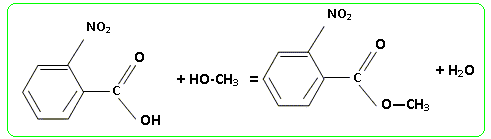
SynthŤse de l'anthranilate de mťthyle. L'anthranilate de mťthyle est un pesticide servant de rťpulsif ŗ oiseaux mais est ťgalement utilisť en parfumerie et dans l'industrie des arŰmes ( on retrouve la molťcule dans les fleurs d'oranger, jasmin, acacia...). Sa formule
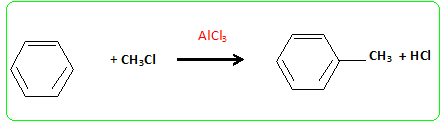
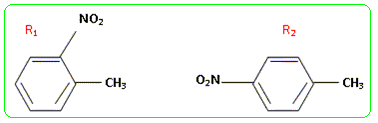
semi-dťveloppťe est : Pour rťaliser sa synthŤse, on rťalise une suite d'opťration ŗ partir du benzŤne : - rťaction 1 : on prťpare le toluŤne ŗ partir du benzŤne et de chloromťthane - rťaction 2 : le toluŤne est soumis ŗ l'action du mťlange sulfonitrique ŗ froid pour conduire ŗ deux composťs R1 ( dťrivť ortho ) et R2 ( isomŤre de R1) - rťaction 3 : R1 est oxydť par les ions permanganate en milieu acide : on obtient le produit S - rťaction 4 : S rťagit avec un rťactif appropriť, en prťsence d'acide sulfurique, pour conduire au 2-nitrobenzoate de mťthyle, composť T - rťaction 5 : T est rťduit par le dihydrogŤne en prťsence de carbonate de cuivre (II) ; on obtient alors l'anthranilate de mťthyle. Obtention du toluŤne. Ecrire l'ťquation de la rťaction en prťcisant les conditions opťratoires. La rťaction est une substitution : prťciser si elle est nuclťophile, ťlectrophile ou radicalaire. Indiquer le nom de la rťaction.
La rťaction est une substitution ťlectrophile du noyau benzťnique : alkylation de Friedel et Craft en prťsence d'un catalyseur AlCl3. Nitration du toluŤne. Donner les formules semi-dťveloppťes de R1 et R2. Indiquer la formule de l'espŤce ťlectrophile intervenant dans cette rťaction. L'espŤce ťlectrophile est : +NO2 : cation nitryle.
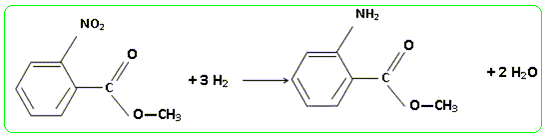
Obtention de l'anthranilate de mťthyle. Ecrire l'ťquation de la rťaction 5.
Nommer l'anthranilate de mťthyle suivant la nomenclature officielle. 2-aminobenzoate de mťthyle.
|
|||||||||||||||||||||||
|
|
|||||||||||||||||||||||
|
|
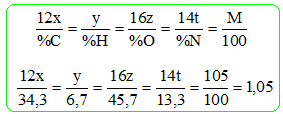
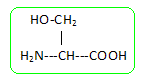 acide 2-amino-3 hydroxypropanoÔque
acide 2-amino-3 hydroxypropanoÔque