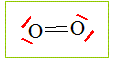|
Autour de l'oxygŤne, structure, dosage du dioxygŤne dissout, iodomťtrie concours Mines 03 |
|||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||
|
Donner la structure ťlectronique de l’atome 168O dans son ťtat fondamental. 1s2 2s2 2p4. L’oxygŤne existe sous la forme de trois isotopes de nombre de masse respectifs 16, 17 et 18. AprŤs avoir rappelť la dťfinition du terme ę isotope Ľ, prťciser la composition du noyau de chacun des isotopes de l’oxygŤne. Deux isotopes ne diffŤrent que par leur nombre de neutrons. Ils possŤdent le mÍme numťro atomique. 168O : 8 protons et 16-8 = 8 neutrons. 178O : 8 protons et 17-8 = 9 neutrons. 188O : 8 protons et 18-8 = 10 neutrons. Le plus important des corps purs simples formťs avec l’oxygŤne est le dioxygŤne O2. Proposer une formule de Lewis pour la molťcule de dioxygŤne.
L’ozone O3 est un gaz se caractťrisant par son odeur forte (ozone, du grec ozein : sentir). Proposez une formule de Lewis pour cette molťcule et prťciser la gťomťtrie de la molťcule (on prťcise que la molťcule d’ozone n’est pas cyclique).
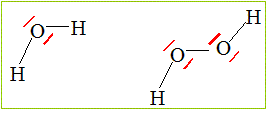
type AX2E2, en forme de V. L’eau H2O et l’eau oxygťnťe, ou peroxyde d’hydrogŤne, H2O2 sont deux molťcules contenant l’ťlťment oxygŤne. Proposer une formule de Lewis pour ces deux molťcules.
Une expťrience amusante consiste ŗ faire dťvier de sa trajectoire un mince filet d’eau ŗ l’aide d’une rŤgle ťlectrisťe. Comment interprťter simplement cette expťrience ? La molťcule d'eau est polaire.
L’eau contient en permanence du
dioxygŤne dissous ; ce dernier y est
consommť ŗ la fois par les systŤmes chimiques et biologiques qui
s’y trouvent. Le dosage du dioxygŤne
dissous dans une eau donnťe permet de dťterminer sa
qualitť : une concentration en
dioxygŤne trop faible est en effet signe de pollution. La mťthode de Winkler,
prťsentťe ici, est une mťthode
de dosage en retour, par iodomťtrie, du dioxygŤne dissous en solution
aqueuse. On ajoute 1,0 g de soude (ou hydroxyde de sodium) NaOH et 1,4 g de chlorure de manganŤse solide MnCl2(s). On bouche alors rapidement l’erlenmeyer en veillant ŗ ne pas y emprisonner d’air, et on agite le mťlange pendant 30 minutes environ. …crire l’ťquation traduisant la prťcipitation des ions Mn2+, provenant du chlorure de manganŤse, et des ions hydroxyde HO-, provenant de la soude, en hydroxyde de manganŤse (II). Le produit de solubilitť correspondant vaut KS = 2.10-13. Mn2+ aq + 2HO-aq = Mn(OH)2 (s).(1) Montrer que les ions hydroxyde sont en excŤs par rapport aux ions manganŤse (II). n(HO-) = m/MNaOH= 1,0/40 =2,5 10-2 mol n(Mn2+) = m/MMnCl2= 1,4/(55+71) =40 =1,1 10-2 mol D'aprŤs les nombres stoechiomťtriques de (1), 0,011 mol d'ion Mn2+ rťagit avec 0,022 mol d'ion hydroxyde. Or, initialement, il y a 0,025 mol d'ion hydroxyde : ce dernier est donc en excŤs.
4 Mn(OH)2(s) + O2(aq) + 2 H2O = 4 Mn(OH)3(s) (2) Ceci se traduit par l’apparition d’un prťcipitť brun dans l’erlenmeyer. Quel est le degrť d’oxydation (ou nombre d’oxydation) de Mn dans Mn(OH)2(s) et Mn(OH)3(s) ? Mn(OH)2 : n.o(Mn) + 2 n.o(H) + 2 n.o(O) = 0 ; n.o(Mn) +2 +2*(-2) = 0 ; n.o(Mn) = +II. Mn(OH)3 : n.o(Mn) + 3 n.o(H) + 3 n.o(O) = 0 ; n.o(Mn) +3 +3*(-2) = 0 ; n.o(Mn) = +III. Pourquoi a-t-on pris soin de boucher rapidement, et sans emprisonner d’air, l’erlenmeyer aprŤs avoir ajoutť la soude et le chlorure de manganŤse (II) ? Il faut ťviter que le dioxygŤne de l'air se dissolvent dans la solution. Le but de la manipulation ťtant le dosage du dioxygŤne dissous, quel composť, de Mn(OH)2(s) et de O2(aq), doit Ítre en excŤs ? Mn(OH)2(s) doit Ítre en excŤs : tout le dioxygŤne dissout doit rťagir avec Mn(OH)2(s).
Ceci a pour effet de rendre la solution acide et de dissoudre les hydroxydes du manganŤse selon les rťactions quantitatives et rapides suivantes : Mn(OH)3(s) formť + 3 H+ = Mn3+ + 3 H2O (3) Mn(OH)2(s) + 2 H+ = Mn2+ + 2 H2O (4) On admet qu’au pH oý se trouve ŗ prťsent la solution, le dioxygŤne dissous ne peut plus oxyder le manganŤse (II). Pourquoi l’ajout d’acide sulfurique doit-il Ítre rapide ? Est-il nťcessaire de reboucher l’erlenmeyer aprŤs cet ajout ? Avant l'ajout d'acide, il ne faut pas que le dioxygŤne de l'air se dissolvent dans la solution. AprŤs l'ajout, on peut laisser l'erlenmeyer ouvert, car il n'y a plus d'oxydation possible par O2 dissout en milieu acide. 4Ťme ťtape : On ajoute alors 3 g de iodure de potassium KI(s). …crire l’ťquation, notťe (5), traduisant la rťaction d’oxydorťduction se produisant entre les ions iodure I- et les ions manganŤse (III) Mn3+. 2I- = I2 + 2e-, oxydation 2Mn3+ + 2e- = 2Mn2+, rťduction. 2Mn3+ + 2I- = I2 +2Mn2+ (5) ; K = [Mn2+]2[I2] / ([I-]2[Mn3+]2) Calculer sa constante d’ťquilibre. Cette rťaction est elle quantitative ? E1 = Eį[I2/I-) + 0,03 log ([I2] / [I-]2) E2 = Eį[Mn3+/Mn2+) + 0,06 log ([Mn3+] / [Mn2+])= Eį[Mn3+/Mn2+) + 0,03 log ([Mn3+]2 / [Mn2+]2) A l'ťquilibre E1 =E2 : Eį[Mn3+/Mn2+)-Eį[I2/I-) = 0,03 log [Mn2+]2[I2] / ([I-]2[Mn3+]2)= 0,03 log K log K =(1,51-0,62)/0,03 = 29,7 ; K= 4,6 1029. K est trŤs grande, la rťaction est donc quantitative.
5Ťme ťtape : On pipette alors exactement V0 = 50,0 mL de cette solution que l’on dose par une solution de thiosulfate de sodium de concentration C = 1,0.10-2 mol.L-1, en prťsence d’empois d’amidon. Soit Ve le volume ŗ l’ťquivalence. …crire l’ťquation, notťe (6), traduisant cette rťaction de dosage. I2 + 2S2O32- = 2I-+S4O62-.(6) ņ quoi sert l’empois d’amidon ajoutť ? Indicateur de fin de rťaction : en prťsence de diiode, l'empois d'amidon donne une couleur violette foncťe. En utilisant les ťquations redox ťcrites, dťterminer la relation entre la concentration initiale en oxygŤne dissous dans cette eau, [O2(aq)], le volume ťquivalent Ve, le volume pipettť V0 et la concentration en thiosulfate de sodium C. d'aprŤs (6) : n(I2) = Ĺn(S2O32- ); V0[I2]==ĹCVe dans un volume V0 = 50 mL Soit pour un volume de 250 mL : n(I2) = 2,5CVe. d'aprŤs (5) : n(Mn3+) =2n(I2) d'aprŤs (3) : n(Mn3+) =n(Mn(OH)3) d'aprŤs (2) : n(O2) =0,25 n(Mn(OH)3) = 0,25 *2n(I2) = 1,25 CVe dans un volume de 250 mL (5 V0). [O2]= n(O2) / (5 V0) = 1,25 CVe / (5 V0) ; [O2] =0,25 CVe /V0. On obtient un volume ťquivalent Ve = 11,0 mL. Dťterminer la concentration en dioxygŤne dissout dans cette eau. [O2] =0,25 CVe /V0 = 0,25*0,01 *11/50 =5,5 10-4 mol/L. soit 32*5,5 10-4 = 1,8 10-2 g/L = 18 mg/L. Qualifier l’eau dosťe d’aprŤs le tableau prťsentť ci-aprŤs.
En considťrant les ťquations redox ťcrites, trouver la relation bilan entre O2 et I-. 4 Mn(OH)2(s) + O2(aq) + 2 H2O = 4 Mn(OH)3(s) (2) 4 Mn(OH)3(s) formť +12 H+ = 4Mn3+ + 12 H2O (3) 4Mn3+ +4I- = 2I2 +4Mn2+ (5) Faire la somme, d'oý : 4 Mn(OH)2(s) + O2(aq) +12 H+ +4I- =2I2 +4Mn2++ 10 H2O. Quel est donc le rŰle des ions Mn3+ ? L'ion manganŤse III n'apparaÓt pas dans ce bilan : il joue le rŰle de catalyseur. |
|||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||
|
|