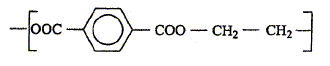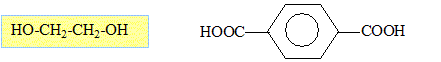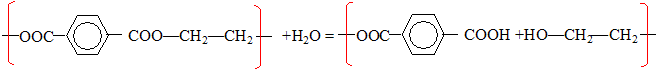|
Thermique, triphasé, matières plastiques bts Plasturgie 2002 |
|||||||||
|
|||||||||
|
Energie Q1 nécessaire pour élever la température de m=12 kg de polymère pris à q 1=18°C à la température de fusion qf=110°C. Capacité thermique massique du polymère solide : CS= 3200 J kg-1K-1. Variation d'enthalpie massique de fusion : DHf= 1,6 105 J kg-1. Q1 = m CS (qf - q 1) + m DHf. Q1 = 12*3200*(110-18) + 12*1,6 105 = 5,45 106 J. Energie Q2 nécessaire pour élever la température de m=12 kg de polymère fondu pris à qf=110 °C à la température d'injecion q=200°C. Capacité thermique massique du polymère fondu : Cf= 3100 J kg-1K-1. Q2 = m Cf (q- qf ). Q2 = 12*3100*(200-110) = 3,35 106 J. Energie Q nécessaire pour élever la température de m=12 kg de polymère pris à q1=18°C à la température q=200°C. Q = 5,45 106 + 3,35 106
= 8,8 106
J.
On donne la variation d'enthalpie massique de fusion pour un polyéthylène 100% cristallin : DHf0=2,8 105 J kg-1. Variation d'enthalpie massique correspondant à la fusion de ce polyéthylène. DHf= 3,4 / 21,2 10-6 = 1,6 105 J kg-1. On retrouve la valeur donnée au début de l'exercice. Taux de cristallinité Xc. Xc=
DHf
/ DHf0
*100 = 1,6/2,8*100 = 57
%.
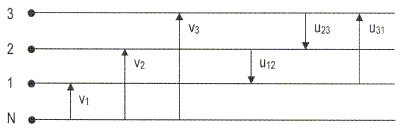
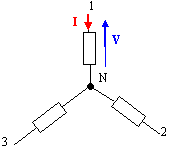
mode de transfert de chaleur
Calcul de la conductivité thermique l . P = l S(q2 -q1 ) / e. P : puissance (W) ; S = 10-2 m2 surface (m2) ; q1 , q2 : température en degré °C ; e = 8 10-3 m épaisseur en mètre ; l : conductivité thermique W K-1 m-1. l = P e / (S(q2-q1)) = 0,97 *8 10-3 / (10-2*2,5) = 0,31 W K-1 m-1.
Polyesters : Ecrire l'équation de la réaction entre l'acide éthanoïque et le propan-1-ol. CH3-COOH +CH3-CH2-CH2-OH = CH3-COO-CH2-CH2-CH3 + H2O Estérification conduisant à un équilibre. On peut déplacer l'équilibre en prenant un réactif en excès ou en éliminant du milieu réactionnel un produit au fur et à mesure qu'il se forme. Cette réaction est lente : on la rend plus rapide en chauffant et en utilisant un catalyseur. Thermoplastique : polymère ramolli par chauffage, durcissant au refroidissement ; la transformation est réversible. exemple : polyéthylène téréphtalate ( PET) Thermodurcissable : Sous l'action de la chaleur ils durcissent progressivement et atteignent un état solide ; la transformation est irréversible. exemple : tergal, nylon. Polycondensation : Les molécules initiales s'additionnent avec élimination d'une petite molécule ( H2O par exemple ). Les molécules initiales possèdent au moins deux fonctions réactives. Le PET est obtenu par polycondensation de l'acide téréphtalique ( acide benzène-1,4-dioïque) sur l'éthylène glycol. Son moti f est :
Formules semi-développées des monomères.
Le PET réagit avec l'eau dans le domaine de température correspondant à sa transformation par injection. Ecrire le bilan de la réaction avec l'eau d'un motif de polytéréphtalate déthylène. Dans quel sens varie la masse molaire moyenne en nombre du PET pendant la transformation. Hydrolyse de l'ester conduisant à l'acide caroxylique et à un alcool.
La masse molaire moyenne en nombre augmente. On transforme par injection un PET, de masse molaire moyenne en nombre 26000 g/mol, contenant 0,07% d'eau ( 0,07 g d'eau pour 100 g de PET. Calculer la quantité de matière d'eau correspondant à une mole de chaînes de PET. masse moalire de l'eau M = 18 g/mol. masse d'eau : 26000*0,07/100 = 18,2 g/mol 18,2 /18 ~1 mol d'eau. En supposant que l'eau contenue dans ce PET a réagit totalement sur le motif du polytéréphtalate d'éthylène durant la transformation par injection, calculer la masse molaire moyenne en nombre de ce PET après sa transformation et conclure. 26000 +18 = 26018 g/mol, variation pratiquement nulle (0,07 %).
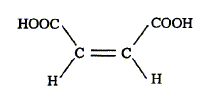
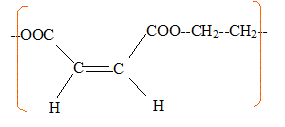
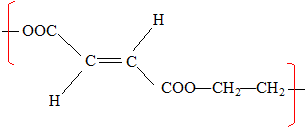
Quel type d'isomérie présente l'acide maléique : type d'isomérie Z E. Quel est la formule semi-développée du motif obtenu par réaction entre l'acide maléique et l'éthylène glycol ?
Le polyester obtenu est un copolymère. De quel type de copolymères s'agit-il ? Justifier. copolymères : polymère formé de plusieurs types de motifs de répétition.
On copolymérise avec le styrène les macromolécules de polyester. De quel type est le copolymère obtenu ? Justifier. |
|||||||||
|
|
|||||||||
|
|