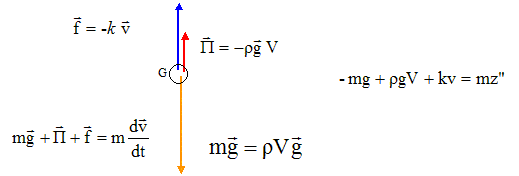|
Diplome d'accès
aux études universitaires B
vitesse limite de
chute, carbone14, dipoles RLC.
2006
|
|||
|
|||
|
Une bille de volume V = 0,50 cm3 et de masse m = 1,5 g a un mouvement de chute verticale dans un liquide de masse volumique r = 0,80 g. cm-3. Ce liquide exerce sur la bille une force de frottement de sens opposé à celui de la vitesse et de valeur f =k.v (k = 8.10-2 SI). Donnée : g = 9,8 m.s-2.
poussée : poids du volume de liquide déplacé F= V r g avec V r 0,5*0,8 = 0,4 g = 4 10-4 kg. F= 4 10-4 *9,8 = 3,92 10-3 N. Le poids est voisin de 3,5 fois la poussée : la poussée n'est pas négligeable devant le poids. La bille est soumise à son poids, à la poussée d'Archimède et à la force de frottements : Ecrire la seconde loi de Newton sur un axe verticale orienté vers le haut.
L'équation différentielle relative à la vitesse s'écrit : dv/dt -k/m v = g(rV/m-1). Vitesse limite : Lorsque la vitesse devient constante, dv/dt s'annule, d'où : -k/m vl = g(rV/m-1). vl =mg/ k (1- rV/m-). vl = 1,5 10-3*9,8/0,08 ( 1-4 10-4 / 1,5 10-3) ; vl = 0,135 m/s.
Exercice n°2 (7 points) DOCUMENT La Terre est bombardée en permanence par des particules très énergétiques venant du cosmos. Ce rayonnement cosmique est composé notamment de protons très rapides. Les noyaux des atomes présents dans la haute atmosphère " explosent " littéralement sous le choc de ces protons très énergétiques et, parmi les fragments, on trouve des neutrons rapides. Ces neutrons rapides peuvent à leur tour réagir avec des noyaux d'azote de la haute atmosphère. Lors du choc, tout se passe comme si un neutron rapide éjectait un des protons d'un des noyaux d'azote et prenait sa place pour former un noyau Y1. Ce noyau Y1 est un isotope particulier du carbone, le carbone 14, qui est radioactif : en émettant un électron et une particule non observable, l'antineutrino, il se décompose en un noyau Y2. La période ou demi-vie du carbone 14 est 5 570 ans. Comme le rayonnement cosmique bombarde la Terre depuis longtemps, un équilibre s'établit entre la création et la décomposition du carbone 14 : il y a autant de production que de décomposition si bien que la teneur en carbone 14 de tous les organismes vivants reste identique au cours du temps. Ce carbone s'oxyde en dioxyde de carbone qui se mélange à celui de l'atmosphère, à celui dissous dans l'eau, etc. et sera métabolisé par les plantes et à travers elles par tous les organismes vivants. Dans chaque gramme de carbone de l'atmosphère ou des organismes vivants, les atomes de carbone sont en très grande majorité des atomes de carbone 12, mais il y a 6,8 . 1010 atomes de carbone 14. D'après I. Berkès " La physique du quotidien ". On donne, pour différents noyaux : H : Z = 1 ; He : Z = 2 ; C : Z = 6 ; N : Z = 7 ; O : Z = 8. 1 an = 365 jours. I - Réactions nucléaires dans la haute atmosphère
I - Réactions nucléaires dans la haute atmosphère Le proton est représenté par le symbole 11H. Le proton est constitué d'une charge positive ( Z=1) et d'un seul nucléon (A=1). L'équation de la réaction qui a lieu
lorsque le neutron rapide éjecte un des protons du
noyau d'azote peut s'écrire : Conservation du nombre de nucléons : 14+1=A+1 d'où A=14 Le noyau de carbone 14 compte 6 protons et 14-6 = 8 neutrons.
146C = 147N + 0-1e radioactivité de type b-. II- Phénomène de décroissance radioactive Définition du temps de demi-vie t1/2. Durée au bout de laquelle l'activité initiale est divisée par deux. Relation entre la constante radioactive l et le temps de demi-vie t1/2. lt1/2
= ln2. t1/2 =5570 *365*24*3600 = 1,75 1011 s. l = ln2 /1,75 1011 = 3,96 10-12 s-1. Nombre de désintégrations par minute et par gramme de carbone d'un organisme vivant à partir du moment de sa mort : -DN =l. N D t = 3,96 10-12 *6,8 1010 *60 = 16,1. Pour un échantillon de 1 gramme et une durée de 1 seconde, l'activité sera égale à : 16,1/60 = 0,27 Bq.
III - Datation au carbone 14
La quantité moyenne de carbone 14 par kilogramme de matière (ou teneur) reste constante pour tous organismes en vie du fait des échanges entre l'organisme et l'atmosphère La teneur en carbone 14 diminue quand un organisme meurt : il n'y a plus d'échanges entre l'organisme et l'atmosphère. On date par la méthode du carbone 14 un morceau de sarcophage en bois trouvé dans une tombe de l'Égypte ancienne. Dans cet échantillon, on mesure en moyenne 10 désintégrations par minute et par gramme de carbone. Nombre de noyaux de carbone 14 subsistant dans cet échantillon : A= l N avec A= 10/60 = 0,167 Bq N= A/l = 0,167 / 3,96
10-12 =4,2
1010 noyaux. N=N0 exp(-lt) ; ln(N0/N) =lt ; t = ln(N0/N ) / l = ln (6,8/4,2) / 3,96 10-12 =1,22 1011 s = 3,86 103 ans.
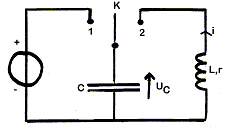
On réalise le circuit correspondant au schéma :
Le condensateur de capacité C = 15 mF est préalablement chargé à l'aide d'un générateur idéal de tension continue (interrupteur en position 1). Il se décharge ensuite (interrupteur en position 2) à travers un circuit comportant une bobine d'inductance L = 1,0 H et de résistance r. I - Étude du circuit
II Modélisation On suppose maintenant que l'oscillateur ne comporte aucune résistance. Dans ces conditions, la tension uC aux bornes du condensateur est de la forme : uC( t ) = Um sin (w0t + F) avec w0 = 2p/T0 = (LC)-½. où T0 est la période propre de l'oscillateur.
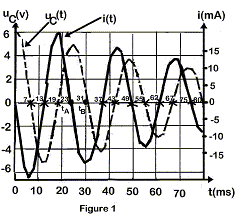
A partir des courbes la valeur de la
pseudo-période des oscillations vaut : 2T = 49 ms ;
T= 24,5 ms.. i = dq/dt avec q = CuC soit i =
CduC/dt. Étude
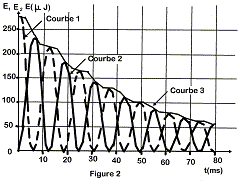
énergétique Courbe 1 : E1 = ½ CuC2 à t=0, le condensateur stocke toute l'énergie du dipole LrC. courbe 2 : E2 = ½ Li 2 à t =0,25 T, la bobine stocke toute l'énergie du dipole. courbe 3 : E = E1+E2. Lors des échanges d'énergie entre condensateur et bobine, une partie de l'énergie est perdue par effet joule dans les parties résistives : E décroît au cours du temps. II Modélisation On suppose maintenant que l'oscillateur ne comporte aucune résistance. Dans ces conditions, la tension uC aux bornes du condensateur est de la forme : uC( t ) = Um sin (w0t + F) avec w0 = 2p/T0 = (LC)-½. où T0 est la période propre de l'oscillateur. T0 = 2p (LC)½ = 6,28(1*15 10-6)½ = 24,3 ms. Expressions : ½CuC2 = ½C U2
m sin2 (w0t
+ F) ½Li2 avec i = CduC/dt =C Um w0 cos(w0t + F) ½Li2 =½LC2 U2m w20 cos2(w0t + F) Or LCw20
= 1 d'où ½Li2 =½C
U2 m cos2
(w0t
+ F) ½C U2 m cos2 (w0t + F) + ½C U2 m sin2 (w0t + F) = ½C U2 m = Constante.
|
|||
|
|