|
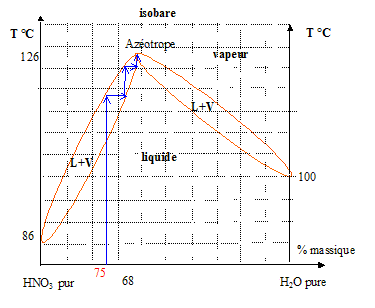
SystŤme binaire HNO3-H2O : ťquilibre liquide-vapeur |
||||
|
||||
|
Les constantes physiques du systŤme binaire HNO3-H2O sont les suivantes : T(ťbullition) : HNO3 : 86įC sous une pression de 1 atm ; H2O : 100įC sous une pression de 1 atm; Azťotrope : 121įC sous pression de 1 atm . (composition en masse de l'azťotrope : 68% HNO3-32% H2O )
Les fractions molaires, molalitť, molaritť de HNO3 dans l'azťotrope : 68 g d'acide nitrique dans 100 g de solution. masse molaire acide nitrique : M= 1+14+3*16 = 63 g/mol Quantitť de matiŤre d'acide nitrique (mol) = masse / masse molaire = 68/63 = 1,08 mol molalitť de l'acide nitrique : 10,8 mol dans 1000 g de solution : 10,8 mol / kg. 32 g d'eau dans 100 g de solution ; M(eau) = 18 g/mol) Quantitť de matiŤre (mol) d'eau : 32/18 = 1,78 mol d'oý la fraction molaire en acide nitrique : 1,08/ (1,08+1,78) = 0,37. volume correspondant ŗ 100 g de solution : 100 / densitť = 100/1,4 = 71,4 mL = 0,0714 L molaritť de l'acide nitrique : 1,08 /
0,0714 = 15,1 mol/L.
- de la vapeur qui par condensation et ťbullition successives, s'enrichit en eau : le distillat final aura la composition de l'azťotrope ( queue de distillation). Par contre, la tÍte de distillation aura pratiquement la composition du mťlange ( 75 % en masse d'acide nitrique) - Le bouilleur, par contre, va progressivement s'enrichir en acide nitrique.
|
||||
|
|