|
|
|||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||
|
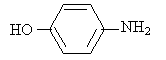
A- Synthèse du paracétamol : Les réactifs intervnant dans cette synthèse sont le para-aminophénol et l'anhydride éthanoïque ( ou acétique). La réaction modélisant la transformation chimique peut être symboliquement écrite sous la forme : para-aminophénol + anhydride éthanoïque =paracétamol + acide éthanoïque. Données :
Protocole : 1- synthèse : à l'aide d'un entonnoir, verser 3,10 g de para-aminoiphénol dans un ballon posé sur un valet et ajouter 10 mL d'eau mesurés à l'aide d'une éprouvette. A l'aide d'une pipette graduée, ajouter 4,0 mL d'anhydride acétique ( introduite en excès) puis chauffer le mélange à reflux pendant 30 minutes. Au bout de 30 minutes, retirer le ballon en abaissant le support élévateur et refroidir le mélange dans un bain d'eau froide. Il apparaît alors un solide blanc. 2- Filtration sur buchner : Préparer un montage de filtration sous le vide de la trompe à eau et filtrer le solide sur le buchner. Laver le solide deux fois avec environ 5 mL d'eau froide. Laisser sécher pendant 5 minutes et récupérer le solide sur une coupelle. 3- Recristallisation du produit obtenu : Placer le paracétamol brut obtenu dans un erlenmeyer avec 40 mL d'eau et le chauffer jusqu'à ébullition. Mettre l'erlenmeyer dans un bain d'eau glacée. Attendre la recristallisation et filtrer sous vide le contenu de l'erlenmeyer. Placer les cristaux à 80°C dans une étuve. Questions : Nommer et entourer les groupes fonctionnels intervenant
dans la para-aminophénol. 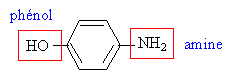
réponse : passage de l'état solide à l'état liquide.
réponse : la température de fusion d'un corps impur n'est pas constante. La température de
fusion d'un corps est d'autant plus élevée que les molécules sont
associées par liaisons hydrogène intramoléculaires.
réponse : C6H7ON
; M= 6*12+7+16+14 = 109 g/mol
réponse : port de lunette, blouse et gants ; travail
sous hotte ; utiliser une pipette surmontée d'un pipeteur.
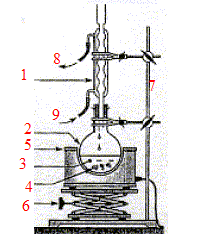
réponse : 1- réfrigérant droit à eau ; 2 -ballon ; 3- mélange réactionnel ; 4- pierre ponce ; 5- chauffe ballon ; 6- élévateur à croisillons ; 7- tige support ; 8- sortie de l'eau ; 9- arrivée de l'eau A quoi sert ce montage ? Quel est le rôle des pierres ponces ? Quel est le rôle du matériel n° 6 ? Ce montage à reflux permet d'accélérer la réaction en travaillant à température modérée ; il évite les pertes de matière : les vapeurs se condensent dans le réfrigérant et retombent dans le ballon. Les pierres ponces
régularisent l'ébullition ; l'élévateur à croisillons permet de monter
ou descendre le ballon ( chaud) sans se brûler.
réponse : pipette graduée voir éprouvette graduée.
Le lavage élimine les impuretés ; à froid le paracétamol est quasiment
insoluble dans l'eau.
réponse : la recristallisation est un procédé de purification. Dans le cas d'un
liquide , on aurait pu utiliser la distillation fractionnée. Le passage
à l'étuve élimine l'eau.( séchage)
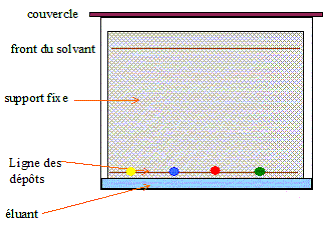
Dessiner et légender le schéma du montage expérimental à réaliser.
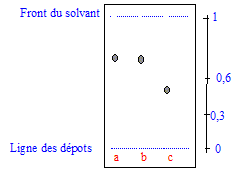
Donner l'allure du résultat observable sur la plaque de chromatographie si le pararcétamol fabriqué est considéré comme pur.
A et B ont le même rapport frontal dans un solvant donné : il s'agit du même produit pur. Quelle autre technique pourrait-on utiliser pour vérifier la pureté du paracétamol synthétisé ? réponse : :mesure du point de fusion sur un banc
Kofler.
|
|||||||||||||||||||||||||||
|
|