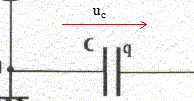|
Cinťtique de la rťaction entre l'acide oxalique H2C2O4 et l'ion permanganate MnO4- spectrophotomťtrie ; ťtude d'un condensateur. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
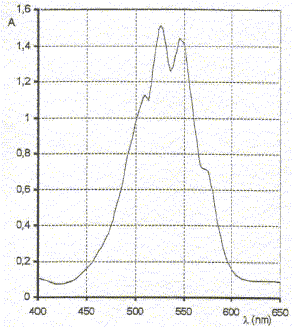
A- Rťglage du spectrophotomŤtre : on
doit rťgler la longueur d'onde de la lumiŤre pour laquelle l'absorption
de la solution est maximale. La seule espŤce chimique colorťe est l'ion
permenganate. On rťalise le spectre d'une solution diluťe de
permanganate de potassium, pour choisir cette longueur d'onde.
B- Etalonnage du spectrophotomŤtre : on mesure l'absorbance de solutions de concentrations connues de permanganate de potassium pour la longueur d'onde lf .
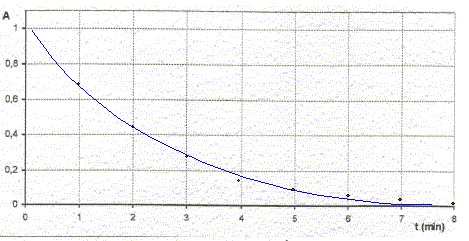
C- Suivi spectrophotomťtrique : dans un bťcher de 50 mL, on mťlange V1= 10,0 mL d'une solution de permanganate de potassium acidifiť de concentration C1 = 1,0 10-3 mol/L. On ajoute une pointe de spatule de nitrate de manganŤse Mn(NO3)2 : les ion Mn2+ jouent le rŰle de catalyseur. A la date t=0 on ajoute V2 = 10 mL d'une solution d'acide oxalique de concentration C2 = 1,0 10-2 mol/L. On homogťnťise et on verse une partie du mťlange dans la cuve du spectrophotomŤtre. Toutes les minutes on note la valeur de l'absorbance de la solution.
corrigť domaine et quelle gamme de longueur d'onde : dans l'intervalle [500 ; 560 nm] ( vert) l'absorption de la solution est trŤs grande. longueur d'onde lf pour faire les mesures d'absorbance de la solution de permanganate de potassium : 530 ou 550 nm La couleur des solutions de permanganate de potassium
est en accord avec le spectre d'absorption proposť : la solution
absorbe le vert ; la couleur complťmentaire du vert est le rose violet,
couleur de l'ion permanganate.
Prťparer ŗ partir de la solution C0 un volume de 100 mL de la solution C2. facteur de dilution F= C0 /C2 = 0,5/0,1 = 5 ; volume fiole jaugťe ( 100 mL) / volume pipette jaugťe = 5 Prťlever 20 mL de solution mŤre C0 ŗ l'aide d'une pipette jaugťe + pipeteur. Placer dans une fiole jaugťe de 100 mL et complťter avec de l'eau distillťe jusqu'au trait de jauge. agiter pour rendre homogŤne.
5 fois { C2H2O4 = 2 CO2 + 2H+ + 2e- }oxydation puis additionner : 2 MnO4- + 5 C2H2O4 + 16H+ + 10e- = 2 Mn2+ + 8 H2O+ 10 CO2 + 10H+ + 10e- 2 MnO4- + 5 C2H2O4 + 6H+ = 2 Mn2+ + 8 H2O+ 10 CO2 Quantitť de matiŤre initiale en acide oxalique (mol) = concentration (mol/L) * volume (L) n C2H2O4= V2C2 = 10 * 10-2 = 10-1 mmol n( MnO4- ) = V1C1 = 10 * 10-3 = 10-2 mmol
Les quantitťs de matiŤre sont en proportions stoťchiomŤtriques si : nMnO4- = 2/5 n C2H2O4 = 0,4*0,1 = 0,04 mmol Or on ne dispose que de 0,01 mmol MnO4- : ce dernier est en dťfaut ; l'acide oxalique est en excŤs.
vitesse volumique v de la rťaction en fonction de
l'avancement x : v = 1/VT
dx/dt avec VT (L) volume total du mťlange et x
avancement (mol)
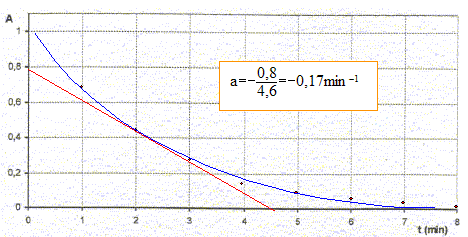
relation entre x et l'absorbance At : At = k [MnO4-]t ; n10 -x =AtVT /k ; [MnO4-] 0 VT -x = AtVT /k ; At= ĹC0 k -kx/ VT. expression de la vitesse volumique v en fonction de At, k et x : dAt/dt = -k/VT dx/dt ; dAt/dt = -k v ; v = -1/k dAt/dt Dťterminer le coefficient directeur de la tangente ŗ la courbe A=f(t) ŗ la date t= 2 min puis diviser par -k = -2 103 L/mol.
v = 0,17/2 103 = 8,4 10-5 mol L-1 min-1. La vitesse diminue au cours du temps car les coefficients directeurs des tagentes diminuent ( les tangentes se rapprochent de l'horizontale) Calcul de A0 : A0= Ĺ C0 k = Ĺ 10-3 * 2 103 = 1. temps de demi rťaction tĹ : durťe au bout de laquelle l'avancement est ťgal ŗ la moitiť de l'avancement final. xtĹ= Ĺxfin = 5 10-6 mol ; AtĹ = ĹC0 k -kxtĹ/ VT = 1-2 103*5 10-6 / 0,02 = 0,5 lecture graphe : tĹ voisin 1,7 min.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
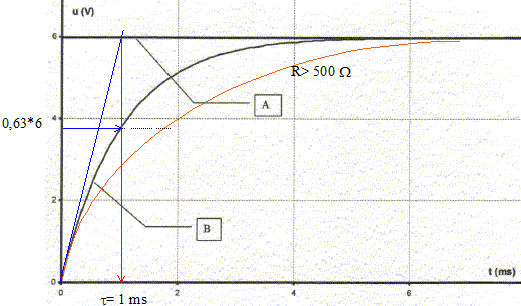
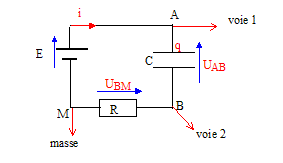
R= 500 W. Un oscilloscope ŗ mťmoire suit l'ťvolution temporelle des deux tensions. A la fermeture de l'interrupteur (t=0) le condensateur est initialement dťchargť. 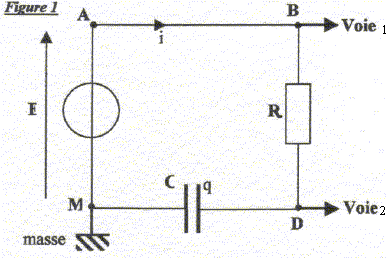
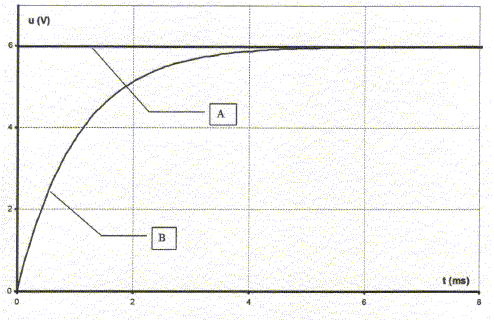
corrigť tensions mesurťes sur chaque voie : voie 1: uBM tension aux bornes du dipole RC ou bien tension E aux bornes du gťnťrateur de tension ; voie 2 : tension uDM aux bornes du condensateur. la courbe A montre une tension constante uBM =E=6 V La courbe B visualise une tension croissante (
exponentielle) au cours du temps : tension uDM
aux bornes du condensateur durťe pour charger complťtement le condensateur : en fin de charge tension uDM aux bornes du condensateur = E = 6 V d'oý la durťe : 5,2 ms ( lecture graphe) pour charger moins vite le condensateur, augmenter la constante de temps t= RC, donc prendre une plus grande valeur de R.
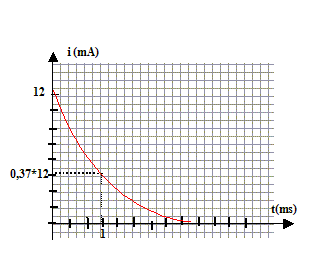
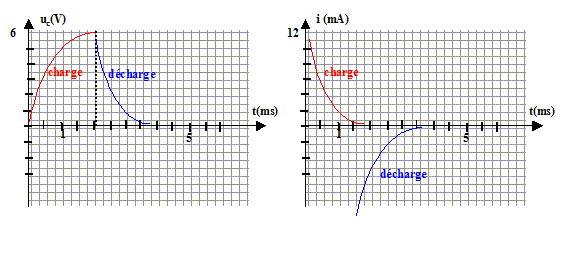
ťquation diffťrentielle relative ŗ uc: additivitť des tensions : E=uAM = uAD+uDM = Ri + uc. i = dq/dt et q=Cuc d'oý i= Cduc/dt. E= RCduc/dt +uc. duc/dt +uc/t =E/t avec t =RC uc = E[1-exp(-t/t)] ; duc/dt =E/t exp(-t/t) repport dans l'ťquation diffťrentielle E/t exp(-t/t) +E/t[1-exp(-t/t)] =E/(RC) vťrifiťe pout tout t si t=RC si t=t : uc/E= 1-exp(-1)= 1-0,37 = 0,63 ; si t=5t : uc/E= 1-exp(-5)=1-0,0067 = 0,993 ŗ t= 5t on peut considťrer que la charge du condensateur est ťgale ŗ 99 % de la charge complŤte. expression de i(t) : i(t) = Cduc/dt =E/R exp(-t/t) = I0exp(-t/t) avec I0 = E/R = 6/500 = 12 mA
L'allure de cette courbe i(t) pourait Ítre fournie par la tension aux bornes du rťsistor au facteur R prŤs : la tension aux bornes d'un rťsistor et l'intensitť qui le traverse sont proportionnelles.
L'intensitť est une fonction discontinue. La tension uc est une fonction continue.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|

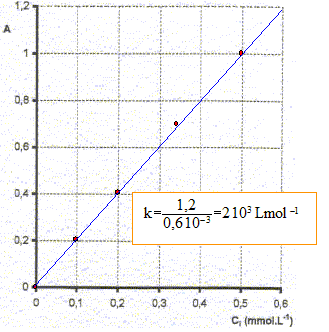 fonction linťaire A= k Ci
.
fonction linťaire A= k Ci
.