|
|
|||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||
|
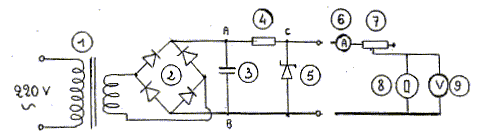 - Donner le nom de chaque élément numéroté : 1 : transformateur ; 2 : pont de diode ; 3 : condensateur ; 4 : résistor ; 5 : diode zener ; 6 : ampčremčtre ; 7 : rhéostat ; 8 : lampe ; 9 : voltmčtre - Préciser le rôle des éléments :1, 2, 3, 4, 5. 1 : modifie la valeur efficace de la tension alternative ; 2 : pont redresseur : ŕ sa sortie on obtient un courant variable mais qui ne change pas de sens ; 3 : permet d'obtenir une tension continue ; 4 : résistor de protection des diodes ; 5 : permet d'obtenir une tension continue stabilisée. - Quelle fonction assurent les éléments 1 ŕ 5 ? passage d'une tension alternative 230 V ŕ une tension continue stabilisée de quelques volts. - Si UAB= 15 V et UAC= 3 V, quelle est la valeur de la tension UCB ? UCB = UCA + UAB = -UAC + UAB =-3+15 = 12 V.
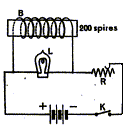
On fait tourner ŕ
grande vitesse un disque de laiton dans l'entrfer d'un électroaimant
non alimenté. On réalise le circuit
ci-contre : B est une bobine ŕ
noyau de fer. On ferme l'interrupteur K et on rčgle le rhéostat de
maničre ŕ ce que la lampe s'allume faiblement. On ouvre l'interrupteur
brusquement. Que se passe-t-il ? (souliger la bonne réponse)
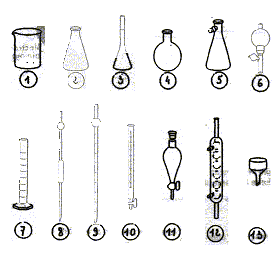
1 : bécher ; 2 : erlenmeyer ; 3 : fiole jaugée ; 4 : ballon ; 5 : fiole ŕ vide ; 6 : poire ŕ aspirer ; 7 : éprouvette graduée ; 8 : pipette jaugée ; 9 : pipette graduée ; 10 : burette graduée
; 11 : ampoule ŕ décanter ; 12 : réfrigérant ŕ boules ; 13 entonoir (
buchner) pour filtration sous vide. On veut prélever un
volume de liquide égal ŕ 8,2 mL. Indiquer le n° de l'appareil
permettant la mesure la plus précise. burette
graduée, pipette graduée.
Compléter le tableau. ( réponses écrites en bleu)
- Indiquer deux méthodes pour mesurer le pH d'un solution. pHmčtre, papier indicateur universel ( peu précis), conductimétrie. - Certains
indicateurs colorés permettent de savoir si une solution est acide ou
basique ; parmi les réactifs de la liste suivante, souligner ceux qui
peuvent ętre utilisés pour cette opération : HCl, NaCl, NH3, NaOH On mesure le pH de
chaque solution en numérotant le becher correspondant. Indiquer dans le
tableau le contenu de chaque becher.
On dispose d'une solution du commerce d'acide chlorhydrique ( 35% ; d = 1,18 ; M=36,46 g/mol ) On veut fabriquer 1,0 L d'une solution aqueuse ŕ 0,1 mol/L de cet acide : - Faire la liste du matériel utilisé : fiole jaugée 1L, pisette d'eau distilée, pipette graduée + pipeteur - Que signifie cette
indication ? - Préciser les indications ŕ prendre. port de blouse, gants et lunettes. - Quel volume ou quelle masse doit-on prélever ? masse de 1 L de solution commerciale : 1,18 kg = 1180 g masse m d'acide pur : 1180*0,35 = 413 g n= m/M = 413/36,46 = 11,33 mol dans 1 L facteur de dilution F= 11,33 / 0,1 = 113,3 volume de solution mčre ŕ prélever pour préparer 1 L de solution ŕ 0,1 mol/L : 1 /113,3= 8,8 10-3 L= 8,8 mL - En présence de bleu de bromotymol, quelle couleur prendra cette solution ? jaune.
|
|||||||||||||||||||||||||||||||||||||||
|
|

 corrosif
corrosif