|
|
- Donner la formule des ions mentionnés sur
l'étiquette.
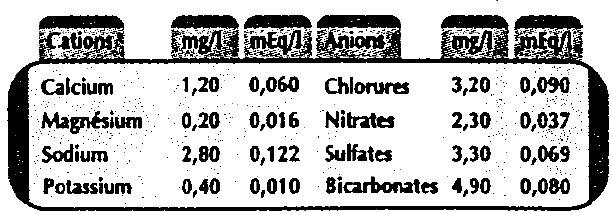
Calcium : Ca2+
; magnésium Mg2+ ; sodium Na+
; potassium : K+ ; chlorure Cl-
; nitrate NO3- ; sulfate
SO42- ;bicarbonate HCO3-
.
- Déterminer la concentration molaire des ions
potassium et calcium. K : 39 ; Ca : 40 g/mol
diviser la
concentration massique ( mg/L) par la masse molaire de l'ion ( g/mol) :
[K+]= 0,40/39 = 1,0 10-2
mmol/L = 1,0 10-5 mol/L
[Ca+]= 1,20/40 = 3,0 10-2
mmol/L = 3,0 10-5 mol/L
- A un prélevement
d'eau minérale proposée, on ajoute quelques gouttes d'indicateur coloré
acido-basique. Préciser la teinte prise par les indicateurs colorés
suivants : ( le pH de l'eau minérale est égal à 6 )
|
nom de l'indicateur
|
zone de virage
|
teinte en présence de l'eau minérale
|
|
hélianthine
|
rouge/3,1-4,4/ jaune
|
jaune
|
|
rouge de méthyle
|
rouge/4,2 - 6,2 / jaune
|
pratiquement jaune
|
|
bleu de bromothymol
|
jaune/6,0- 7,6/bleu
|
jaune
|
|
phénolphtaléine
|
incolore/8,2 - 10/rose
|
incolore
|
- Pour vérifier le
degré hydrodimétrique ( 0,25) de cette eau minérale, on prépare V= 100
mL de solution aqueuse d'EDTA de concentration C donnée.
- Faire une liste du matèriel à utiliser et indiquer les précautions à
prendre.
fiole jaugée
100 mL, balance, spatule, capsule de pesée, entonnoir, hotte, pissette
eau distillée, gants, lunette, bouchon.
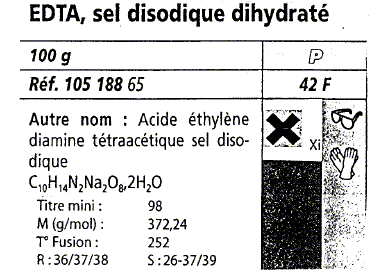
- Calculer la masse d'EDTA à peser pour préparer une solution aqueuse
de concentration c=0,1 mol/L
quantité de
matière (mol) = concentration (mol/L) * volume (L) = 0,1*0,1 = 0,01 mol
masse (g) =
masse molaire (g/mol) * quantité de matière (mol) = 372,24 * 0,01 =
3,72 g.
Donner le nom du
matériel suivant :

|

|
|
machine de Wimshurst
|
transformateur
|
Préciser un exemple d'expérience réalisable avec le matériel ci-dessous
:
 étude d'un pendule pesant étude d'un pendule pesant

mouvement d'un
chariot sur banc à coussin d'air ; acquisition des données avec
ordinateur et interface

étude de l'effet
Joule : calorimétrie
Optique
:
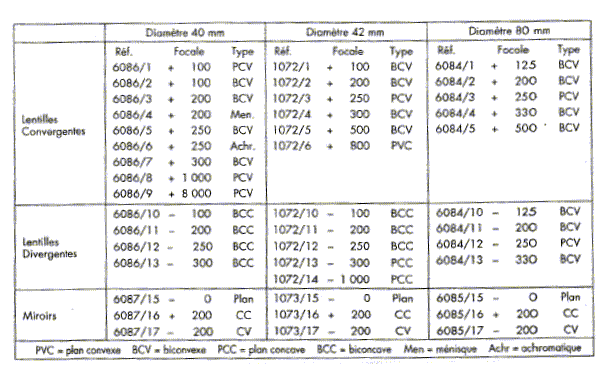
Lire l'extrait du catalogue et compléter le tableau
suivant :
|
référence
|
vergence (dioptries)
|
|
6086 / 3
|
focale 200 mm = 0,2 m ; vergence = 1/0,2 = 5 d
|
|
1072 / 2
|
focale 200 mm = 0,2 m ; vergence = 1/0,2 = 5 d
|
|
6084 / 2
|
focale 200 mm = 0,2 m ; vergence = 1/0,2 = 5 d
|
|
1072 /11
|
focale -200 mm = -0,2 m ; vergence = -1/0,2 =
-5 d
|
électricité :
Déterminer la résistance du fil en utilisant les mesures
effectuées à l'aide du montage ci-dessous :

R= U/I avec U= 0,8 V et I = 0,6 A d'où R= 0,8/0,6 = 1,3 W.
|





 étude d'un pendule pesant
étude d'un pendule pesant

