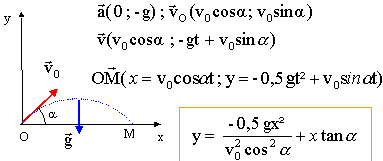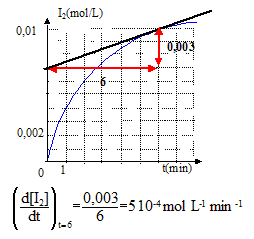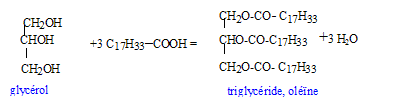|
|
|||||||||||||||||||
|
|||||||||||||||||||
|
Un joueur utilise un club de golf et communique ŗ la balle un vecteur vitesse v0 dans le plan vertical. A la date t=0 la balle, supposťe ponctuelle et de masse m, part du popint O avec le vecteur vitesse v0. On nťglige les frottements de l'air sur la balle ; on donne g= 10 m/s≤ ; H=d=1 m. Le rťfťrentiel liť ŗ la terre est supposť galilťen. Dans un premier temps le joueur tente de lancer la balle le plus loin possible avec une vitesse v0 = 40 m/s. 
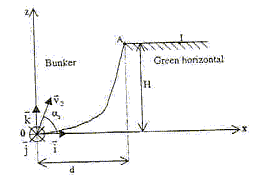
chute libre ( boulet soumis uniquement ŗ son poids) avec vitesse initiale.
ťquation d'une branche de parabole
lorsque le boulet retombe sur le sol horizontal, y=0, l'abscisse est ťgale ŗ la portťe L. 0 = -Ĺ gL≤ /(v0≤cos≤a) + L sin a / cosa. multiplier par cos a et diviser par : 0= -ĹgL/(v0≤cosa) + sin a . ĹgL/(v0≤cosa) = sin a . L= 2 v0≤cosa sin a/ g soit encore L = v0≤ sin (2a)/ g. portťe maximale si sin (2a) = 1 soit a = 45į. Lmax
= v0≤/g
= 40*40/10 = 160 m.
Au sommet de la trajectoire , le vecteur vitesse est horizontal : la composante suivant Oy est nulle. D' oý tS= v0sin a / g. Puis on remplace le temps dans l'expression donnant l'ordonnťe y et x. d'oý : xS=v0 cos a v0sin a / g =v0≤ sin acos a / g = Ĺv0≤ sin (2a)/ g = ĹL yS= -Ĺg(v0sin a / g)≤ + v0sina v0sin a / g = Ĺv0≤sin≤ a / g ; flŤche maxi si a = 90į. flŤche h0 pour a0 =45į ; h0
= 0,5 *40≤ sin≤45 / 10 = 40 m
yA = -Ĺg xA≤/(v0cos a)≤ + xA tan a = -0,5*10*1≤/(10 cos70)≤ + 1* tan 70 = 2,32 m valeur supťrieure ŗ H=1 m , donc la balle peut sortir du bunker. Expression littťrale de la vitesse v1 de la balle en I : ťnergie mťcanique initiale en O : Ĺmv0≤ ; ťnergie mťcanique en I : Ĺmv1≤ +mgH conservation de l'ťnergie mťcanique : Ĺmv0≤ = Ĺmv1≤ +mgH v1≤ = v0≤ -2gH ; v1 = (v0≤ -2gH)Ĺ.
|
|||||||||||||||||||
|
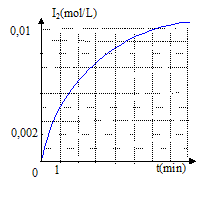
l'ťquation bilan est : H2O2 + 2I- +2H3O+= 4H2O+I2.
corrigť les deux demi-ťquations d'oxydo-rťduction correspondant aux couples envisagťs 2I- =I2 + 2e- oxydation H2O2 +2e- +2H3O+= 4H2O rťduction l'ťquation bilan de la rťaction : H2O2 + 2I- +2H3O+= 4H2O+I2. refroidir le tube avant le dosage du diiode : on rťalise un blocage cinťtique. Quantitťs de matiŤre initiales : n0(H2O2)= V1 [H2O2] = 4*0,2 = 0,8 mmol n0(H3O+)= V3 [H3O+] = 1*1 = 1 mmol ; n0(I-)= V2 [I-] =5*0,1 = 0,5 mmol ŗ partir de 0,8 mmol d'eau oxygťnťe il faut 1,6 mmol d'ion iodure et 1,6 mmol d'ion oxonium : or on ne dispose que de 0,5mmol d'ion iodure ; ce dernier est en dťfaut et constitue le rťactif limitant. concentration en diiode dans un tube ŗ la fin de la rťaction : nf(I2 ) = Ĺn0(I-)= 0,25 mmol volume total du mťlange : 4+5+1 = 10 mL ; [I2]f = 0,25/10= 2,5 10-2 mol/L Cette valeur n'est pas atteinte ( sur le graphe on lit ŗ t= 6 min , [I2]f =10-2 mol/L) ; la rťaction n'est pas encore terminťe. rendement de la rťaction en diiode formť ŗ t = 6 min : concentration rťelle / concentration thŤorique *100 = 0,01 / 0,025 *100 = 40% vitesse de formation du diiode : 1/V dx/dt = d[I2]/dt avec V : volume du mťlange rťactionnel et x avancement (mol) valeur de la vitesse de formaton du diiode ŗ la date t= 6 min
|
|||||||||||||||||||
|
Masse molaire M(HCOOH) = 46,0 g/mol ; pKa( HCOOH / HCOO-) = 3,8 ŗ 25įC. Une solution commerciale S d'acide mťthanoÔque porte les indications suivantes : masse volumique m ; pourcentage massique en acide : p%.
corrigť concentration molaire volumique C de la solution S : masse volumique m en g/mL masse de 1 L de solution S : 1000 m g ; masse d'acide pur dans 1 L : 1000 m p/100 = 10m p g Qtť de matiŤre d'acide dans 1 L : masse (g) / Masse molaire (g/mol) = 10m p / M(HCOOH) mol dans 1 L verrerie utilisťe pour prťlever le volume V de solution S et pour prťparer la solution S1 : pipette (+ pipeteur) de 50 mL relation liant les concentrations C et C1 : facteur de dilution F =V1/V = 500 / 50 = 10 de plus F= C/C1 = 10 d'oý C= 10 C1. verrerie utilisťe pour dťterminer le volume Vťq : burette graduťe couples mis en jeu lors du mťlange des solutions S et S0 par ordre de pKa dťcroissant : espŤce majoritaires ťcrites en rouge avanr toute rťaction
HCOOH + HO- --> HCOO- + H2O constante K1 de cette rťaction : K1 = [HCOO-] / ([HCOOH][HO-]) or Ka = [HCOO-][H3O+]/[HCOOH] soit [HCOO-] / [HCOOH] = Ka /[H3O+] d'oý : K1 = Ka /([H3O+][HO-])=Ka /Ke = 10-3,8 / 10-14 = 1010,2, valeur grande donc rťaction totale. valeur de C1 : ŗ l'ťquivalence V2C1=Vťq C0 soit C1=Vťq C0 / V2=24,4*0,1/10 = 0,244 mol/L Or C = 10 C1 = 2,44 mol/L. espŤces majoritaires prťsentes dans le mťlange rťactionnel obtenu ŗ l'ťquivalence :
HCOO- + H2O = HCOOH + HO- constante K2 = [HCOOH][ HO-]/[HCOO-] =1/K1 = 10-10,2 , valeur trŤs faible, rťaction trŤs limitťe. Le mťlange rťactionnel ŗ l'ťquivalence contient la base [HCOO- : le pH est supťrieur ŗ 7 , milieu basique. La zone de virage de l'indicateur colorť doit contenir le pH du point ťquivalent, d'oý le choix de la phťnolphtalťine.
|
|||||||||||||||||||
|
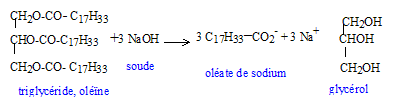
corrigť diastťrťoisomŤres : 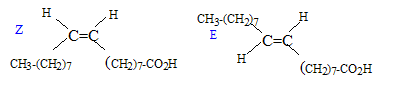
glycťrol : HO-CH2-CHOH-CH2OH ( 2 fonctions alcool primaire et une fonction alcool secondaire). La molťcule n'est pas chirale : absence de carbone asymťtrique.( carbone tťtragonal portant 4 substituants diffťrents) estťrification, lente, athermique, limitťe par l'hydrolyse du triester
On utilise un excŤs d'acide olťique afin de dťplacer l'ťquilibre vers la formation de l'ester ( obtention d'un meilleur rendement) On chauffe pour accťlťrer la rťaction et atteindre plus rapidement l'ťquilibre.
saponification, lente mais totale :
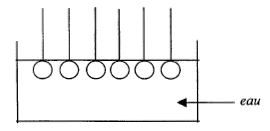
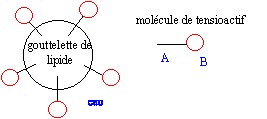
rťactif nuclťophile HO- : savon obtenu : olťate de sodium masse de savon thťoriquement obtenu en faisant rťagir une masse d'olťine notťe molťine avec un excŤs de soude : n( olťine) =molťine / Molťine d'aprŤs les coefficients de l'ťquation : n( savon) =3 n( olťine) = 3molťine / Molťine or n( savon) =msavon / Msavon d'oý msavon = 3 molťineMsavon / Molťine partie hydrophile : groupe COO- symbolysť par "O" et partie hydrophobe de cet ion : la chaÓne carbonťe symbolysťe par "---------". ions carboxylates ŗ la surface de l'eau : ions carboxylate sur une tache de graisse (lipide) :
|
|||||||||||||||||||
|
|