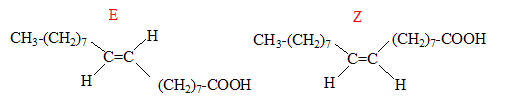|
|
||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||
corrigť Les coupes mis en jeu sont : I2 / I- : 2I- = I2 + 2e- oxydation H2O2/ H2O
: H2O2 + 2e- +
2H+= 2H2O rťduction Il faut acidifier le milieu rťactionnel car l'ion H+ est l'un des rťactif. Il ne faut pas que l'anion apportť par l'acide ait des
propriťtťs oxydantes qui concurencerait H2O2.
n0(I-) =
10*0,2 = 2 mmol ; n0(H2O2)
= 2*0,2 = 0,4 mmol ; d'aprŤs les coefficients stoechiomťtrique de (1), 2 mol d'ion iodure rťagissent avec une mol d'eau oxygťnťe donc 0,4 mmol d'eau oxygťnťe rťagit avec 0,8 mmol d'ion iodure. Or nous disposons de 2 mmol d'ion iodure : ce dernier
est en excŤs de : 2-0,8 = 1,2 mmol. ŗ partir de 0,4 mmol d'eau oxygťnťe il se forme 0,4 mmol de diiode ; volume du mťlange : 30 mL = 0,03 L [I2]max =
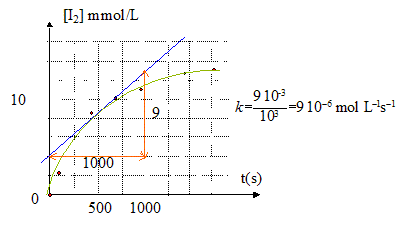
0,4/0,03 = 0,0133 mol/L
= 13,3 mmol/L
coefficient directeur de la tangente ŗ la courbe ci-dessus ŗ la date considťrťe. avec x : avancement (mol) et V : volume de la solution (L)
|
||||||||||||||||||||||||||||||||||||||
|
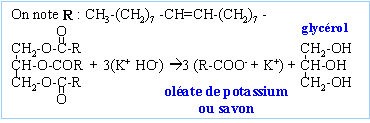
Donnťes : olťine Mol= 884 ; savon : Ms= 304 g/mol ; masse volumique de l'olťine r= 0,88 kg/L. L'olťine est un corps gras de formule brute C57H104O6 prťsente dans l'huile d'olive. On souhaite fabriquer un savon ŗ partir de celle-ci. Pour cela, on utilise le montage suivant : dans un ballon on introduit 20 mL de soude concentrťe ŗ 10 mol/L, 50 mL d'eau, 50 mL d'ťthanol et 20 mL d'huile d'olive. On ajoute un barreau magnťtique, puis on place le ballon sur un agitateur chauffant aprŤs l'avoir muni d'un rťfrigťrant vertical. On laisse la rťaction de saponification se faire pendant 30 min. AprŤs refroidissement, le mťlange est versť dans une solution de chlorure de sodium, puis le savon est recueilli par ťcrťmage.
corrigť L'acide olťique est l'acide gras de formule CH3-(CH2)7-CH=CH-(CH2)7-COOH. Il prťsent l'isomťrie de type Z E ( diastťrťoisomťrie)
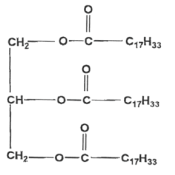
la formule semi-dťveloppťe de l'olťine :
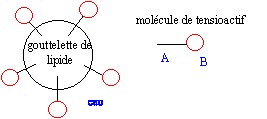
Schťma de l'action d'un savon peut agir sur une tache de graisse : partie hydrophile : groupe COO- symbolysťe par "O" et partie hydrophobe de cet ion : la chaÓne carbonťe symbolysťe par "---------".
ions carboxylate sur une tache de graisse (lipide) :
quantitť de matiŤre initiale (mol) : n0(soude) = 0,02*10 = 0,2 mol masse d'huile (g) = volume ( mL) * masse volumique ( g/mL) = 20*0,88 = 17,6 g n0( olťine )= 17,6 / 884 = 0,02 mol D'aprŤs les coefficients de l'ťquation bilan, ŗ partir de 0,02 mol d'olťine il faut 0,02*3 = 0,06 mol de soude. Or nous avons 0,2 mol de soude : celle-ci est en excŤs
de 0,2-0,06 = 0,14 mol. ( olťine en dťfaut) D'aprŤs les coefficients de l'ťquation bilan, ŗ partir de 0,02 mol d'olťine on obtient 0,02*3 = 0,06 mol de savon masse (g) = quantitť de matiŤre (mol) * masse molaire
(g/mol) = 0,06*304 = 18,2 g. le rendement de la rťaction : masse rťelle / masse thťorique * 100 = 12,3/18,2*100 = 67,6 % ( 68 %).
|
||||||||||||||||||||||||||||||||||||||
|
|