|
|
||||||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
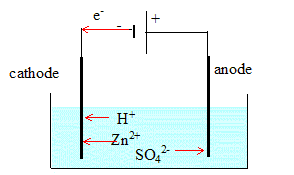
Plus de 50 % de la production mondiale de zinc est obtenu par ťlectrolyse d'une solution de sulfate de zinc, acidifiťe ŗ l'acide sulfurique. Les ions sulfates ne participent pas aux rťactions ťlectrochimiques.. On observe un dťpŰt mťtallique sur une ťlectrode et un dťgagement gazeux sur l'autre. I- Etude de la transformation :
II- Exploitation : l'ťlectrolyse a lieu sous 3,5 V. L'intensitť du courant peut atteindre 80 kA. AprŤs 48 H de fonctionnement, le dťpŰt de zinc est suffisamment ťpais. Il est alors sťparť et fondu en lingots.
les rťactions susceptibles de se produire sur chaque ťlectrodes : ŗ la cathode nťgative, rťduction : Zn2+ (aq) + 2e- = Zn(s) majoritaire mais aussi 2H+ (aq) + 2e- = H2(g) ŗ l'anode positive, oxydation : H2O (l)= ĹO2 (g)+ 2H+ (aq) + 2e-. d'oý l'ťquation globale de cette ťlectrolyse : Zn2+(aq) + H2O(l) = Zn + ĹO2(g) + 2 H+(aq) L'ťlectrolyse est une transformation forcťe qui nťcessite un apport d'ťnergie ťlectrique. vťrification thťorique : comparer le quotient initial et la constante d'ťquilibre .
Zn2+ (aq) + 2e- = Zn(s) d'oý : la quantitť de matiŤre d'ťlectrons n( e-) est ťgale ŗ 2 fois la quantitť de matiŤre de zinc. n( e-) = 2x Quantitť de matiŤre d'ťlectricitť Q= 96000 n(e-) =96000*2 x = 1,92 105 x ordre de grandeur de la masse de zinc produite en 2 jours par une cellule : de plus Q= I t = 8 104 * 2*24*3600 = 1,38 1010 C d'oý x = 1,38 1010 / 1,92 105 = 7,2 104 mol masse de zinc (g)= masse molaire (g/mol) * Qtť de matiŤre (mol) = 65* 7,2 104 =4,68 106 g = 4,68 t. on obtient une quantitť de zinc infťrieure ŗ celle attendue : les ion H+ se rťduisent ťgalement ŗ la cathode. relation entre l'avancement x et le volume V de dioxygŤne rťcupťrť : quantitť de matiŤre de O2 (mol) = volume (L) / volume molaire (L/mol) = V/24 = Ĺ x soit V= 12 x ordre de grandeur de V : 12*7,2 104 = 8,6 105 L = 8,6 102 m3. en tenant compte du rendement : 8,6 102*0,8 = 688 m3.
|
||||||||||||||||||||||||||
|
|