|
d'aprŤs
concours manipulateur
ťlectroradiologie mťdicale AP Paris, Nantes, Rennes
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
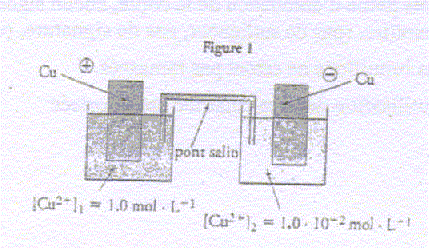
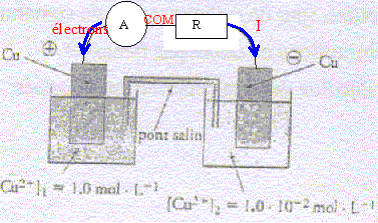
I- Rťalisation de la pile : On rťalise une pile ŗ partir des couples Pb2+(aq) / Pb(s) et Sn2+(aq)/Sn(s). Les ions Pb2+(aq) proviennent d'une solution de nitrate de plomb( Pb2+(aq)+2NO3-(aq)), les ions Sn2+(aq) proviennent d'une solution de nitrate d'ťtain ( Sn2+(aq) +2NO3-(aq)). La demi-pile de gauche contient le mťtal ťtain plongeant dans une solution de volume V2 = 30,0 mL, C2= 2,0 10-2 mol/L. La demi-pile de droite contient le mťtal plomb plongeant dans une solution de volume V1= 20 mL, C1 = 3,0 10-2 mol/L. Le pont salin est rťalisť avec du nitrate de potassium. M(Pb)= 207,2 ; M(Sn)=118,7 g/mol ; e = 1,6 10-19 C ; NA= 6,02 1023 mol-1 ; Pb2+(aq) + Sn(s) = Sn2+(aq)+ Pb(s). K1= 2,18 Sn2+(aq)+ Pb(s) = Pb2+(aq) + Sn(s) ; K2 = 0,46. L'ťlectrode positive de cette pile est l'ťlectrode de plomb.
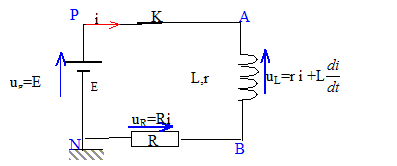
II. Circuit RL : on remplace la pile maison par un gťnťrateur de tension stabilisťe de fem E=1,5 V. Le montage ťlectrique consiste en une association sťrie d'une bobine rťelle (L ; r= 8,6 W), d'un conducteur ohmique (R=10 W ), d'un interrupteur et du gťnťrateur.
corrigť 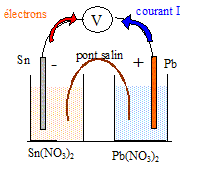
Sn (s ) = Sn2+(aq)+ 2e- : oxydation du rťducteur l'ťtain. Pb2+(aq) +2e-=Pb (s ) rťduction de l'oxydant Pb2+(aq) Sn (s ) + Pb2+(aq) = Sn2+(aq) + Pb (s ) Dans la solution et dans le pont salin, les cations positifs se dťplacent dans le sens conventionnel du courant, tandis que les anions nťgatifs se dťplacent en sens contraire. utilitť du pont salin : assure la continuitť ťlectrique et assure l'ťlectroneutralitť des solutions. variation de masse de l'ťlectrode de plomb : augmentation de masse Q=It= 0,015*2*3600 = 108 C soit n(e-) = 108/96500 = 1,12 10-3 mol d'ťlectrons. or Pb2+(aq) +2e-=Pb (s ) d'oý n(Pb)= Ĺn(e-) =5,6 10-4 mol masse de plomb correspondante (g) = n(Pb) M( Pb) = 5,6 10-4
*207,2 = 1,16 10-1 g ( 0,12 g)
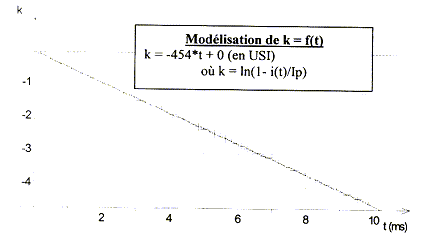
valeur de la constante de temps : d'une part i=IP(1-exp(-t/t)) soit i/IP = 1-exp(-t/t) d'autre part k = ln(1-i/IP) = ln(exp(-t/t)) = -t/t = -454 t d'oý t = 1/454 = 2,20 10-3 s. valeur de l'inductance de la bobine :t = L/(R+r) soit L= t (R+r) = 2,20 10-3 *18,6 = 4,1 10-2 H. la constante de temps est homogŤne ŗ un temps exprimť en seconde : t = L/(R+r) ĹLI≤ a la dimension d'une ťnergie en J ; L a la dimension d'unť ťnergie divisťe par une intensitť au carrť : J A-2. (R+r) I≤ t a la dimension d'une ťnergie soit (R+r) a la dimension d'unť ťnergie divisťe par une intensitť au carrť, divisťe par un temps : J A-2 s-1. donc L/(R+r) a la dimension d'un temps. ťquation diffťrentielle traduisant l'ťvolution temporelle du courant i(t) : ug = uL+uR ; E= ri+Ldi/dt+Ri Ldi/dt + (R+r)i = E soit di/dt = E/L-(R+r)/L i = E/L-454 i= 36,59-454 i complťter le tableau : i(10-3) =i(5 10-4) + Di(tn) = i(5 10-4) + (di/dt)5 10-4Dt = 0,018+28,29*5 10-4 = 0,0321 A (di/dt) 10-3=36,59-454 *0,0321=21,99. i(1,5 10-3) =i(1 10-3) + Di(tn) = i(1 10-3) + (di/dt) 10-3Dt = 0,0321+21,99*5 10-4 = 0,0431 A (di/dt) 1,5 10-3=36,59-454 *0,0431=17,02. i(2 10-3) =i(1,5 10-3) + Di(tn) = i(1,5 10-3) + (di/dt) 1,5 10-3Dt = 0,0431+17,02*5 10-4 = 0,0516 A (di/dt) 1,5 10-3=36,59-454 *0,0516=13,16.
avec un pas plus petit on augmente la prťcision, mais on multiplie le nombre de calculs.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Electrolyse : On envisage de chromer ( Cr) entiŤrement un pare-chocs mťtallique en y dťposant une couche de chrome, d'une ťpaiseur e=50 mm. Le parre-chocs est considťrť comme un bloc parallŤlťpipťdique de longueur L= 2,0 m, de largeur l=0,10 m, de hauteur h= 5,0 mm. On plonge le parre-chocs dans une solution contenant des ions chrome III Cr3+, puis on ťlectrolyse cette solution, entre l'ťlectrode constituťe par le parre-chocs et une seconde ťlectrode de nature adťquate. L'opťration dure 10 heures et son rendement est 95%.
corrigť ťquation de la rťaction d'ťlectrode qui permet la formation du chrome mťtallique ŗ partir des ions chrome III : Cr3+(aq) + 3e- = Cr(s) , rťduction ŗ la cathode nťgative volume de la couche de chrome ŗ dťposer : surface du bloc : 2(L+l)h+2Ll = 2*210*0,5+2*200*10 =210+4000=4210 cm≤ v= e *surface du bloc =50 10-4 * 4210= 21 cm3. masse de chrome : r v = 7,2*21 = 151,6 g Qtť de matiŤre (mol) : n(Cr) = m/M= 151,6/52 = 2,92 mol donc d'aprŤs les coefficients de l'ťquation ci-dessus : n(e-) = 3 n(Cr) = 8,75 mol quantitť d'ťlectricitť Q qui a traversť l'ťlectrolyseur : Q= 96500 n(e-) = 96500*8,75 = 8,44 105 C de plus Q= It soit I = Q/t = 8,44 105 /(10*3600) = 23,4 A en tenant compte du rendement ťlectrolytique : 23,4/0,95 = 24,7 A.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|