|
concours aide
laboratoire Groupe II d'après concours 2005
|
||||||||||||||||||
|
||||||||||||||||||
|
On désire préparer 500 mL d'une solution aqueuse (S) de permanganate de potassium de concentration 2,00 10-2 mol/L. L'étiquette du flacon est reproduite ci-dessous. 
- Donner la signification des pictogrammes : substance comburante, irritant ou nocif, danger pour l'environnement. Quelle masse peser sur la balance au centigramme ? Quantité de matière (mol) = concentration (mol/L) * volume de la solution (L) = 0,02*0,5 = 0,01 mol masse (g) = quantité de matière (mol) * masse molaire (g/mol) = 0,01*158 =1,58 g. Dresser la liste du matériel pour préparer la solution. fiole jaugée 500 mL, balance, spatule, capsule de pesée, entonnoir, hotte, pissette eau distillée, gants, bouchon. On vous demande de préparer à partir de la solution S, 200 mL d'une solution de permanganate de potassium 20 fois moins concentrée. Dresser la liste du matériel pour préparer la solution. facteur de dilution F=20 ; volume pipette jaugée = volume fiole jaugée / 20 = 200 / 20 = 10 mL fiole jaugée 200 mL ; pipette jaugée 10 mL+ pipeteur ; bouchon ; pissette eau distillée.
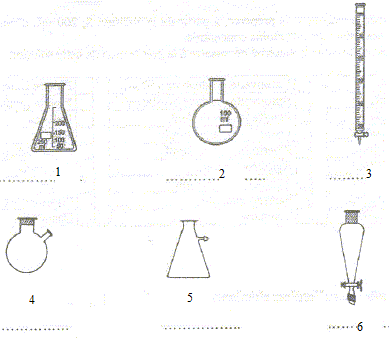
1 : erlenmeyer ; 2 : ballon à fon rond ; 3 : burette graduée ; 4 : bicol ; 5 :fiole pour filtration sous vide ( trompe à eau) ; 6 : ampoule à décanter. stockage des produits : règles de sécurité : Produits toxiques étiquetés T+ : armoires fermées à clef produits explosifs étiquetés E : locaux et armoires spécifique produits étiquetés O ( comburants ) : stockés à part des produits facilement inflammables étiquetés F ou F+ ( enceintes sécurité ventilées) produits donnant des réactions dangereuses avec l'eau : armoires spécifiques sans contact avec l'eau acide concentré étiqueté C ( corrosif) : stoockage séparé des base concentrées étiqueté C
|
||||||||||||||||||
|
On désire préparer V1 =500 mL d'une solution aqueuse (S1) d'hydroxyde de sodium de concentration c1 =1 mol/L. Cette solution sera utilisée pour obtenir V2= 200 mL d'une solution aqueuse (S2) d'hydroxyde de sodium de concentration c2 =0,1 mol/L. La masse molaire de l'hydroxyde de sodium est 40 g/mol. Quantité de matière (mol) = concentration (mol/L) * volume de la solution (L) = 1*0,5 = 0,5 mol masse (g) = quantité de matière (mol) * masse molaire (g/mol) = 0,5*40 =20 g. Dresser la liste du matériel pour préparer la solution S2. facteur de dilution F=C1/C2 =10 ; volume pipette jaugée = volume fiole jaugée / 10 = 200 / 10 = 20 mL fiole jaugée 200 mL ; pipette jaugée 20 mL+ pipeteur ; bouchon ; pissette eau distillée.
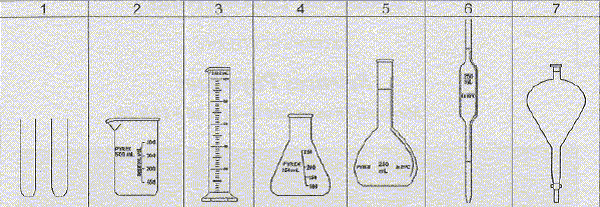
1 : tube à essais ; 2 : bécher gradué ; 3 : éprouvette graduée ; 4 : erlenmeyer ; 5 :fiole jaugée ; 6 : pipette jaugée 7 : ampoule à décanter. sécurité
: que représentent ces pictogrammes ?
|
||||||||||||||||||
|
|
 danger
pour l'environnement
danger
pour l'environnement  toxique.
toxique.