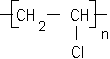|
|
||||||||||||||||
|
||||||||||||||||
|
Un bassin de grande surface est rempli d'eau. Il peut se vidanger par une canalisation horizontale de section S située ŕ sa base. Un tube témoin servant de détecteur de fuites, permet de déterminer la pression statique dans la canalisation sans perturber l'écoulement. 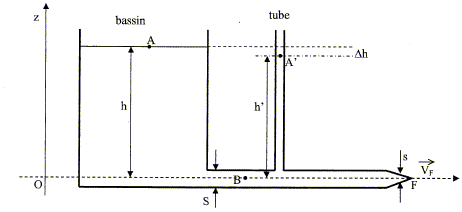 La canalisation fermée ŕ son extrémité présente une fuite en F, on la schématise par un trou de section s. L'eau étant considérée comme un fluide parfait on peut lui appliquer le théorčme de Bernoulli ; 1/(2g)( v˛2-v˛1) +(z2-z1)+(P2-P1)/(rg)=0. La fuite d'eau étant faible, on admet que la hauteur d'eau dans le bassin ne varie pas.
corrigé Expression littérale de la vitesse d'écoulement vF de l'eau ŕ travers le trou de fuite en fonction de h et g : Ecrire le théorčme de Bernoulli entre les points F (2) et A (1) : d'une part, la surface du récipient étant trčs grande par rapport ŕ la section du trou, la vitesse de l'eau en A est presque nulle d'autre part, on considčre le point F dans le jet d'eau, en contact avec l'air extérieur d'oů : PF-PA=0 par suite : 1/(2g)( v˛F-0) +(zF-zA)=0 ; 1/(2g) v˛F- h=0 soit v˛F = 2gh ; vF= (2gh)˝. si h = 10 m alors vF= 200˝ = 14 m/s. Débit volumique qv de fuite si s = 1 mm˛ : qv = s vF avec s= 10-6 m˛ ; qv =10-6 *14 = 1,4 10-5 m3/s. Expression de la valeur de la vitesse V de l'eau dans la canalisation en fonction de vF, S et s : le débit volumique se conserve d'oů : s vF = SV ; V= s /S vF =10-6 / 10-4 *14 = 0,14 m/s. Expression de la différence de pression entre les points B et A' en fonction de la hauteur d'eau h' dans le tube : Ecrire le théorčme de Bernoulli entre les points B et A : 1/(2g)( V˛-v˛A) +(zB-zA)+(PB-PA)/(rg)=0 PB-PA =rg[h- V˛/(2g) ] L'eau étant en équilibre dans le tube témoin : PB-PA' =rgh' de plus : PA' =PA =pression atmosphérique d'oů : rgh' = rgh -˝rV˛ ; h-h'= V˛/(2g) Dh =
h-h'=V˛/(2g) = 0,14˛/20 = 10-3 m = 1 mm. Valeur minimale de la section du trou de fuite s, que l'on peut détecter pour S= 1 cm˛ et h = 10 m : Dh = 5 10-3 m ; V˛/(2g) = 5 10-3 soit V˛ = 0,1 ; V= 0,316 m/s or V= s /S vF soit s = V S/vF = 0,316*10-4 / 14 =2,26 10-6 m˛ = 2,3 mm˛.
|
||||||||||||||||
|
On désire comparer le prix de revient de deux installations, l'une utilisant des lampes ŕ incandescence, l'autre des lampes fluorescentes compactes. On veut obtenir la męme efficacité lumineuse soit six lampes ŕ incandescence pour une lampe fluorescente compacte et une męme durée de vie.
corrigé Coűt total de 8000 h d'éclairage avec les lampes ŕ incandescence puis avec les lampes fluorescentes : Le prix du kWh est 0,076 euro ; énergie kWh) = puissance (kW)*durée (h) une lampe fluorescente compacte : 0,01*8000 = 80 kWh soit 80*0,076 =6,1 euros six lampes incandescentes sonr utiles pour une męme efficacité lumineuse de 60 lm W-1. énergie : 6*0,06*8000 = 2880 kWh soit 2880*0,076 = 219euros soit 36 fois plus cher q'avec des lampes fluorescentes. Avantage et un inconvénient pour chaque type de lampe : lampe fluorescente compacte : économie d'énergie mais coűt plus élevé ŕ l'achat. lampe incandescente : peu économe en énergie mais faible
coűt ŕ l'achat.
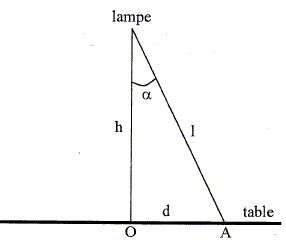
F = 60*10 = 600 lm ; I= F/(4p) = 600/12,56 = 47,8 Cd ; cos a = cos 0 = 1 ; h = l = 1,3 m E0= I /h˛ = 47,8 / 1,3˛= 28,3 lm m-2 = 28,3 lx. Eclairement EA en un point A de la table situé ŕ d= 1 m du centre : F = 60*10 = 600 lm ; I= F/(4p) = 600/12,56 = 47,8 Cd ; tan a = d/h = 1/1,3 =0,769 ; a =37,6° ; cos 37,6 = 0,793 l =h/cos a = 1,3 / cos37,6 = 1,64 m EA= I cos a/l˛ = 47,8*0,793/1,642= 14,1 lx.
|
||||||||||||||||
Données :masse atomique molaire (g/mol) : H : 1,0 ; C : 12 ; Cl : 35,5. corrigé réaction 1 : réaction d'addition du dichlore sur une double liaison carbone-carbone : H2C=CH2+ Cl2 ---> ClH2C--CH2Cl : 1,2-dichloroéthane n(éthylčne) = n(dichlore) = n( 1,2-dichloroéthane) réaction 2 : ClH2C--CH2Cl --->ClHC=CH2 + HCl n( 1,2-dichloroéthane) = n(chlorure de vinyle) = n (HCl) réaction 3 : polymérisation radicalaire en chaîne : n : indice de polymérisation ou nombre moyen de motif élémentaire dans le polymčre. La masse molaire de ce PVC est de 94 kg/mol. Degré de polymérisation : masse molaire du polymčre / masse molaire du monomčre =
94 000 / (12*2+3+35,5) = 1504. quantité de matičre de PVC (mol) = masse (g) / masse molaire CH2=CHCl = 1,5 106 / (12*2+3+35,5) = 2,4 104 mol donc 2,4 104 mol déthylčne masse d'éthylčne (g) = quantité de matičre (mol) * masse molaire éthylčne (g/mol) = 2,4 104*28 = 6,72 105 g = 0,67 tonne. Le chlorure d'hydrogčne produit par la réaction 2 est trčs soluble dans l'eau. Equation de la dissolution de ce gaz dans l'eau : HCl + H2O = H3O+ + Cl- solution d'acide chlorhydrique. Par dilution de la solution S1 on
prépare une solution S2. Ensuite on effectue un
dosage de 20,0 mL de S2 par une solution de
soude de concentration cB=0,025 mol/L.
L'équivalence est obtenue pour un volume vBe=
15,2 mL de solution de soude versée. H3O+ + HO-
= 2H2O ŕ l'équivalence : cAVA
= cBVB soit cA=cBVB
/VA =0,025*15,2/20 = 0,019
mol/L. pH= -log cA= -log 0,019 = 1,7.
|
||||||||||||||||
|
|
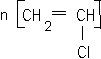 ---->
---->