|
|
||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||
|
Le moteur de Stirling fait aujourd'hui l'objet de nombreux programmes de recherche dťveloppement aux …tats-Unis, au Japon et en Europe du Nord, oý il y a dťjŗ quelques opťrations de dťmonstration en vraie grandeur, notamment en Allemagne et aux Pays-Bas. Le moteur de Stirling prťsente des avantages significatifs par rapport ŗ un moteur ŗ explosion, Diesel ou essence : ∑ peu de maintenance et une longue durťe de vie ; ∑ moteur peu bruyant ; ∑ la combustion extťrieure et continue, ŗ basse pression, peut Ítre parfaitement contrŰlťe pour ťmettre peu de gaz polluants (3 ŗ 4 ppm d’oxydes d’azote) ; ∑ enfin, dans les installations de cogťnťration, la quasi-totalitť de la chaleur non dťpensťe peut Ítre rťcupťrťe et exploitťe, ce qui conduit ŗ un rendement global potentiel trŤs ťlevť, de l'ordre de 95 %. Les tempťratures notťes T sont des tempťratures absolues, en K. Gťnťralitťs sur les moteurs Un moteur est un systŤme fermť ťchangeant un travail W avec l’extťrieur, une chaleur QF avec une source froide (tempťrature TF) et une chaleur QC avec une source chaude (tempťrature TC).
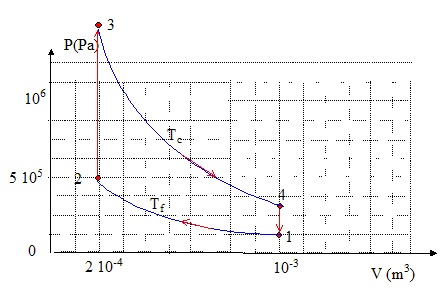
travail cťdť ŗ l'extťrieur, nťgatif par dťfinition Qc recu par le systŤme, positif par dťfinition Qf cťdťe par le systŤme, nťgatif par dťfinition rendement : travail mis en jeu / Chaleur cťdťe par la source chaude rendement Carnot : (Tc-Tf)/Tc. Il n'existe pas, ŗ priori, un moteur de plus grande performance, ŗ TF et TC donnťes : dans le cycle de Carnot, toutes les transformations sont rťversibles et le rendement est maximum. allure du cycle de transformations relatif ŗ ce moteur en coordonnťes de Clapeyron (P, V),
nombre de moles de gaz parfait mis en jeu : avec les donnťes de l'ťtat 1 par exemple n= PV/RT = 105*10-3
/ (8,31*270)= 4,46 10-2
mol. Lors de la transformation 1-->2, le travail W12 reÁu par la quantitť n de gaz parfait s'ťcrit : P= nRT/ V d'oý : dW= -nRT/ VdV = -nRTf d ln V ŗ Tf = constante. puis intťgrer entre V1 et V2 d'oý W12=nRTfln(V1/V2) de plus ŗ tempťrature constante V1/V2= P2/P1 d'oý : W12=nRTfln(V1/V2) = nRTfln(P2/P1) Travaux W12, W23, W34, W43 ťchangťs au cours des diffťrentes transformations du gaz, ainsi que le travail total ťchangť au cours du cycle : W12 = 4,46 10-2 *8,31*270 ln (10-3 / 2 10-4) = 161 J. W23=0 ( isochore) ; W41 = 0 ( isochore) W34= nRTc ln( V3/V4) = 4,46 10-2 *8,31*770 ln (2 10-4/10-3 ) = -460 J. W= -460+161 = -299 J. variations d'ťnergie interne : DU12 = DU34 = 0 ( isothermes) quantitťs de chaleur Q12 et Q34 : en consťquence W34+Q34=0
soit Q34 = - W34 = 460 J
; W12+Q12=0
soit Q12 = - W12 = -161 J rendement =| (W12+W34)/ Q34 |= | (W12+W34)/ (-W34 ) |=| -W12/W34-1| W12 / W34= -Tf / Tc d'oý le rendement : |Tf / Tc -1| = |270 / 770-1 |= 0,65. rendement intŤressant car identique au rendement d'une machine de Carnot fonctionnant entre deux source de chaleur aux mÍme tempťratures que ce moteur. Le cycle est rťpťtť 500 fois par minute, la puissance mťcanique fournie par le moteur ŗ l'alternateur vaut : travail total sur un cycle : 299 J sur 500 cycles : 299*500 = 1,5 105 J puissance 1,5 105 /60 = 2,5 kW. puissance thermique fournie au systŤme de chauffage de la maison : 161*500/60 = 1,3 kW.
|
||||||||||||||||||||||||||||||||||||
|
Un moteur est situť dans un local de surface au sol 2*2,5 m≤ et de hauteur 2,5 m. Toutes les parois de ce local sont en bťton ( coefficient d'absorption a1 = 0,02) On mesure , quand ce moteur fonctionne, le niveau d'intensitť acoustique Lp ŗ l'aide d'un sonomŤtre ťquipť d'un analyseur de filtres d'octaves de frťquences centrales f0.
Formule de Sabine pour la durťe dr rťverbťration d'un local : T= a(V/A) avec a = 0,16 s m-1 ; V : volume du local ; A : aire absorbante ťquivalente. Variation DL du niveau acoustique rťsultant d'une variation de la durťe de rťverbťration DL= 10 log (T2/T1) corrigť niveau de pression acoustique total notť L1 : pour chaque intervalle, calcul du niveau d'intensitť acoustique I= I0 100,1 L = 10-12 * 100,1 L :
L1 = 10 log (Itotal
/ I0 ) = 10 log (2,68 10-6
/ 10-12) = 64,3
dB.
Formule de Sabine pour la durťe dr rťverbťration d'un local : T= a(V/A) avec a = 0,16 s m-1 ; V : volume du local ; A : aire absorbante ťquivalente. A= aire totale du local *coefficient d'absorption a1 du bťton aire du local = aire sol + aire plafond + aire des murs = 5 +5 + 9*2,5 =32,5 m≤ A= 32,5a1 = 32,5*0,02 =0,65 m≤ volume du local : V= 5*2,5 = 12,5 m3. T1 = 0,16 *12,5/0,65 =3,1 s.
durťe de rťverbťration notťe T2 : A= aire absorbante ťquivalente = aire du plafond a2 + aire des murs a1 A = 5*0,8 + 27,5*0,02 =4,55 m≤. T2 = 0,16 *12,5/4,55 =0,44 s. nouvelle valeur du niveau de pression acoustique total notť L2: Variation DL du niveau acoustique rťsultant d'une variation de la durťe de rťverbťration DL= 10 log (T2/T1) DL= 10 log (0,44/3,1) = -8,5 dB ; L2 = 64,3-8,5 = 55,8 dB.
|
||||||||||||||||||||||||||||||||||||
|
On souhaite dissoudre le calcaire ou carbonate de calcium CaCO3 existant dans une canalisation. Pour cela on utilise l'acide chlorhydrique du commerce. L'ťquation de la rťaction est : Ca2+ + CO32- + 2(H+ + Cl-) = CO2 + H2O+ Ca2+ +2Cl-
Ca : 40 ; C : 12 ; O : 16 g/mol H3O+/H2 : V ; Fe2+/Fe : -0,44 V ; Cu2+/Cu : 0,34 V ; Pb2+/Pb : -0,13 V. corrigť masse de carbonate de calcium dissoute avec 1L de solution d'acide chlorhydrique de concentration C= 11 mol/L : quantitť de matiŤre d'acide (mol) = volume (L) * concentration (mol/L) =1*11 = 11 mol Ca2+ + CO32- + 2(H+ + Cl-) = CO2 + H2O+ Ca2+ +2Cl- D'aprŤs les coefficients de l'ťquation, la quantitť de matiŤre de carbonate de calcium est ťgale ŗ la moitiť de la quantitť de matiŤre d'acide soit 5,5 mol. Masse molaire CaCO3 : M= 40 +12+3*16 = 100 g/mol masse (g) = masse molaire (g/mol) * quantitť de matiŤre
(mol) = 100 *5,5 = 550 g.
Le facteur de dilution est ťgal ŗ : F= 500/5 = 100 ; la solution diluťe est 100 fois moins concentrťe que la solution commerciale. pH = 1= - logc d'oý c = 0,1 mol/L et C= 100*0,1 = 10 mol/L.
L'indicateur colorť change de couleur ŗ l'ťquivalence ( passage du jaune au bleu). L'indicateur colorť permet de repŤrer l'ťquivalence. La solution titrante est une solution d'hydroxyde de sodium de concentration cb=0,10 mol/L. Le volume de solution titrante nťcessaire pour atteindre l'ťquivalence est 10,8 mL : ŗ l'ťquivalence caVa = cbVb soit ca= cbVb / Va =0,1*10,8/10 = 0,108 mol/L et C= 100*0,108 = 10,8 mol/L L'indication portťe par l'ťtiquette est correcte ( ťcart
relatif =(11-10,8)/10,8 *100 = 2 % )
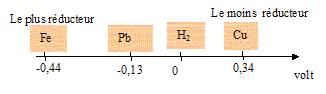
Il est possible d'utiliser l'acide chlorhydrique pour dťtartrer une canalisation de cuivre (H3O+ n'attaque pas le cuivre) ; par contre le plomb et le fer ( fonte) sont des mťtaux plus rťducteurs que H3O+ : en consťquence le plomb et le fer sont attaquťs par H3O+ ; le dťtartrage par l'acide chlorhydrique n'est pas possible dans ce cas.
|
||||||||||||||||||||||||||||||||||||
|
|