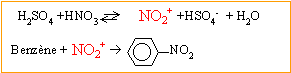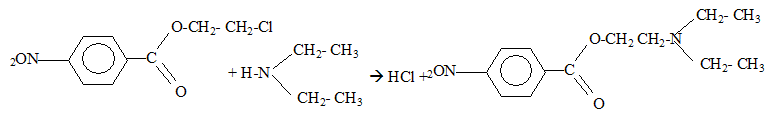|
|
||||||||||||||||
|
||||||||||||||||
|
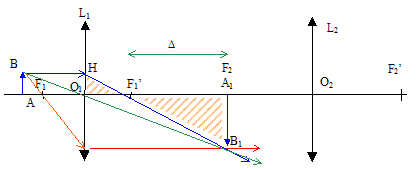
Un microscope optique comporte un oculaire de grossissement x10 et un objectif de grandissement x40. L'ouverture numťrique ( n sin u) de l'objectif vaut 0,65 et l'intervalle optique D est de 16 cm. Ce microscope est modťlisť par l'association de deux lentilles convergentes, de mÍme axe optique, et il est rťglť pour donner une image A'B' ŗ l'infini d'un objet AB rťel, perpendiculaire ŗ l'axe optique.
corrigť 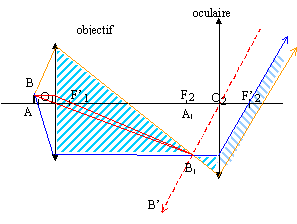
grandissement de l'objectif : les distances algŤbriques sont ťcrites en bleu et gras. g = A1B1/AB. La valeur absolue du grandissement |g| est ťcrite sur la monture de l'objectif : |g| = 40. grossissement commercial et puissance intrinsŤque : Le grossissement du microscope G est ťgal au produit du grandissement de l'objectif et grossissement de l'oculaire. Grandissement de l’objectif et grossissement de l’oculaire sont habituellement gravťs sur les montures de ces ťlťments. G = |g| Goc= 40*10 = 400 d ( dioptries) Puissance intrinsŤque = 4 G = 1600 d. distance focale image de l'objectif :
Les cŰtťs des deux triangles hachurťs O1HF'1 et A1B1F'1 sont proportionnels : A1B1 / O1H = A1F'1 / O1F'1 ; or O1H = AB ; A1F'1 = -D et A1B1 /AB = g ; d'oý g = -D / O1F'1 = -D / f'1. f'1 = -D / g =0,16 / 40 = 4 10-3 m = 4 mm. distance focale image de l'oculaire : Le grossissement commercial de l'oculaire est ťgal ŗ 0,25 fois la vergence de l'oculaire : voc = 10/0,25 = 40 ; f'2 = 1/40 = 0,025 m = 25 mm. distance du centre optique O1de l'objectif ŗ l'objet AB pour avoir une image finale A'B' ŗ l'infini : utiliser la formule de conjugaison : 1/ O1F'1 = 1/O1A1 -1/O1A avec O1A1 = D + f'1 = 0,164 m 1/O1A = -1/ O1F'1 + 1/O1A1 =-1/ 4 10-3 + 1/ 0,164 ; O1A = -4,1 10-3 m. Le pouvoir sťparateur du microscope est donnť par : e = 0,6 l /( nsin u) avec nsin u = 0,65 Si l = 500 nm e = 0,6 *500 10-9/0,65 = 4,6 10-7 m = 0,46 mm. la plus petite distance entre deux points de l’objet qui sont vus sťparťs ŗ travers l’instrument vaut 0,46 mm. Donc il est possible d'observer un staphylocoque de 1mm ŗ traves le microscope.
|
||||||||||||||||
|
On considŤre la rťaction de fusion suivante : 31X + 21Y --->baZ + 01n
1 u = 1,66 10-27 kg ; 1 u = 931,5 MeV c≤ ; MZ= 4,0 g/mol ; MX= 3,0 g/mol ; 1 eV= 1,6 10-19 J ; NA= 6,02 1023 mol-1. corrigť 31X + 21Y --->baZ + 01n Dťtermination des symboles chimiques X, Y, Z ainsi quedes valeurs de a et b : Le numťro atomique de X et Y est 1 : il s'agit de
l'ťlťment hydrogŤne conservation de la charge : 1+1=a d'oý a= 2 ; on identifie Z ŗ l'ťlťment hťlium. 31H + 21H --->42He + 01n Les rťactions de fusion dans l'univers, se produisent
dans les ťtoiles.
31H ---> AZX + -10 e particule b- ou ťlectron conservation du nombre de nuclťons : A=3 ; conservation
de la charge : Z= 2 ; on identifie X ŗ He.
l tĹ=ln2
soit l=ln2/ tĹ=ln2
/ 12,3 = 5,64 10-2 an-1 =
ln2/(12,3*365*24*3600)= 1,79
10-9 s-1.
quantitť de matiŤre (mol) = masse (g) / masse molaire (g/mol) = n = 0,1/3 = 3,33 10-2 mol nombre de noyaux contenus dans cet ťchantillon : N0=nNA=
3,33 10-2* 6,02 1023 =2,0 1022
noyaux.
N30 = N0 exp(-30l) = 2 1022 exp(-30/12,3) = 2 1022 *0,1844 = 3,68 1021 noyaux. l'activitť de cet ťchantillon sera : A30
= lN30
= 1,79 10-9 * 3,68 1021
= 6,58 1012
Bq.
|Dm|= |mn+mZ -mX-mY | =| 1,0087+4,0026 -2,0136-3,0155|= 1,78 10-2 u E= 1,78 10-2 * 931,5 = 16,58 MeV ou bien 16,56 106/1,6 10-19 = 2,65 10-12 J.
quantitť de matiŤre (mol) = masse (g) / masse molaire (g/mol) = n = 10/4 = 2,5 mol nombre de noyaux contenus dans cet ťchantillon : N0=nNA= 2,5* 6,02 1023 =1,5 1024 noyaux. E= 2,65 10-12 * 1,5 1024 = 4 1012 J. Comparaison de cette ťnergie avec celle libťrťe par la combustion d'une tonne de pťtrole ( 4,2 1010 J) : 4 1012 / 4,2 1010 = 95 tonnes de pťtrole.
|
||||||||||||||||
|
Le dihydrogŤne peut Ítre produit selon la rťaction suivante : CH4(g) + H2O(g) = CO(g) + 3H2(g) Donnťes ŗ 298 K :
corrigť enthalpie de rťaction, notťe DrHį1 ŗ 298 K : DrHį1 =DrHį(CO) + 3DrHį(H2)- DrHį(CH4) -DrHį(eau) DrHį1 = -110,52 + 3*0 +241,43+74,85 = 205,8 kJ mol-1. valeur positive, la rťaction est endothermique.
DrSį =Sį(CO) + 3Sį(H2)- Sį(CH4) -Sį(eau) DrSį =3*130,6+197,9-188,7-186,2 = 214,9 J mol-1 K-1. la stoechiomťtrie de la rťaction donne Dn =2 ( le nombre de moles de
produits est supťrieur au nombre de moles des rťactifs : donc DrSį
>0.
DrGį1
= DrHį1
-TDrSį
=205,8 103 -298 *214,9 = 141,8 103
kJ/mol.
DrGį1 = -RT ln K ; ln K = -DrGį1 /(RT) = -141,8 103 / (8,31*298) = -57,2 ; K= 1,35 10-25. K est trŤs faible : l'ťquilibre est fortement dťplacť
vers la gauche (rťaction inverse)
DrGį1 = DrHį1 -TinversionDrSį =0 Tinversion = DrHį1/DrSį =205,8 103 / 214,9 = 958 K.
|
||||||||||||||||
|
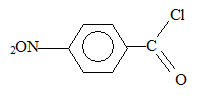
La synthŤse de la procaÔne peut Ítre rťalisťe de la maniŤre suivante :
corrigť La nitration du toluŤne C6H5-CH3 permet d'obtenir majoritairement le composť A : 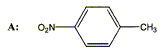 A : 4-nitrotoluŤne ; cette nitration s'effectue en prťsence du mťlange sulfonitrique.
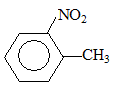
Il se forme ťgalement
un composť A' minoritaire( le groupe CH3 oriente
une seconde substitution en para et en ortho, mais en position il y a
gŤne stťrique) : A' est le 2-nitrotoluŤne ; L'oxydation par les
ions permanganate ŗ chaud en milieu acide du composť A conduit ŗ
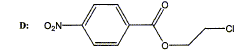
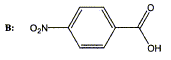
l'acide 4- nitrobenzoÔque B de formule semi-dťveloppťe / demi-ťquations ťlectroniques : ( couple MnO4-/Mn2+) : MnO4- + 8H+ + 5e-= Mn2++ 4H2O rťduction (1) ( couple C7H5NO4
/ C7H7NO2)
: C7H7NO2
+ 2H2O = C7H5NO4+
6H+ + 6e- oxydation (2) 6 fois (1) + 5 fois (2) donne : 6MnO4- +18H+ +5C7H7NO2 =6 Mn2++ 14H2O + 5C7H5NO4. La fonction acide
carboxylique de B est activťe par le chlorure de thionyle SOCl2
selon l'ťquation : B+SOCl2 = C+SO2+HCl L'action de C sur le composť HO-CH2-CH2-Cl conduit ŗ la formation d'un composť D et de chlorure d'hydrogŤne selon : C+ HO-CH2-CH2-Cl = D + HCl
type de rťaction :
estťrification D est traitťe par (C2H5)2NH
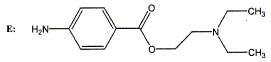
pour donner le composť E de formule brute : C13H18N2O4.
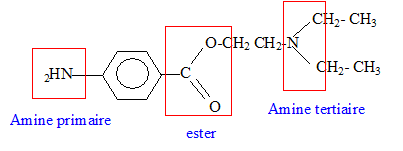
type de rťaction : substitution La rťduction de E par
le fer en milieu acide conduit ŗ la procaÔne :
|
||||||||||||||||
|
|
 .
Ecrire les demi-ťquations ťlectroniques ( couple MnO4-/Mn2+)
.
Ecrire les demi-ťquations ťlectroniques ( couple MnO4-/Mn2+)