|
-
Propagation d'une onde :
On fixe un vibreur ŗ l'extrťmitť d'une corde tendue. Une onde
sinusoÔdale de frťquence f = 25 Hz se propage le long de la corde. Le
milieu n'est pas dispersif.
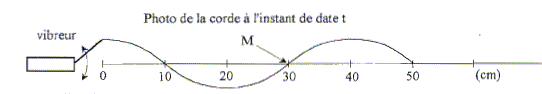
L'onde est transversale : sa direction de propagation est
perpendiculaire ŗ la direction de la dťformation du milieu.
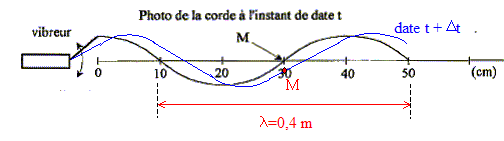
La cťlťritť de l'onde v est ťgale ŗ la longueur d'onde l (m)
multipliťe par la frťquence f (Hz).
l = 40 cm = 0,4 m ; f = 25 Hz d'oý v = 25*0,4 = 10 m/s.
Le milieu n'est pas dispersif : la cťlťritť de l'onde ne dťpend
pas de la frťquence de la source.
Au moment de la prise de vue, le point M descend.
Dans un milieu non dispersif, une onde rectiligne sinusoÔdale traverse
une fente dont la largeur "a", fixe, est de l'ordre de grandeur de la
longueur d'onde l.
L'ťcart angulaire vaut q= l/a : la diffraction est d'autant plus marquťe que cet
ťcart est important ( "a" ťtant fixť, l doit Ítre grand)
Or l = v/f ; si l est grand, la frťquence f est petite.
d'oý : la diffraction est d'autant plus marquťe si la frťquence est
petite ( la largeur de la fente ťtant fixťe et le milieu ťtant non
dispersif).
-
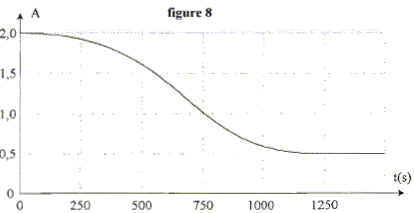
Radioactivitť :
Le graphe reprťsente l'ťvolution temporelle de l'activitť A d'un
ťchantillon de radon 222.
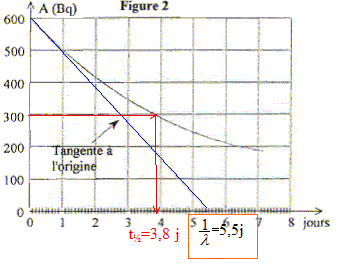
La demi-vie du radon 222 est : t1/2 = 3,8 jours
ŗ l'instant de date t = 1,0 jour, l'activitť est A=
500 Bq ;
Or A= lN ; N=A /l avec 1/l = 5,5 jours = 5,5*24*3600 secondes =4,75 105
s.
il reste N= 500* 4,75 105 =2,4 108 noyaux de
radon 222 dans l'ťchantillon.
-
…volution des systŤmes
ťlectriques :
La rťsistance du circuit de la figure
ci-dessous est rťglable.
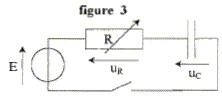
Le gťnťrateur dťlivre une tension constante E = 6,0 V. Le condensateur
a une capacitť C = 1,0 ĶF.
Un systŤme d'acquisition permet d'enregistrer l'ťvolution de la tension
aux bornes du condensateur en fonction du temps.
ņ l'instant de date t = 0 s, on ferme
l'interrupteur.
A l'instant de date t = 0 s, le condensateur n'a pas
eu le temps de se charger : la tension ŗ ces bornes est nulle.
En rťgime permanent l'intensitť du courant qui circule dans le circuit
est nulle.
i = dq/dt = Cduc/dt avec uc = E=constante ; en
consťquence duc/dt =0.
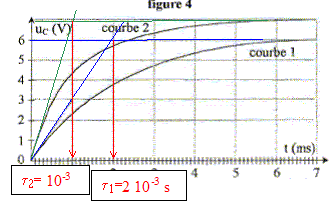
Pour obtenir la courbe 1, la valeur R est ťgale ŗ : t1=2
ms = 2 10-3 s ( lecture graphe)
de plus t1 =RC avec C= 10-6 F d'oý R= 2 10-3 /
10-6 = 2000 W.
courbe 2 : la valeur finale de uC vaut 7 V
; t2=1 ms = 1 10-3 s
de plus t2 =RC avec C= 10-6 F d'oý R= 10-3 /
10-6 = 1000 W.
-
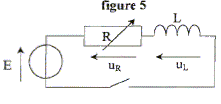
La rťsistance du circuit
ci-dessous est rťglable. Le gťnťrateur dťlivre une tension constante E
= 6,0 V. La bobine a une rťsistance interne nťgligeable devant R et une
inductance L. Un systŤme d'acquisition permet d'enregistrer l'ťvolution
au cours du temps de l'une des tensions indiquťes sur le schťma.
A l'instant de date t = 0 s, on ferme
l'interrupteur.
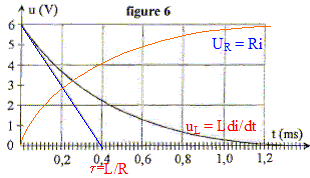
L'intensitť du courant qui circule dans le circuit vťrifie l'ťquation diffťrentielle :
uR= Ri ; uL= Ldi/dt
additivitť des tensions : uR+uL=E ; Ri + Ldi/dt =E.
Les courbes ci-dessous reprťsentent uL et uR :
en rťgime permanent l'intensitť est constante ; di/dt = 0 d'oý E=RImax
soit Imax= E/R
-
…volution des systŤmes
chimiques :
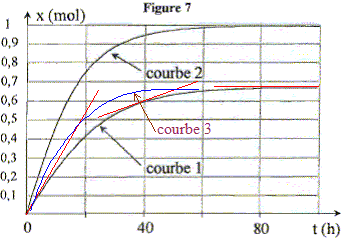
La courbe l ci-dessous reprťsente l'ťvolution au cours du temps de
l'avancement de la rťaction entre une mole d'acide ťthanoÔque et une
mole d'ťthanol ŗ 100įC sans catalyseur.
La rťaction conduit ŗ un ťquilibre
chimique.
A l'instant de date t = 0 h, la vitesse de la rťaction est maximale : la tangente
est presque verticale ; le coefficient directeur de la tangente est
proportionnelle ŗ la vitesse.
La vitesse de la rťaction diminue au cours du temps,
du fait de la disparition des rťactifs. Les tangentes sont de moins en
moins inclinťes sur l'horizontale.
Une ťlťvation de tempťrature du milieu rťactionnel, facteur
cinťtique, augmente la vitesse de rťaction.
L'ajout d'un catalyseur dans le
milieu rťactionnel permet d'atteindre plus rapidement l'ťquilibre sans
en changer la composition : la courbe 2 ne correspond pas ŗ l'ajout
d'un catalyseur. La courbe 3 convient.
-
On ťtudie la rťaction
d'oxydation de l'acide oxalique HOOC-COOH
(solution incolore) par l'ion permanganate
MnO4- (aq) en
milieu acide (solution de couleur
violette). Le suivi de la rťaction est
rťalisť par un enregistrement spectrophotomťtrique.
La transformation est totale. Parmi tous les rťactifs et produits
prťsents dans le milieu rťactionnel, seul
l'ion permanganate est colorť
et absorbe ŗ la longueur d'onde choisie.
L'ťvolution de l'absorbance du milieu rťactionnel en fonction du temps
est donnťe sur le graphe ci-dessous.
L'ion permanganate n'est pas le rťactif limitant : en effet
l'absorbance finale n'est pas nulle.
-
On rťalise une pile avec les
couples Fe3+(aq)/Fe2+(aq) et Ag+(aq)/Ag(s).
Fe3+(aq) +Ag(s) = Fe2+(aq) + Ag+(aq)
La constante d'ťquilibre associťe ŗ la rťaction vaut : K = 0,31.
Tous les ions en solution ont initialement la mÍme concentration :
[Fe2+(aq)]ini =
[Fe3+(aq)]ini = [Ag+(aq)]ini
= 0,20 mol/L
Quand le courant circule dans le circuit extťrieur,
la transformation qui s'effectue dans la pile est une transformation spontanťe.
Qr,i = [Fe2+(aq)]ini [Ag+(aq)]ini
/ [Fe3+(aq)]ini = 0,2.
Qr,i < K : le sens spontanť d'ťvolution de la rťaction
est le sens direct.
En multipliant par 2 la
concentration initiale des ions Ag+(aq) sans changer les
autres concentrations, Qr,i devient ťgal ŗ 0,4 :
Qr,i est alors supťrieur ŗ K : le sens spontanť d'ťvolution
de la rťaction est le sens inverse.
|