|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
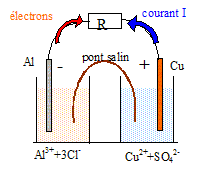
La pile cuivre aluminium :
corrigé polarité de la pile : le voltmčtre indique une valeur positive lorsque sa borne COM est reliée ŕ la plaque d'aluminium ; en conséquence celle-i est la borne négative de la pile. Quant ŕ la plaque de cuivre elle constitue la borne positive de la pile. rôle du pont salin : il assure la continiuté électrique et il contribue ŕ l'électroneutralité des solutions dans chaque bécher.
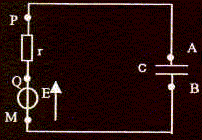
Dans les solutions et le pont salin, les cations positifs se déplacent dans le sens conventionnel du courant ; par contre les anions négatifs se déplacent en sens contraire du sens conventionnel du courant. les réactions aux électrodes : ŕ l'anode négative, oxydation Al = Al3+ + 3e-.(1) ŕ la cathode positive, réduction : Cu2+ + 2e- = Cu.(2) puis 2 fois (1) + 3 fois (2) donnent : 2Al + 3Cu2+ = 2Al3+ +3 Cu. avec K= 1020. Quotient de réaction initial : Q r i = [Al3+]i2/[Cu2+]i3 = 0,12 / 0,13 = 10. Q r i < K la réaction évolue dans le sens direct, de la gauche vers la droite, ce qui est cohérent avec le fonctionnement de la pile. Quantité d'électricité Q échangée en 1h 30 min si I= 40 mA = 0,04 A : Q= It = 0,04*3600*1,5 = 216 C ( 2,2 102 C ) Quantité de matičre d'électrons correspondante : Q= n(e-) F avec F= 9,65 104 C n(e-) =216/9,65 104 = 2,24 10-3 mol ( 2,2 10-3 mol) relation entre n(e-) et n(Al) : Al = Al3+ + 3e-. d'aprčs les coefficients de cette demi-équation : n(e-) = 3n(Al) ou n(Al) = 1/3 n(e-) =2,24 10-3 /3 = 7,46 10-4 mol ( 7,5 10-4 mol) perte de masse de l'électrode d'aluminium : m = n(Al) * M(Al ) = 7,46 10-4 *27 = 2,0 10-2 g. 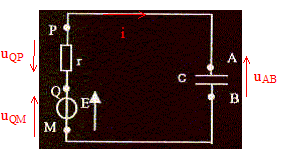 signe de la charge de l'armature A du condensateur lors de la charge : les électrons se déplacent en sens contraire du sens conventionel du courant ; l'armature B acquiert une charge négative ; l'armature A acquiert une charge positive. qA= CuAB, charge et tension aux bornes du condensateur sont proportionnelles ; le coefficient de proportionnalité est la capacité du condensateur, exprimée en farad (F). Le condensateur est soumis ŕ un échelon de tension E : 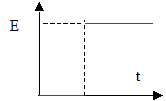
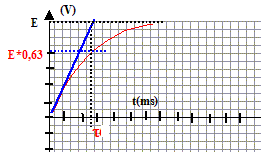
expression de la constante de temps t : équation différentielle relative ŕ la tension uAB : E= rC duAB/dt + uAB. C est la capacité du condensateur (farad) solution de cette équation différentielle : uAB =E(1-exp(-t/t)) dériver par rapport au temps : duAB/dt = E/t exp(-t/t) repport dans l'équation différentielle : E= rCE/t exp(-t/t)+E(1-exp(-t/t)) 0 = rC/t exp(-t/t)-exp(-t/t) relation vérifiée quel que soit le temps si t=rC la constante de temps t a la dimension d'un temps, s'exprime en seconde : r : résisatance soit tension / intensité C : capacité soit charge / tension et une charge est une intensité fois un temps d'oů C : intensité * temps / tension par suite rC a la dimension d'un temps. valeurs en fonction de E de la tension uAB aux dates : uAB(t)=E(1-e-1) = 0,63 E; uAB(3t)=E(1-e-3) =0,95 E ; uAB(5t)=E(1-e-5) =0,99 E ; uAB(10t)=E(1-e-10) = E ;
énergie maximale emmagasinée par le condensateur : ˝CE˛ = 0,5*0,1*1,8˛=0,16 J. Cette énergie est transférée au moteur ; ce dernier convertit cette énergie en énergie mécanique ( potentielle de pesanteur mgh) avec un rendement de 100% la hauteur maximale atteinte sera : 0,16/(mg) = 0,16 /(0,1*10) = 0,16 m.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Léthanoate de pentyle ou parfum de poire est plus connu sous le nom d'acétate d'amyle. Sa formule semi-développée est : 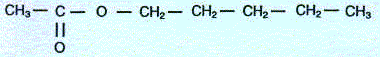 Etude théorique :
Etude cinétique :
corrigé étude théorique :
Dans cette molécule la fonction ester est présente. Cet ester est obtenu ŕ partir d'un acide carboxylique, l'acide éthanoďque CH3-COOH ( noté A) et d'un alcool primaire, le pentan-1-ol ( noté B) CH3-CH2-CH2-CH2-CH2OH Equation de la réaction conduisant ŕ l'ester : CH3-COOH + CH3-CH2-CH2-CH2-CH2OH = CH3-COO-CH2-CH2-CH2-CH2-CH3 + H2O ( eau) cette réaction porte le nom d'estérification. Etude cinétique : Mode opératoire permettant de suivre l'évolution de la quantité de matičre du réactif A : A l'instant initial, mélanger les réactifs, fractionner le milieu réactionnel en 10 parties identiques, placées dans un bain thermostaté. ŕ intervalle de temps régulier, prélever l'une des parties ; plonger l'erlenmeyer dans un bain d'eau glacée ( blocage cinétique) puis effectuer un dosage de l'acide restant par une solution titrante d'hydroxyde de sodium. rôle de l'acide sulfurique : catalyseur ; ce catalyseur accélčre la réaction ; il est régénéré ŕ la fin de celle-ci et en conséquence n'intervient pas dans l'équation de la réaction. tableau d'évolution :
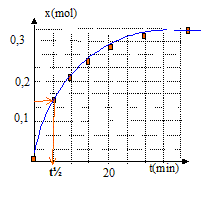
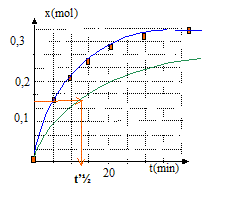
vitesse volumique v = 1/V dx/dt avec V = volume constant du milieu réactionel ( V=83 mL) La vitesse diminue au cours du temps car les concentrations (facteur cinétique) des réactifs diminuent. A partir de t= 50 min, l'avancement est constant : en conséquence la composition du milieu réactionnel n'évolue plus ; on atteind un état d'équilibre chimique. temps de demi-réaction t˝ : durée au bout de laquelle l'avancement est égal ŕ la moitié de l'avancement final t˝ voisin de 6 min Si la synthčse se fait sans ajout d'acide sulfurique, la vitesse de la réaction est plus faible : l'état déquilibre sera plus long ŕ atteindre, mais la composition de cet état ne changera pas ; dans ce cas le temps de demi réaction t'˝ sera supérieur ŕ la valeur précédente.( courbe verte ci-dessous)
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
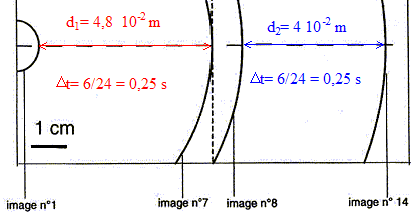
I- Étude sur une cuve ŕ ondes : On laisse tomber une goutte d'eau sur une cuve ŕ ondes. Le fond de la cuve ŕ ondes présente un décrochement de telle sorte que l'onde créée par la chute de la goutte d'eau se propage d'abord ŕ la surface de l'eau dont l'épaisseur au repos est e1 = 3 mm puis ensuite ŕ la surface de l'eau dont l'épaisseur au repos est e2 = 1 mm. On filme la surface de l'eau ŕ l'aide d'une webcam. Le clip vidéo est effectué avec une fréquence de 24 images par seconde. Le document 1 ci-dessous représente les positions du front de l'onde créée par la chute de la goutte d'eau, repérées sur les images n° 1, n° 7, n° 8 et n° 14 du clip. 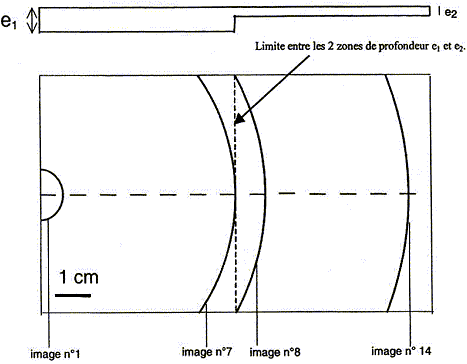
II- Ondes périodiques : On installe sur la cuve ŕ ondes un vibreur qui permet d'obtenir des ondes planes. La fréquence du vibreur a été fixée ŕ 24 Hz. Une source lumineuse éclaire la surface de l'eau. Cette lumičre traverse l'eau et est captée ensuite par la webcam. Le document 2 d'échelle 1 ci-dessous représente l'onde périodique obtenue ŕ partir d'une image du clip vidéo. 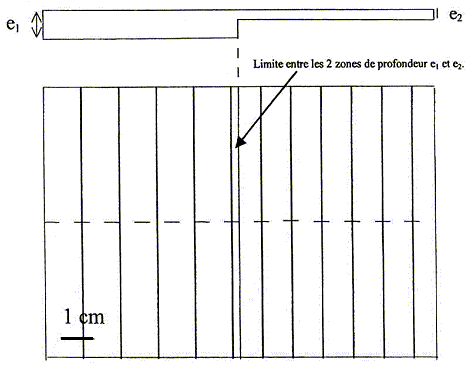
III - Un phénomčne caractéristique des ondes :
corrigé onde mécanique transversale : perturbation se propageant dans un milieu, sans transport de matičre ; la déformation du milieu est perpendiculaire ŕ la direction de propagation de l'onde : l'onde créée par la goutte d'eau sur la cuve ŕ ondes, appartient ŕ ce type d'ondes. onde mécanique longitudinale : perturbation se propageant dans un milieu, sans transport de matičre ; la déformation du milieu et la direction de propagation de l'onde ont la męme direction célérité c de cette onde pour les deux épaisseurs d'eau : Le clip vidéo est effectué avec une fréquence de 24 images par seconde : entre deux images il s'écoule 1/ 24 seconde. Entre les images 7 et 1 d'une part, et entre les images 14 et 8 d'autre part, il s'écoule 6/24 = 0,25 s.
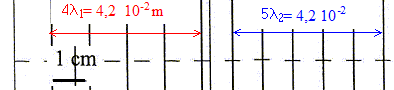
La célérité (m/s) est une distance (m) divisée par une durée (s) : c1 = 4,8 10-2 / 0,25 = 0,19 m/s ; c2 = 4,0 10-2 / 0,25 = 0,16 m/s La célérité c de l'onde diminue donc lorsque l'épaisseur de l'eau diminue. Ondes périodiques : La distance séparant deux franges brillantes (ou sombres) successives est la longueur d'onde, notée l, exprimée en mčtre. La longueur d'onde est égale ŕ la célérité c de l'onde multipliée parsa période temporelle T : l= cT = c/f, f étant la fréquence (Hz) Célérité c de l'onde périodique pour les deux épaisseurs d'eau de 3 et 1 mm : f = 24 Hz.
l1 = 4,2 10-2 / 4 = 1,05 10-2 m ; c1 = 1,05 10-2 * 24 = 0,25 m/s. l2 = 4,2 10-2 / 5 = 8,4 10-3 m ; c2 = 8,4 10-3 *24 = 0,20 m/s. La célérité c de l'onde diminue donc lorsque l'épaisseur de l'eau diminue.
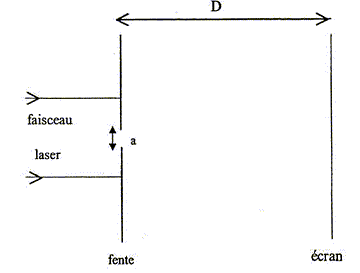
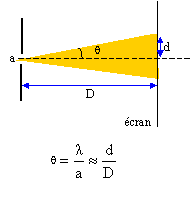
Un phénomčne caractéristique des ondes : Le phénomčne observé est la diffraction des ondes par une ouverture dont les dimensions sont du męme ordre de grandeur que la longueur d'onde l. Longueur d'onde de ce faisceau laser : q=l/a.
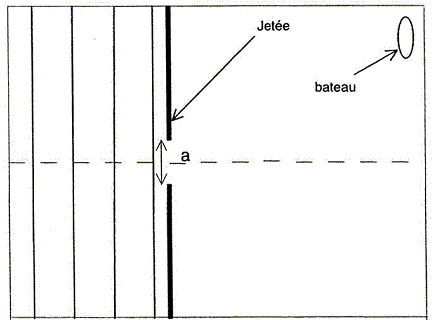
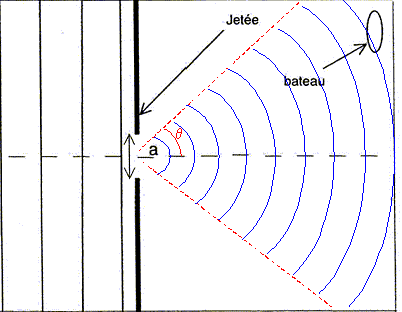
d'oů l = ad/D avec a = 0,08 mm = 8 10-5 m ; d = 0,5*4,7 cm = 2,35 10-2 m et D= 3,00 m. l = 8 10-5 * 2,35 10-2 / 3,00 = 6,2 10-7 m ( 6 10-7 m, "a" est donné avec un seul chiffre significatif) Étude sommaire de la houle : Les vagues sont espacées de 230 mčtres. Une vague remplace la précédente aprčs une durée de 12 secondes. La vitesse de déplacement des vagues ŕ la surface de l'océan vaut : 230/12 = 19 m/s. Cette houle arrive sur un port dont l'ouverture entre deux jetées a une largeur a = 200 m, valeur du męme ordre de grandeur que la longueur d'onde des vagues : on s'attend donc ŕ un phénomčne de diffraction avec q=l/a= 230/200 = 1,15 radian ou 66°. Le bateau ressent donc les effets de la houle.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
| |
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|