|
d'aprŤs bac S |
||||
|
||||
|
|
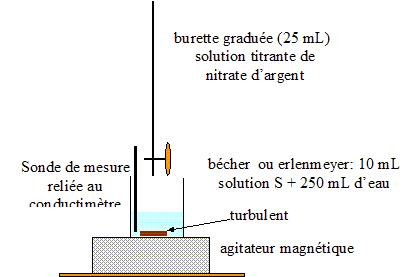
On prťlŤve un volume V0 = 20,0 mL de lait (solution S0) et on les introduit dans une fiole jaugťe de volume VS = 100,0 mL : le facteur de dilution F est ťgal ŗ : F= VS /V0 = 100/20 = 5. De plus F= C0 /CS d'oý : C0 =5CS. prťlever V1 = 10,0 mL de la solution S : verser un peu de solution S dans un bťcher, prendre une pipette jaugťe de 10,0 mL ( rincťe avec la solution S) surmontťe d'un pipeteur ; utiliser un autre bťcher pour placer ce prťlevement. schťma annotť du dispositif expťrimental de suivi conductimťtrique :
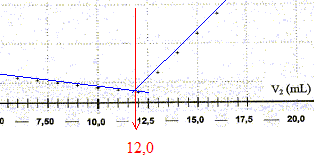
La conductivitť initiale de la solution est due ŗ tous les ions qu'elle contient et en particulier ŗ l'ion chlorure. variation de la valeur de la conductivitť s du milieu rťactionnel au cours du dosage : avant l'ťquivalence, les ions chlorure sont en excŤs, les ions argent ajoutťs sont tous consommťs ; on ajoute des ions nitrate d'oý l'expression de la conductivitť s du milieu rťactionnel : s = lCl- [Cl-] + lNO3- [NO3-]. Du point de vue de la conductivitť, tout se passe comme si on remplaÁait les ions chlorure par les ions nitrate ; de plus le volume de la solution est ŗ peu prŤs constant : or lNO3- <lCl- , en consťquence la conductivitť va diminuer. aprŤs l'ťquivalence, les ions chlorure ont disparu, les ions argent ajoutťs ne sont plus consommťs ; on ajoute des ions nitrate d'oý l'expression de la conductivitť s du milieu rťactionnel : s = lAg+ [Ag+] + lNO3- [NO3-]. Les concentrations de ces deux ions croissent et en consťquence la conductivitť va augmenter. L'abscisse du point particulier, intersection des deux segments de droites, apparaissant sur la courbe s = f(V2) , donne le volume de solution titrante ajoutť ŗ l'ťquivalence. V2E =12,0 mL
D'aprŤs les coefficients stoechiomťtriques de l'ťquation de rťaction : Ag+(aq) +Cl-(aq) = AgCl(s), ŗ l'ťquivalence la quantitť de matiŤre en ions argent introduits est ťgale ŗ la quantitť de matiŤre en ions chlorure initialement prťsents. C2V2E =V1CS d'oý CS =C2V2E /V1 = 5,00 10-3 * 12,0 / 10,0 = 6,00 10-3 mol/L en tenant compte de la dilution, C0 = 5 CS =3,00 10-2 mol/L. Masse d'ions chlorure prťsents dans 1 L de lait ťtudiť
: CS *M(Cl-) = 3,00 10-2 *35,5 =1,07 g/L.
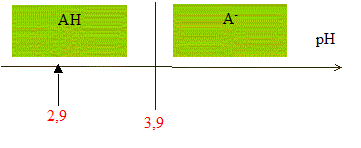
le pH initial du lait est pH= 2,9 ; l'ťquivalence est obtenue pour VBE= 12 mL de soude. Equation de la rťaction qui se produit lors du mťlange : HA + HO- = A- + H2O Une rťaction adaptťe ŗ un dosage doit Ítre totale et rapide. Expression de la constante de rťaction K correspondante : K= [A- ]/([HA][HO- ]) ( 1) de plus AH + H2O = A- + H3O+ avec Ka3 = [A- ][H3O+]/[AH] soit [A- ] / [AH] = Ka3 /[H3O+] repport dans (1) : K=Ka3 /([H3O+][HO- ]) = Ka3 / Ka1 = 10-3,9 / 10-14 = 1010,1. Je conclus : K ťtant trŤs grand, [HA]ťq , figurant au dťnominateur dans l'expression de K, est trŤs faible : la rťaction est donc bien totale. Utiliser un diagramme de prťdominance :
pH dťbut < pKa3 donc l'espŤce chimique prťdominante au dťbut du dosage est AH. HA(aq) et A-(aq) sont prťsents en quantitťs ťgales lorsque pH = pKa3 c'est ŗ dire ŗ la demi-ťquivalence de ce dosage ( V=ĹVB= 6 mL) quantitť de matiŤre d'acide lactique prťsente dans le volume VA de lait : ŗ l'ťquivalence, les quantitťs de matiŤre de rťactifs mis en prťsence sont en proportions stoechiomŤtriques : VACA= VBCB soit CA= VBCB / VA = 12,0*5,00 10-2 / 20,0 = 3,00 10-2 mol/L. soit 3,00 10-2 / 50 = 6,00 10-4 mol AH dans 20 mL de lait. Masse d'acide lactique prťsente dans un litre de lait : M(HA) CA= 90* 0,0300 = 2,7 g/L. M(acide lactique)= M(HA) = 90 g.mol-1 On considŤre qu'un lait frais a une concentration en acide lactique infťrieure ŗ 1,8 g.L-1 ; la valeur trouvťe, 2,7 g/L ťtant supťrieure ŗ 1,8 g/L, ce lait n'est donc pas frais..
|
|||
| |
||||
|
|