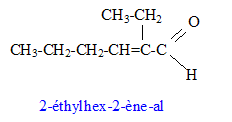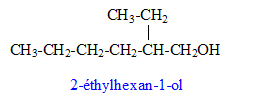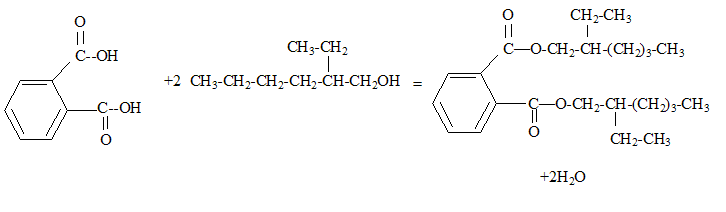|
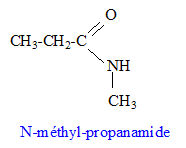
phtalate de di(2-ťthylhexyle), N-mťthyl-propanamide |
||||
|
||||
|
|
Un plastifiant du polychlorure de vinyle (PVC) est un diester aromatique qui peut Ítre synthťtisť par rťaction entre un alcool J et l’acide benzŤne-1,2-dicarboxylique.
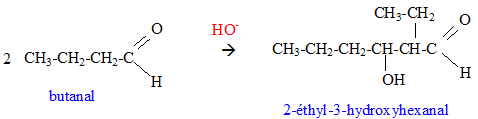
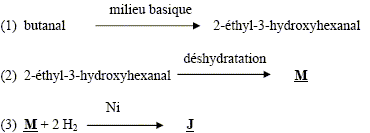
aldolisation : condensattion en milieu basique formule semi-dťveloppťe de M : Les rťactions de dťshydratation suivent la rŤgle de ZaÔtsev : l’alcŤne le plus substituť se forme prťfťrentiellement. formule semi-dťveloppťe de J : addition de H2 sur la double liaison carbone- carbone et rťduction de l'aldehyde en alcool primaire On note CH3-F-CH3 le 1,2-dimťthylbenzŤne CH3-F-CH3 + 4 H2O = HOOC-F-COOH + 12e- + 12H+ oxydation 2 Cr2O72- + 28 H+ +12e- = 4 Cr3+ + 14 H2O rťduction CH3-F-CH3 +2 Cr2O72- + 16H+ = HOOC-F-COOH + 4 Cr3+ + 10 H2O ťquation de la rťaction entre J et l’acide benzŤne-1,2-dicarboxylique :
Le phtalate de di(2-ťthylhexyle) (DEHP) est le plastifiant le plus utilisť de l'industrie du polychlorure de vinyle (PVC), Pour amťliorer le rendement de cette rťaction : utiliser l'un
des rťactifs en excŤs, ťliminer l'un des produits au fur et ŗ mesure
qu'il se forme
|
|||
|
Un amide primaire N-substituť A a une masse molaire M = 87 g.mol-1. Sa composition massique centťsimale est :C : 55,2 % ; H : 10,3 % ; O : 18,4 % ; N : 16,1 %. Masse atomique ( g/mol) : C : 12 ; H : 1,0 ; O : 16 ; N : 14 ; K : 39.
corrigť la formule brute de A : CxHyOz Nt. 12x/55,2 = 0,87 soit x= 4 ; y/10,3 = 0,87 soit y = 9 ; 16 z /18,4 = 0,87 soit z = 1 ; 14t/16,1 = 0,87 soit t =1 ; C4H9ON. ťquation de la rťaction de A avec la solution d’hydroxyde de potassium : amide primaire monosubstituť ŗ l'azote : R-CO-NHR' R-CO-NHR' + (K+ ; HO-)-->R-COO- + K+ + R'-NH2. Masse molaire de B : (R-COO- + K+ ) ou CnH2n-1 O2K : M= 14 n+70 Or B contient 34,9 % de potassium en masse : 39/0,349 = 14 n +70 soit n = 3 CH3-CH2-COO- + K+ : propanoate de potassium acide carboxylique B’ correspondant : acide propanoÔque CH3-CH2-COOH formule semi-dťveloppťe de l’amine C : CH3-NH2 mťthanamine formule semi-dťveloppťe de A : le spectre infrarouge de D prťsente une large bande
d’absorption vers 3400 cm-1 : la fonction chimique prťsente
dans D est une fonction alcool ( association par liaisons hydrogŤne
intermolťculaires) amine primaire traitťe par NaNO2 +HCl ŗ 5įC CH3 -NH2 + NaNO2 + HCl -->CH3-OH + N2 +H2O +NaCl
|
||||
|
|