|
|
||||||||||||||||||
|
||||||||||||||||||
|
|
La vitamine C ou acide ascorbique est vendue en pharmacie sous forme de comprimés. Données ŕ 25°C : masse molaire de l'acide ascorbique : 176 g/mol ; pKa = 4 masse d'acide ascorbique dans un comprimé : 500 mg d'aprčs le fabricant concentration de la soude utilisée : Cb= 0,02 mol/L
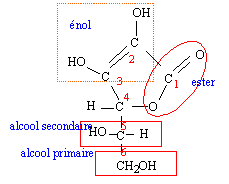
Un atome de carbone asymétrique est un atome de carbone tétračdrique relié ŕ 4 atomes ou groupes d'atomes différents. Les atomes de carbone n°4 et n°5 sont asymétriques
L'acide ascorbique est représenté par la formule simplifiée AH. équation bilan de la réaction de dosage : AH + HO-
donne A- + H2O Kr =[A-] / ([AH][HO-]) =[A-] [H3O+] / ([AH][HO-][H3O+] ) Or AH + H2O =H3O+ +A- ; Ka = [A-] [H3O+] /[AH] d'oů Kr= Ka/Ke = 10-4 / 10-14 = 1010. cette constante étant trčs grande, la réaction est totale. L'équivalence du dosage : ŕ l'équivalence, les quantités de matičre des réactifs mis en présence sont dans les proportions stoéchiométriques ; avant l'équivalence l'un des réactifs est en excčs ; aprčs l'équivalence, l'autre réactif est en excčs. Les coordonnées du point d'équivalence:
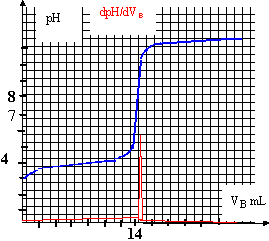
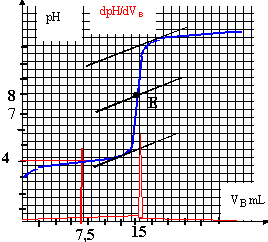
on utilise la méthode des tangentes ; on remarque que la courbe dérivée passe par un maximum ŕ l'équivalence. Les espčces chimiques majoritaires ŕ l'équivalence : ŕ
pH supérieur ŕ pKa ( 4 dans ce cas) la base conjuguée
prédomine. L 'espčce majoritaire ŕ l'équivalence est l'ion A-,
base conjuguée de l'acide AH ; la présence de la base faible A-
majoritaire, est responsable de la valeur pH =8 (milieu basique ) ŕ l'équivalence :C a Va = Cb Vb --> Ca = 0,02*15 / 10 = 0,03 mol L-1. soit 0,003 mol dans 100 mL, c'est ŕ dire dans un comprimé. masse d'acide ascorbique dans un comprimé : 0,003*176 =0,528 g ou 528 mg. écart relatif : 28 /500 =0,056 ( 5,6%); cet écart est faible. On ajoute de l'eau afin d'immerger correctement la sonde du pH-mčtre ; l'eau n'apportant pratiquement pas d'ion oxonium, le volume de soude ajouté ŕ l'équivalence ne sera pas modifié. A la demi équivalence du dosage acide faible base forte, le pH est égal au pKa du couple acide base faible. lecture graphique : ˝ Vb équi =7,5 mL et pH voisin de 4 soit Ka voisin de 10-4. choix d'un indicateur coloré : Le changement de couleur de l'indicateur coloré permet de repčrer l'équivalence. La zone de virage de l'indicateur coloré doit contenir le pH du point équivalent ( soit pH=8 dans ce cas) : on choisit donc le rouge de crésol.
|
|||||||||||||||||
|
|