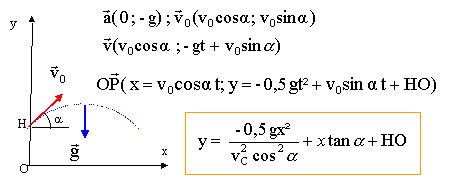|
Haut parleur ; Projectile ; eau de Javel ; spectrophotomťtrie ; ťquilibre chimique physique 1 h ; chimie 0,5 h ; d'aprŤs concours kinť Rennes 2005 |
|||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
|
|
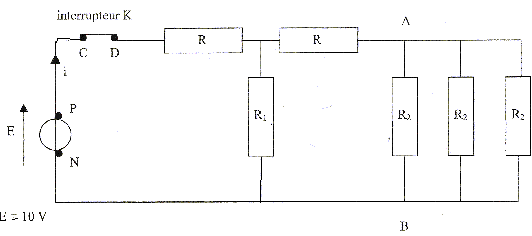
Associations de rťsistors (6 pts) Pour chaque rťponse donner l'expression littťrale, puis la valeur de la grandeur rechechťe.
corrigť entre A et B, trois rťsistors identiques en dťrivation : rťsistance ťquivalente R4= R2/3 = R puis R et R4 en sťrie, ťquivalents ŗ :R5=R+R4 = 2R puis R1 et R5 en parallŤle, ťquivalent ŗ : R6= R1R5/(R1+R5)=2R*2R/(4R) = R puis R en sťrie avec R6 : Rťqui = R+R6 = 2R= 20 ohms. I= E/Rťqui = 10/20 = 0,5 A.
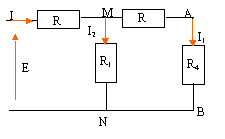
I=I1+I2 avec R1I2 = (R+R4)I1 ; 2RI2 = (R+R)I1 ; I1=I2 = ĹI UAB= R4I1
= RĹI= 10*0,22 = 2,5 V ; UDC=0 , interrrupteur fermť.
R4=R/3 ; R5=R+R/3=4R/3 ; R6 = R1R5/(R1+R5)=4 R/7 ; Rťqui = R+4R/7 = 11R/7. E= Rťqui I =11R/7 I soit R= 7E/(11I) = 70 / (11*0,4) = 15,9 W. Energie fournie par le gťnťrateur : E(V) I(A) t(s) = 10*0,4*60 = 240 J. Energie dissipťe dans les rťsistors : dans R situť ŗ gauche de M : RI≤ t = 15,9*0,4≤*60 = 152,6 J dans le rťsistor R situť entre M et A : RI1≤t avec : R1I2 = (R+R4)I1 ; RI2 = (R+R/3)I1 ; I1+I2 = I I1 = 3I/7 = 0,171 A ; I2 = 7/3 I1 = 0,229 A RI1≤t =15,9*0,171≤*60 = 27,8 J dans le rťsistor situť entre M et N : RI2≤t = 15,9 * 0,229≤*60 = 50 J dans R4 : R4I≤1 t = 5,3*0,171≤*60 = 9,4 J. interrupteur K ouvert : UAB=0 et UDC= - E = -10 V.
|
||||||||||||||||||||||||||||||
|
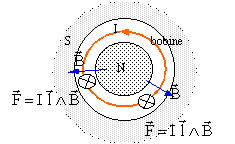
Un haut parleur est posť sur une table horizontale, dŰme vers le haut. 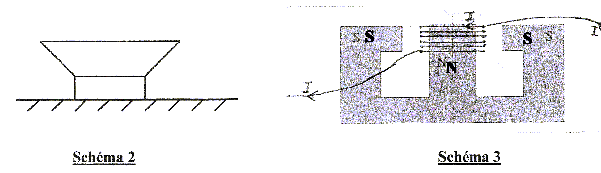
corrigť La bobine susceptible de se dťplacer, traversťe par un courant I, placťe dans un champ magnťtique, est soumise aux forces de Laplace.
Le forces de Laplace sont verticales, vers le bas.( vers le haut, si I change de sens) A l'ťquilibre la membrane ( solidaire de la bobine et du cŰne) est soumise ŗ la force de Laplace, verticale, vers le haut , valeur n B I l ( n : nombre de spires de la bobine) et au poids des masses marquťes , vertical, vers le bas, valeur mg. Ces forces sont opposťes et ont m^me valeur : mg = n B I l la masse et l'intensitť sont proportionnelles.
l'une des mesures est fausses ; l'affirmation ci-dessus est bien vťrifiťe. |
|||||||||||||||||||||||||||||||
|
Une bille d'acier que l'on suppose ponctuelle, est lancťe vers le haut ŗ t=0 avec une vitesse v0 faisant un angle a avec l'horizontale d'une hauteur H= 6,0 m au dessus du sol. On nťglige les frottements avec l'air. Le repŤre est tel que l'axe Ox est horizontal et se trouve au niveau du sol, l'axe Oy est vertical vers le haut. A t=0 , les coordonnťes de la bille sont (0 ; 6).
Au sommet S la vitesse est horizontale : -gt + v0sin a=0 soit t = v0sina/ g. xS= v0≤ sina cosa / g = v0≤ sin(2a)/(2g) yS= -Ĺ g v0≤ sin≤a/g≤ + v0≤ sin≤a/g + HO = Ĺv0≤ sin≤a/g + HO (yS-HO)/xS= Ĺtan a soit tan a = 2*(6,4-6)/1 = 0,8 ; a = 38,66 į. v0≤ = 2gxS/ sin(2a) =
2*9,8*1/sin 77,3) = 20,1 soit v0 = 4,48 m/s.
en H : Ĺmv≤0 + mgOH ; en B : Ĺmv≤B ( O : origine de l'ťnergie potentielle de pesanteur) v≤B = v≤0 + 2gOH = 4,48≤+2*9,8*6 = 137,7 ; vB= 11,73 m/s. au sol : xB= v0sin a t = 4,48 cos 38,66 t = 3,5 t. yB=0 = -4,9 t≤ + 4,48*sin 38,66 t + 6 ; -4,9 t≤ + 2,8 t+6 = 0 rťsoudre ; on trouve t= 1,428 s. par suite xB= 3,5*1,428 = 5 m. ťquation horaire du mouvement de la voiture : x= Vt + x0 = 5t + x0 ; ŗ t = 1,428 s, x= xB=5 m ; x0 = x-Vt= 5-5*1,428 = -2,14 m ( ŗ t=0, la voiture est 2,14 m ŗ gauche de O).
|
|||||||||||||||||||||||||||||||
|
Vm= 22,4 L/mol ( C.N.T.P) ; Vm= 24 L/mol
ŗ 20įC sous 1 bar. L'eau de javel : (2 pts) L'eau de javel est obtenue par l'action du dichlore gazeux sur une solution d'hydroxyde de sodium. Le principe actif de l'eau de Javel est l'ion hypochlorite ClO-(aq) qui est responsable de l'action dťcolorante sur les textiles.On caractťrise la teneur en ion hypochlorite par le degrť chloromťtrique. : c'est le nombre de litres de dichlore mesurť dans les conditions normales de tempťrature et de pression, qui sont absorbťs lors de la prťparation de 1 L d'eau de Javel.
corrigť Cl2(g) + 2HO- = ClO- + Cl- + H2O Le dichlore se dismute : Cl2(g) + 2e- = 2Cl- rťduction du dichlore Cl2(g) + 4HO- = 2ClO-+ 2e- +2 H2O oxydation du dichlore 12įCh, donc 12 L de dichlore dissous dans 1 L de solution Qtť de matiŤre de dichlore (g) = volume (L) / volume molaire( L/mol) (CNTP) = 12 / 22,4 = 0,536 mol soit [ClO-]= 0,536 mol/L.
|
|||||||||||||||||||||||||||||||
|
En solution aqueuse le peroxyde d'hydrogŤne H2O2 rťagit lentement avec l'ion iodure I-(aq). Le diiode en solutionprťsente un maximum d'absorption vers lmax= 350 nm. A cette longueur d'onde une solution aqueuse de diiode de concentration [I2]=0,7 10-5 mol/L a une absorbance Al= 1,75. On rappelle que l'absorbance d'une solution est proportionnelle ŗ sa concentration, loi de beer-Lambert. Dans la cuve du spectrophotomŤtre on mťlange 3,0 mL de solution de iodure de potassium accidifiť, de concentration [I-]=0,01 mol/L avec un volume de 0,5 mL d'une solution de peroxyde d'hydrogŤne, de concentration [H2O2]= 5 10-5 mol/L. On relŤve l'absorbance en fonction du temps :
corrigť Cette rťaction peut Ítre suivie par spectrophotomťtrie, car seul l'ion iodure prťsente une forte absorption ŗ la longueur d'onde choisie. H2O2 + 2e- +2H+= 2H2O rťduction 2I- = I2 + 2e- oxydation bilan : H2O2 +2I- +2H+ = I2 +2H2O Qtť de matiŤre initiale d'ion iodure : volume (L) * concentration = 3 10-3 * 0,01 = 3 10-5 mol. Qtť de matiŤre initiale de H2O2 : 0,5 10-3 * 5 10-5 = 2,5 10-8 mol (en dťfaut) Qtť maximale de matiŤre I2 : 2,5 10-8 mol dans 3,5 mL ; [I2]max = 2,5 10-8 / 3,5 10-3 = 7,14 10-6 mol/L Une solution aqueuse de diiode de concentration [I2]=0,7 10-5 mol/L a une absorbance Al= 1,75 : Al= k [I2] avec k une constante ťgale ŗ : 1,75 / 0,7 10-5 = 2,5 105 L mol-1. Aoo= k [I2]max 2,5 105 *7,14 10-6 =1,785. L'absorbance Aoo est pratiquement ťgale ŗ l'absorbance mesurťe ŗ t = 30 min. Donc la rťaction est pratiquement terminťe ŗ t = 30 min.
|
|||||||||||||||||||||||||||||||
|
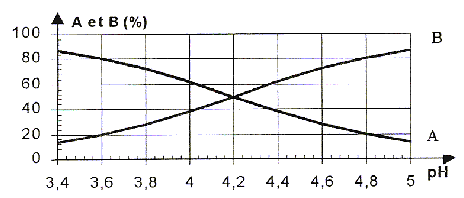
Ce diagramme permet de dťfinir les domaines de prťdominance ainsi que la distribution des espŤces donnťes C6H5-COOH ( notť A) et C6H5-COO- ( notť B) en solution aqueuse en fonction du pH de la solution. On ťtudie la transformation rapide associťe ŗ la rťaction acido-basique ŗ 25 įC C6H5-COOH + H2O = C6H5-COO- + H3O+.
corrigť C6H5-COOH + H2O = C6H5-COO- + H3O+ ou A + H2O = B +H3O+ Qr,i =[B]i[H3O+]i/[A]i avec[B]i/[A]i =0,2/0,8 = 0,25 ( lecture graphe ŗ pH=3,6) Qr,i =0,25 10-3,6 =6,27 10-5. or la constante d'ťquilibre vaut : pKa= 4,2 soit Ka = 10-4,2 =6,3 10-5.( lecture graphe ŗ l'intersection des courbes) Qr,i = Ka, donc l'ťquilibre est atteint.
Qr =[B][H3O+]/[A] =4* 10-4,8 =6,34 10-5. Qr = Ka, donc l'ťquilibre est atteint. |
|||||||||||||||||||||||||||||||
|
L'acťthylŤne C2H2 peut Ítre fabriquť par action de l'eau sur le carbure de calcium CaC2(s). Il se forme ťgalement de l'hydroxyde de calcium Ca(OH)2 (s). L'acťthylŤne rťagit avec le dioxygŤne de l'air avec formation de dioxyde de carbone et d'eau. Il se produit une flamme ťclairante. Un spťlťoloque utilise une lampe ŗ acťthylŤne qui consomme 10 L( volume mesurť ŗ 20įC et sous 1,013 105 Pa) de ce gaz par heure de fonctionnement. Il dťsire disposer de 10 heures d'ťclairage mais il souhaite Ítre chargť au minimum. Calculer la masse de carbure de calcium et d'eau qu'il doit emporter.
corrigť CaC2(s) + 2H2O = C2H2 +Ca(OH)2 (s). Qtť de matiŤre acťthylŤne = volume (L) / volume molaire (L/mol) = 100 / 24 = 4,17 mol. n(CaC2) =4,17 mol ; n(H2O) =2*4,17 = 8,34 mol masse (g) = masse molaire (g/mol) * qtť de matiŤre (mol) m((CaC2) =( 40,1+2*12) * 4,17 =267,3 g. m(eau) = 18*8,34 =150,1 g. |
|||||||||||||||||||||||||||||||
|
|