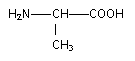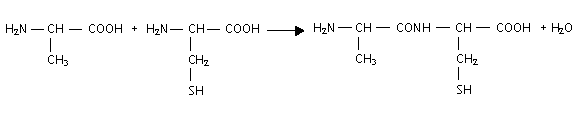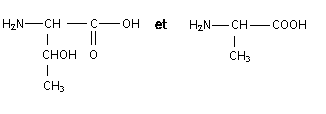|
|
||||
|
|
||||
|
||||
|
|
Donnťes : Masse molaire atomique du chlore : MCl = 35,5 g.mol-1. On rappelle qu'un oxydant est une espŤce chimique capable de gagner des ťlectrons alors qu'un rťducteur est une espŤce chimique capable de cťder des ťlectrons. L'eau de Javel est obtenue par dismutation du dichlore Cl2 en milieu basique. L'ťquation de la rťaction de dismutation s'ťcrit : Cl2 + 2(Na+ + HO-) ---> Na+ + ClO- + Na+ + Cl- + H2O.
corrigť Cl2 + 2e- = 2Cl-. le chlore gagne des ťlectrons : c'est l'oxydant du couple redox Cl2/Cl-. On appelle degrť ou titre chloromťtrique d'une eau de Javel le volume de dichlore, mesurť en litres dans les conditions normales de tempťrature et de pression, nťcessaire ŗ la fabrication d'un litre de cette eau de Javel. masse molaire du dichlore : 35,5*2 = 71 g/mol. quantitť de matiŤre n (mol) de dichlore = masse (g) / masse molaire (g/mol) = 35,5/71 = 0,5 mol. degrť chloromťtrique de l'eau de Javel ainsi fabriquťe : 11,2 į Chl. cet ajout d'eau dans la solution est une dilution. le degrť chloromťtrique t de l'eau de Javel obtenue est 1,12 įChl car on a diluť 10 fois la solution initiale ( volume initial = 1 L ; volume final = 10 L) 2I- + ClO- + H2O = I2
+ Cl- + 2HO-.
|
|||
|
Le molybdŤne 9942Mo est un radionuclťide dont la dťsintťgration spontanťe produit du technťtium 9943Tc.
corrigť 9942Mo = 9943Tc +AZX la charge ťlectrique se conserve : 42 = 43 + Z soit Z= -1 le nombre de nuclťons se conserve : 99 = 99 +A soit A=0 la particule X est identifiťe ŗ un ťlectron. La "pťriode radioactive" ou demi-vie d'un radionuclťide est la durťe au bout de laquelle la moitiť des noyaux radioactifs initiaux s'est dťsintťgrťe. C'est encore la durťe au bout de laquelle l'activitť de l'ťchantillon est divisťe par deux. au bout de 6 heures A1 = ĹA0 = 0,5 * 5,6 107 = 2,8 107 Bq. au bout de 12 heures A2 = ĹA1 = A0/22=0,25 * 5,6 107 = 1,4 107 Bq. 120 h correspondent ŗ 20 pťriodes. au bout de 120 heures A20 = A0/220 = 5,6 107 /220 = 53 Bq.( la dose est inactive) 1 jour = 24 h donc 120 h = 5 jours (moins d'une semaine). Un examen qui utilise le technťtium ne peut pas Ítre rťalisť quelques semaines aprŤs l'injection de la dose.
|
||||
|
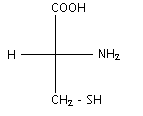
La cystťine est un acide a -aminť de formule semi-dťveloppťe : 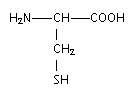
corrigť 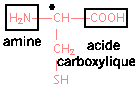
un carbone asymťtrique est liť ŗ qutre atomes ou groupes d'atomes diffťrents.
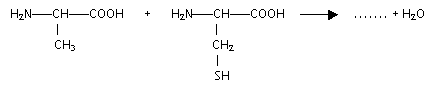
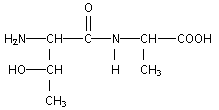
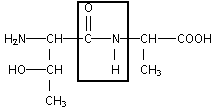
encadrer la liaison peptidique : formules semi-dťveloppťes des acides a -aminťs mis en jeu dans la synthŤse de ce dipeptide
|
||||
|
|