|
lancer
du poids d'aprÒs
bac Nlle CalÕdonie ( avec calculatrice)- d'aprÒs "LabolycÕe"
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
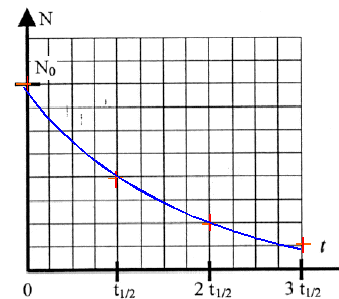
corrigÕ Le noyau 13153I est composÕ de 53 protons et 131-53=78 neutrons. QuantitÕ de matiÒre correspondant Á 1,00 çg de l'isotope : masse(g) / masse molaire (g/mol) n =10-6 / 131 =7,63 . 10-9 mol Dans une mole d'atomes il y a 6,02 1023 atomes : nombre d'atomes N0 = n NA = 7,63 . 10-9 mol * 6,02 . 1023 = 4,60 1015 atomes Equation de dÕsintÕgration : 13153I = AZX + 0-1e conservation du nombre de nuclÕons : 131 =A+ 0 donne A=131 conservation de la charge : 53=Z-1 d'oª Z=54 et X est le xÕnon. La loi de dÕcroissance est donnÕe par : N(t) = N0 e-lt. La demi-vie reprÕsente la durÕe au bout de laquelle la moitiÕ de la quantitÕ initiale de noyaux radioactifs s'est dÕsintÕgrÕe. Á t = t1/2, on a N(t) = § N0 = N0 e(-lt§). ln § = -ln2 = -lt§ soit ln2 = lt§ A chaque fois qu'une durÕe Õgale Á une demi-vie s'est ÕcoulÕe, la moitiÕ des noyaux radioactifs initialement prÕsents disparaŸt
dÕriver par rapport au temps : N(t) = N0 e-lt. dN(t)/dt = N0(-l)e-lt= -lN(t) ; |dN(t)/dt|=A= lN(t) A t= 0, on a A0 = l N0 ; or l = ln2 / t§ d'oª A0 =N0 ln2 / t§ Application numÕrique : t§=8*24*3600=6,91 105 s ; A0 = 4,6 1015 *ln2/6,91 105= 4,61 109 Bq. A t = 4 heures = 4*3600= 1,44 104 s : A = lN(t) =lN0e-lt avec l =ln2 / t§ = ln2/(8*24*3600)=1,0 10-6 s-1 ; l t = 1,0 10-6 *4*3600=1,44 10-2. A = 4,6 1015 *1,0 10-6 exp(-1,44 10-2)= 4,53 109 Bq. La perte relative
vaut : (4,61-4,53)/4,6=0,017 soit 1,7 %.
Par calcul du temps au bout duquel l'activitÕ de l'iode vaut 4,53 109 Bq. A = A0e-lt avec l =ln2 / t§ = ln2/(13,2*3600)=1,46 10-5 s-1 ; 4,53 109 = 4,61 109 exp(-1,46 10-5t); exp(-1,46 10-5t)=0,98 -1,46 10-5t = ln 0,98= -1,75 10-2 ; t =1,75 10-2 / 1,46 10-5= 1,84 105 =1198 s voisin de 20 min.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
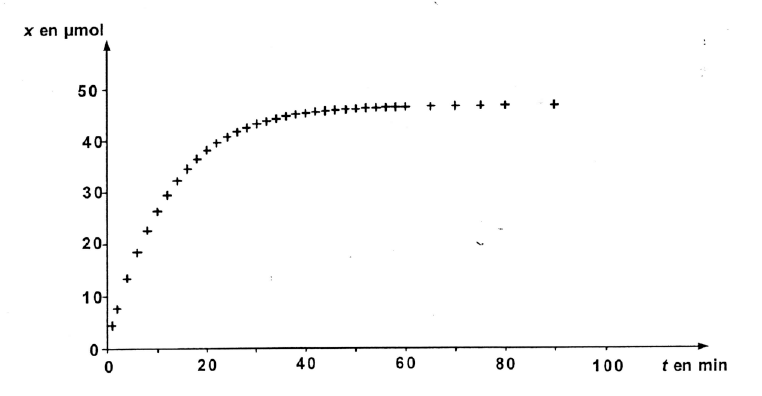
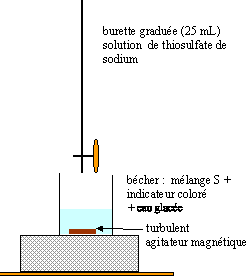
Les ions iodures I- rÕagissent avec les ions thiosulfate S2O82-. L'Õquation associÕe Á cette rÕaction s'Õcrit : 2I-(aq) + S2O82-(aq) = I2(aq) + 2 SO42-(aq) (1) En prÕsence d'ion iodure, le diiode se transforme en triiodure I3- de couleur brune. Pour simplifier l'Õcritue, on raisonnera Á partir de l'Õquation (1) sans tenir compte de la formation des ions triiodure. A un instant pris comme origine des dates (t=0), on rÕalise un mÕlange rÕactionnel S Á partir d'un volume V1=10,0 mL de solution aqueuse d'iodure de potassium ( K+ ; I-) de concentration molaire en solutÕ apportÕ c1= 0,50 mol/L et d'un volume V2 = 10,0 mL d'une solution de peroxodisulfate de sodium (2Na+ ; S2O82-) de concentration molaire en solutÕ apportÕ c2=5,0 10-3 mol/L.
corrigÕ RÕaliser un suivi conductimÕtrique, la solution contenant des ions dont les concentrations varient. A = k c d'oª k = A/c =1,7 / 5 10-3 = = 3,4 102 L.mol-1. QuantitÕ de matiÒre en diiode (mol) = concentration (mol/L) * volume de la solution (L) nI2 (t) = c VTotal = c (V1 + V2) = A(t) / k (V1 + V2) A t = 90 min, A (t)= 0,79, d'oª nI2 =0,79/340( 10 +10)10-3 = 4,6 10-5 mol. La vitesse volumique v de rÕaction est proportionnelle Á dx/dt, coefficient directeur de la tangente Á la courbe au point considÕrÕ. Or les tangentes Á la courbe sont de plus en plus inclinÕes sur l'horizontale lorsque le temps augmente. Le coefficient directeur de ces droites tangentes,et en consÕquence la vitesse, est maximum Á t =0 puis diminue pour atteindre une valeur nulle (partie horizontale de la courbe). La concentration des rÕactifs, un facteur cinÕtique, est maximum au dÕpart puis diminue car les rÕactifs sont consommÕs : en consÕquence la vitesse de rÕaction diminue au cours du temps. En augmentant la
tempÕrature (facteur cinÕtique), on peut obtenir plus rapidement la
mõme quantitÕ final de diiode.
L'Õquivalence correspond au changement de rÕactif limitant. A l'Õquivalence
les quantitÕs de matiÒre des rÕactifs sont en quantitÕs
stoechiomÕtriques
nI2 =xÕqui nI2 = 0,5* 2,5 10-3* 9,2 10-3 = 1,15 10-5 mol de diiode dans 5 mL Donc dans 20 mL
du mÕlange rÕactionnel S : 4*1,15 10-5 = 4,6 10-5 mol.
I2/I- : 2 I- = I2 + 2 e- oxydation S2O82- / SO42- : S2O82- + 2 e- = 2 SO42- rÕduction
si S2O82-en dÕfaut : 5 10-5 -xmax =0 soit xmax =5 10-5 mol La quantitÕ maximale de diiode formÕe nI2 = 5 10-5 mol. L'Õcart relatif vaut : (5-4,6)/5 = 0,080 soit 8,0 %. L'Õcart est infÕrieur Á 10% : le rÕsultat expÕrimental est en accord avec le rÕsultat thÕorique.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
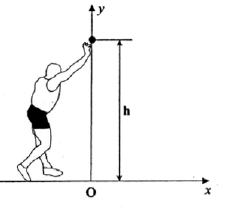
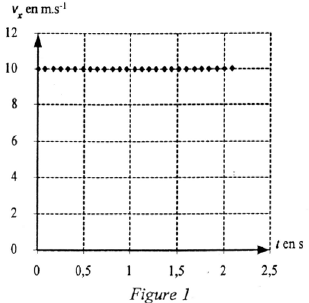
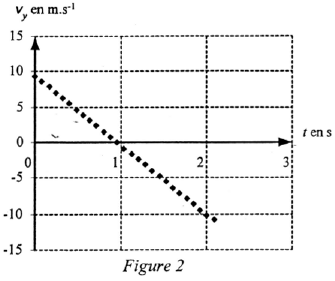
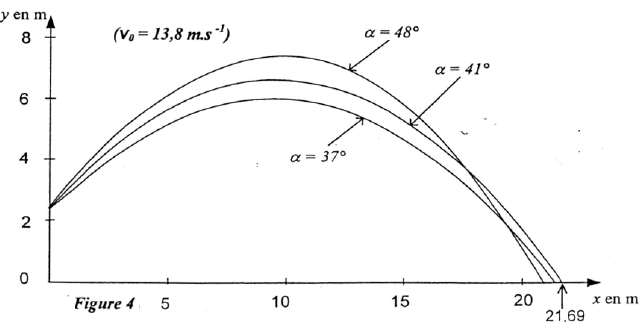
Lors des derniers championnats du monde, le vainqueur du lancer du poids a rÕussi un jet Á une distance D= 21,69 m. Pour simplifier le raisonnement on ne travaillera que sur le centre d'inertie du boulet ( nom courant donnÕ au poids) . l'entraŸneur de l'un de ses concurrents souhaite Õtudier ce lancer. Pour cela il dispose pour le centre d'inertie du boulet, en plus de la valeur 21,69 m du reccord, de la vitesse initiale v0= 13,7 m/s mesurÕe Á l'aide d'un cinÕmomÒtre et de l'altitude h=2,62 m. Un mogiciel informatique lui permet de rÕaliser une simulation de ce lancer et de dÕterminer la valeur de l'angle du vecteur vitesse initiale avec l'horizontale a=43¯. L'entraŸneur a ÕtudiÕ le mouvement du centre d'inertie du boulet et a obtenu 3 graphes : le graphe de la trajectoire y=f(x) du boulet, les graphes vx et vy en fonction du temps oª vx et vy sont les composantes horizontale et verticale du vecteur vitesse. Pour chacun des graphes, les dates correspondant Á deux points successifs sont sÕparÕs par le mõme intervalle de temps.
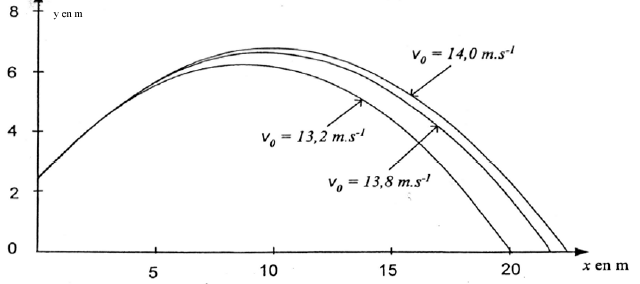
corrigÕ Quelle que soit la date, en particulier Á t=0, et Á la date correspondant au passage au sommet S de la trajectoire, la composante v0x de la vitesse est constante et vaut 10,0 m.s-1. En consÕquence, suivant l'axe Ox, le mouvement est uniforme. A t = 0, sur la figure 2 on dÕtermine : v0y = 9,40 m.s-1. La valeur v0 du vecteur vitesse initial est donnÕe par : v0ý= racine carrÕe (v0yý + v0xý) v0 =(9,4ý+10ý)§=13,7 m.s-1. De plus tan a =v0y/v0x = 9,4/10 = 0,94 ; soit a = 43¯ Ces valeurs correspondent Á celles donnÕes dans le texte. Les caractÕristiques du vecteur vitesse au sommet S: sa direction est horizontale, son sens est celui du mouvement et sa valeur vS = 10 m.s-1.
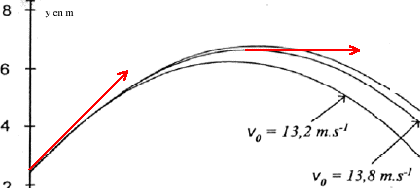
La valeur de la poussÕe d'ArchimÒde exercÕe par l'air sur le boulet : PA = m' V g La valeur du poids du boulet : P = m g = m V g Faire le rapport PA/P =m'/m= 1,29/7100=1,8 10-4 soit 0,018 % : la valeur de la poussÕe d'ArchimÒde est donc nÕgligeable devant le poids du boulet. Bilan des forces : le poids (les autres forces sont nÕgligeables) D'aprÒs la 2Òme loi Newton, le vecteur accÕlÕration est Õgal au vecteur champ de pesanteur, vertical, dirigÕ vers le bas, de valeur Õgale Á g. Projection du vecteur accÕlÕration sur le systÒme d'axes (O,x,y), on a : (0 ; -g) La vitesse est une primitive de l'accÕlÕration : vx(t) = v0x = v0 cos a. vy(t) = - g t+ v0y = -g t + v0 sin a. Le vecteur position est une primitive du vecteur vitesse et Á t=0 : x0=0 et y0=h x(t)= v0 cos a t (1) ; y(t) = -§gtý + v0 sin a t + h (2) (1) donne t = x(t)/ v0 cos a repport dans (2) : y = -§gxý/( v0 cos a )ý + tan a x + h C'est l'Õquation de la trajectoire du centre d'inertie du boulet. distance horizontale xmax = D du jet : dÕriver y par rapport Á x et annuler cette dÕrivÕe y'= -gxmax/( v0 cos a )ý + tan a =0 ; gxmax = ( v0 cos a )ý tan a D= xmax = v0ý sin a cos a /g = v0ý sin (2a ) /(2g ) Quand v0 augmente ( a Õtant constant) la distance horizontale D du jet augmente. Quand a augmente la distance horizontale D du jet : augmente, passe par un maximum pour a =45¯ puis diminue. On constate sur la figure 3 qu'une simulation dÕpasse les 21,69 m. Pour battre le record du monde, il faut avoir (d'aprÒs la figure 3) : a = 41¯ et v0 = 14,0 m.s-1.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|