|
|
||||||
|
||||||
|
|
Données à 25 °C · Masses atomiques (g.mol-1) : Na = 23,0 F = 19,0 · Constante d'acidité : HF/F- : pKa = 3,2 · Produit ionique de l'eau : pKe = 14,0 · Le fluor (Z=9) possède un seul isotope naturel de nombre de masse 19
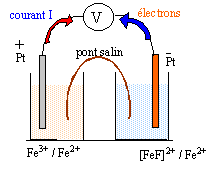
OXYDO-REDUCTION ET COMPLEXATION Données à 25 °C · Produit ionique de l'eau : pKe = 14,0 · Sel de Mohr : FeSO4,(NH4)2SO4, 6 H2O Alun ferrique : Fe2(SO4)3,K2SO4, 4 H2O · Potentiel standard : E°(Fe3+/Fe2+) = 0,77 V · RT/F ln x = 0,06 lg x, en V On se propose de déterminer la constante de dissociation (Kd) du complexe [FeF]2+. Pour cela on réalise les deux demi-piles suivantes : Demi-pile n°1 : une lame de platine plongeant dans une solution aqueuse contenant des ions Fe3+ et Fe2+ à la même concentration, 1,0 10-2 mol.L-1 pour chacune de ces espèces. Demi-pile n°2 : une lame de platine plongeant dans 100 mL de solution aqueuse contenant 1,0 10-3 mol de sel de Mohr et 5 10-4 mol d'alun ferrique à laquelle on ajoute 1,0 10-2 mol d'ions fluorure, sans variation de volume. On suppose que seul l'ion complexe [FeF] 2+ est formé.
A= 19 donc 19-9=10 neutrons. structure électronique de l'atome : 2 électrons sur le niveau n=1 et 7 électrons sur le niveau n=2 (K2L7) donc seconde période et 17 ème colonne : le fluor appartient à la famille des halogènes. HF+H2O = F-+H3O+. Ka = 10-3,2 = 6,3 10-4 = [F-][H3O+] /[HF] solution électriquement neutre ( HO- négligeable en milieu acide) : [F-]=[H3O+] conservation de l'élément fluor : [HF]+[F-] = 0,1 mol/L acide fluorhydrique peu dissocié donc [F-] négligeable devant [HF] : [HF] voisin 0,1 mol/L 6,3 10-4 =[H3O+]2 /0,1 ; [H3O+]2 = 6,3 10-5 ; [H3O+] = 7,93 10-3 mol/L l'approximation "[F-] négligeable devant [HF] " est justifiée. pH= - log(7,93 10-3
)=2,1.
Qté de matière NaF : 2,1 / (23+19)= 0,05 mol [Na+]=[F-]=Qté matière (mol) / volume solution (L) =0,05/0,25 = 0,2 mol/L. solution C : Qté de matière : HF : 0,15*0,1 = 0,015 mol dans 0,25 L ; [HF]=0,015/0,25=0,06 mol/L F- : 0,1*0,2 = 0,02 mol dans 0,25 L ; [F-] = 0,02/0,25 = 0,08 mol/L la solution C contient le couple acide base HF / F- tel que [HF] voisine de [F-]. C est une solution tampon dont le pH varie peu lors de l'ajout modéré d'acide ou de base ; dont le pH ne varie pas par dilution. calcul du pH de la solution C : pH=pKa (HF/F-) + log ([F-] /[HF]) pH=3,2 + log(0,08
/ 0,06)=3,32.
E1 = E°(Fe3+/Fe2+) + 0,06 log ([Fe3+]/[Fe2+]) or [Fe3+]=[Fe2+] donc E1 = E°(Fe3+/Fe2+) =0,77 V. [Fe2+] = Qté de matière (mol) / volume solution (L) =10-3 / 0,1 = 0,01 mol/L l'alun ferrique conduit à : Fe2(SO4)3= 2 Fe3++ 3 SO42-. [Fe3+] =2* 5 10-4 /0,1 = 0,01 mol/L [FeF]2+ :anion fluoroferrate (III) E= E1-E2 = 0,25 V soit E2 =0,77-0.25 = 0,52 V. E2 = E°(Fe3+/Fe2+) + 0,06 log ([Fe3+]/[Fe2+]) avec [Fe2+] =0,01 mol/L 0,52=0,77+0,06 log ([Fe3+]/0,01) ; log ([Fe3+]/0,01) = -0,25/0,06 = -4,16 ([Fe3+]/0,01 = 10-4,16 =6,9 10-5 ; [Fe3+] = 6,9 10-7 mol/L. [FeF]2+ = Fe3+ + F- constante associée Kd= [Fe3+] [F-]/ [[FeF]2+] conservation de l'élément fer (III) : [Fe3+] + [[FeF]2+] = 0,01 mol/L donne :[FeF]2+] = 0,01 -6,9 10-7 = 0,01 mol/L conservation de l'élément fluor : [F-]+[[FeF]2+] = 0,01/0,1 = 0,1 mol/L donne [F-] = 0,1 -[[FeF]2+] = 0,1 -0,01 = 0,09 mol/L Kd= [Fe3+] [F-]/ [[FeF]2+]= 6,9 10-7 *0,09 /0,01 = 6,21 10-6.
|
|||||
|
|