|
|
||||
|
||||
|
|
Description du matériel et principe de la mesure : On introduit une masse connue de matériau dans la bombe calorimétrique (cylindre en acier). On y installe un dispositif de mise ŕ feu (fil au contact du combustible qui sera traversé au moment par un courant fort). On remplit la bombe de dioxygčne (comburant) sous forte pression. On place la bombe en métal trčs conducteur de la chaleur dans un calorimčtre rempli d'eau dont on peut mesurer la température. On connecte le dispositif de mise ŕ feu et on met en route un systčme d'agitation de l'eau. On déclenche la mise ŕ feu et on lit la variation de température de l'eau du calorimčtre. On réalise l'expérience avec un étalon (acide benzoďque) de PCS connu et avec l'échantillon inconnu. Par comparaison, on déduit le Pouvoir Calorifique Supérieur de l'échantillon inconnu. Etalonnage de la bombe avec de l'acide benzoďque : On charge la coupelle de bombe avec une pastille d'acide benzoďque de masse mb = 0,99 g. On mesure L1 = 10 cm de fil que l'on dispose de façon ŕ ce que par effet Joule, il initie la combustion de l'acide benzoďque. La bombe est chargée en dioxygčne pur sous 30 bar. Elle est ensuite placée dans un calorimčtre rempli d'eau. On appelle C la capacité thermique de l'ensemble calorimčtre, eau et accessoires. L'objectif de l'étalonnage est de déterminer C, connaissant le pouvoir calorifique PC de l'acide benzoďque : PCb = 26453 J.g-1 et celui du fil PCf = 9,5 J.cm-1(on compte les pouvoirs calorifiques positivement). Juste avant la mise ŕ feu la température et q1= 21,02 °C. Aprčs la mise ŕ feu la température maximale atteinte est q 2 = 23,63°C. Quand on démonte la bombe, on mesure L2 = 1,8 cm de fil non brűlé.
Détermination du pouvoir calorifique d'une matičre plastique : On refait l'expérience avec cette fois-ci un échantillon de plastique de masse m = 1,02 g et de pouvoir calorifique PC inconnu. Le calorimčtre et son contenu sont inchangés. On mesure : L1 = 10 cm ; L2 = 2,1 cm ; q1 = 20,38 °C et q2 = 22,96 °C.
Qunatité de chaleur produite par la combustion de l'acide et de le fil : pour l'acide : masse (g) * pouvoir calorifique (J g-1) = mb PCb. pour le fil : longueur (cm) * pouvoir calorifique ( J cm-1)= ( L1-L2) PCf. Q= mb PCb+ ( L1-L2) PCf. La chaleur dégagée par la combustion sert ŕ élever la température du calorimčtre et accessoires. CDq = mb PCb+ ( L1-L2) PCf. C= [mb PCb+ ( L1-L2) PCf.]/Dq . C=[ 0,99*26453+(10-1,8)*9,5]/ (23,63-21,02) = [ 26188,5+
77,9]/ 2,61 = 10 063 J K-1.
m PC = CDq- (L1-L2) PCf. PC= [CDq- (L1-L2) PCf]/m. PC= [10063*(22,96-20,38)-(10-2,1)*9,5]/1,02 =(25962-75)/1,02 = 25380 J g-1.
|
|||
|
Conditionneur : La mesure de la température dans le calorimčtre se fait ŕ l'aide d'un capteur dont la résistance R est fonction affine de la température : R = a.q + b avec a et b constantes. Ce capteur est placé dans un pont de Wheatstone dont on mesure la tension de déséquilibre u. Cette tension est ensuite amplifiée et saisie par un ordinateur qui suit son évolution au cours du temps et détermine automatiquement Dq avec si nécessaire des corrections. 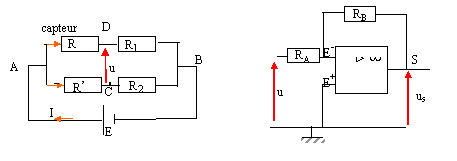
R1=R2=15 kW ; E=12V; R' réglable; RA=2 kW ; RB=10 kW.
corrigé Quand le pont est équilibré : u=0 i1 : intensité dans la branche ADC ; i2 intensité dans la branche ACB) uAD=UAC soit Rref i1= R'i2 ou i1/ i2 = R'/Rref uDB=UCB soit R1 i1= R2i2 ou i1/ i2 = R2/R1 R'/Rref = R2/R1 soit R' = Rref R2/R1. R'= 12,65 kW. Quand le pont est déséquilibré : u différent de zéro. E= uAD+ uDB =( Rref + DR +R1)i1 donne i1 = E/(Rref + DR +R1) E= uAC+ uCB =( R' +R2)i2 donne i2 = E/( R' +R2) E= uAC+ uCD + uDC ; E= R'i2- u + R1i1 E= R' E /( R' +R2) - u + R1 E/(Rref + DR +R1) u= E[R'/( R' +R2)+R1/(Rref + DR +R1)-1] réduire au męme dénominateur : ( R' +R2)(Rref + DR +R1) u= E( R1R' + R2Rref -R2 DR) / [( R' +R2)(Rref + DR +R1)] on peut négliger DR devant R1, R2 et Rref. u= E( R1R' - R2Rref -R2 DR) / [( R' +R2)(Rref +R1)] de plus R1R' = R2Rref ( pont ŕ l'équilibre) u= -R2E / [( R' +R2)(Rref +R1)] DR = k DR avec k = -R2E / [( R' +R2)(Rref +R1)] or R= a.q + b donne D R= a D q . u= k a D q ; u est proportionnelle ŕ D q . montage amplificateur inverseur : E+ et E- masse virtuelle : donc u= RAi et uS= -RB i soit uS /u= -RB/RA ; uS= -RB/RA u or u = k a D q donc uS = - k a RB/RA D q. uS est proportionnelle ŕ D q. Application numérique : k = -R2E / [( R' +R2)(Rref +R1)] = - 15 103*12/(12,65 103 + 15 103)˛= -180 10-3 /763,4 = -2,36 10-4. q-qref= 23,63 -0 = 23,63 °C ; a = 100 W °C-1 ; RA=2 kW ; RB=10 kW. uS = -(-2,36 10-4)*100*10/2*23,63 = 2,8 V. |
||||
|
|