|
Le degré
alcoolique d'un vin est le pourcentage volumique d'alcool mesuré à une
température de 20°C.
Pour déterminer
le degré alcoolique d'un vin, il faut d'abord isoler l'alcool des
autres composés du vin (acides, matières minérales, sucres, esters,...)
en réalisant une distillation. Cette méthode de séparation ne permet
pas d'obtenir de l'éthanol pur mais un mélange eau - éthanol dont les
proportions sont constantes. Il est donc nécessaire d'ajouter de l'eau
au vin pour être sûr de recueillir pratiquement tout l'éthanol contenu
dans celui-ci.
La solution
aqueuse d'éthanol est ensuite ajustée à 100 mL avec de l'eau distillée,
pour simplifier les calculs.
Puis l'alcool est
oxydé quantitativement en acide acétique (éthanoïque) par un excès de
dichromate de potassium.
L'oxydant
excédentaire est ensuite dosé par une solution de sel de Mohr [FeSO4,(NH4)2SO4].
Ce dosage est appelé dosage indirect (ou en retour).
- Extraction
de l'éhtanol
Pour
ce dosage, on prélève 10,0 mL de vin étiqueté 12 degrés auxquels on
ajoute environ 50 mL d'eau. On distille ce mélange et on recueille un
volume de 42 mL de distillât (noté S1). On considère qu'il
contient alors tout l'éthanol du vin.
- Compléter sur la figure 1 de l'annexe ( à remettre avec la copie ) le
nom des éléments du montage désignés par les flèches et préciser le
sens de circulation de l'eau.
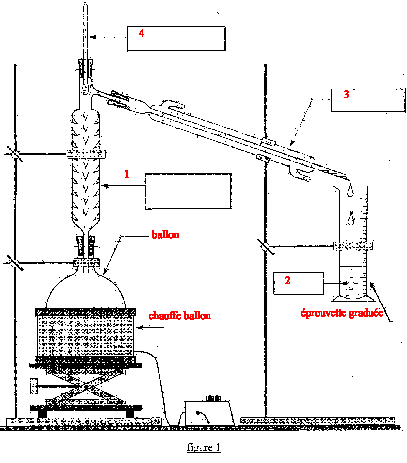
- Préparation
de la solution à titrer
On
complète S1 à 100,0 mL avec de l'eau distillée. On obtient
ainsi une solution notée S2. S2 contient donc
l'éthanol présent dans les 10 mL de vin prélevé, dilué 10 fois.
- Réaction
entre éthanol et dichromate de potassium
Dans un erlenmeyer, on mélange V0 = 10,0 mL de solution S2,
V1 = 20,0 mL d'une solution de dichromate de potassium (2K+(aq)
+ Cr2O72-(aq)) de concentration C1
= 1,00.10-1 mol.L-1 et environ 10 mL d'acide
sulfurique concentré. On bouche l'erlenmeyer et on laisse réagir
pendant environ 30 minutes. On obtient alors une solution verdâtre
appelée S3. L'équation de la réaction entre l'ion dichromate
et l'éthanol est :
2 Cr2O72- + 16 H3O+
+ 3 CH3-CH2OH = 4 Cr3++ 27 H2O
+ 3 CH3-COOH
- Justifier la couleur de la solution S3.
- Pourquoi doit-on boucher l'erlenmeyer ?
- En vous aidant éventuellement d'un tableau d'avancement, montrer que
la relation entre la quantité n0 d'éthanol oxydé et la
quantité n(Cr2O72- ) restant d'ions
dichromate restant après cette oxydation est : n(Cr2O72-
) restant = C1V1 - 2/3 n0.
- Dosage de
l'excès de dichromate de potassium
On dose alors les ions dichromate en excès avec une solution de sel de
Mohr de concentration C2 = 5,00.10-1 mol.L-1.
Le volume de solution de sel de Mohr nécessaire pour atteindre
l'équivalence (repérée à l'aide d'un indicateur de fin de réaction) est
V2 = 7,6 mL. L'équation de la réaction entre les ions fer II
et les ions dichromate est :
Cr2O72- + 14 H3O+
+ 6 Fe2+ = 2 Cr3++ 21 H2O + 6 Fe3
+
- En vous aidant éventuellement d'un tableau
d'avancement, montrer que : n0= 3/2 C1V1
- 1/4 C2V2.
- Faire l'application numérique.
- Exploitation :
- Déterminer la quantité de matière d'éthanol contenue dans 100 mL de
vin.
- Déterminer le degré alcoolique du vin étudié. Masse volumique éthanol
r = 0,78 g/ mL
- L'étiquette de la bouteille indique que le vin a un degré alcoolique
d = 12°. Cette indication est le résultat d'un contrôle (alcoométrie
directe) réalisé à l'aide d'un densimètre (aussi appelé alcoomètre)
directement gradué en degré alcoolique.
La densité (donc le degré alcoolique) varie avec la température et les
densimètres utilisés sont étalonnés pour 20°C. Pour comparer le
résultat du dosage précédent réalisé à 21 °C et l'indication portée sur
l'étiquette, il faut apporter une correction au degré lu sur
l'étiquette (voir tableau ci-dessous). Quelle correction doit-on
apporter à la valeur d = 12° inscrite sur l'étiquette ?
- Le résultat du dosage est-il alors en accord avec la valeur corrigée
de ce degré ?
couples oxydant réducteur mis en jeu : acide
éthanoïque ( incolore) / alcool éthylique (incolore) ;
ion dichromate (orange) / ion chrome III ( vert) ; ion fer III
(rouille) / ion fer II ( verdâtre)
|
t °C
|
degré alcoolique à t°C sur l'alcoomètre
|
|
10
|
11
|
12
|
13
|
14
|
|
18
|
+0,34
|
+0,36
|
+0,39
|
+0,42
|
+0,45
|
|
19
|
+0,17
|
+0,18
|
+0,20
|
+0,21
|
+0,23
|
|
21
|
-0,17
|
-0,18
|
-0,19
|
-0,20
|
-0,21
|
|
22
|
-0,37
|
-0,40
|
-0,42
|
-0,44
|
-0,46
|
exemple : on lit sur l'alcoomètre 14 % à 18°C ; à 20°C : 14 + 0,45 =
14,45 degrés
corrigé
La solution S3 a une couleur verte due de la
présence des ions Cr3+ formés au cours de la transformation.
il faut boucher l'erlenmeyer car
:
L'éthanol est un liquide volatil ; les vapeurs d'éthanol sont
facilement inflammables.
Les ions dichromate sont cancérigènes, il vaut mieux éviter
tout contact.
L'acide éthanoïque formé irrite les voies respiratoires.
quantité de
matière d'ion dichromate initiale : volume solution (L) * concentration
Cr2O72- (mol/L) =0,02*0,1 = 2 10-3
mol
|
avancement (mol)
|
2 Cr2O72-
|
+ 16 H3O+
|
+ 3 CH3-CH2OH
|
= 4 Cr3++
|
+27 H2O
|
+ 3 CH3-COOH
|
|
initial
|
0
|
n(Cr2O72-
)
= C1V1
=2 10-3 mol
|
excès
|
n0
|
0
|
excès
( solvant)
|
0
|
|
en cours
|
x
|
C1V1 -2x
|
n0 -3x
|
4x
|
3x
|
|
fin
|
xmax
|
C1V1 -2xmax
|
n0 -3x max=0
|
4xmax
|
3xmax
|
n0 -3x max=0 donc xmax =n0/3
n(Cr2O72-
) restant = C1V1 -2xmax=C1V1 -2n0/3.
Cr2O72- + 14 H3O+
+ 6 Fe2+ = 2 Cr3++ 21 H2O + 6 Fe3
+
|
avancement (mol)
|
Cr2O72-
|
+ 14 H3O+
|
+ 6 Fe2+
ajouté
|
= 2 Cr3++
|
+21 H2O
|
+6 Fe3
+
|
|
initial
|
0
|
n(Cr2O72-
)restant
|
excès
|
0
|
0
|
excès
( solvant)
|
0
|
|
en cours
|
x
|
n(Cr2O72-
)restant -x
|
6x
|
2x
|
6x
|
|
équivalence
|
xéqui
|
n(Cr2O72-
)restant -x équi
=0
|
6x équi =C2V2
|
2xéqui
|
6xéqui
|
6x équi =C2V2 donc xéqui
=C2V2/6
n(Cr2O72-
) restant = C2V2/6 = C1V1 -2n0/3.
2/3n0
= C1V1 -C2V2/6 ; n0 =3/2 C1V1 -1/4C2V2
n0 =
1,5 *0,02*0,1 -0,25
*0,5*7,6 10-3 = 2,05 10-3 mol éthanol dans 10 mL
de S2.
soit 2,05 10-2
mol éthanol dans 100 mL de S2.
soit en tenant
compte de la dilution 2,05 10-1 mol éthanol dans 100 mL de
vin.
Le degré
alcoolique d'un vin est le pourcentage volumique d'alcool mesuré à une
température de 20°C.
masse molaire
éthanol = 46 g/mol ; masse alcool dans 100 mL de vin : 0,205*46 = 9,43 g
masse volumique
éthanol r = 0,78 g/ mL ; volume alcool
dans 100 mL de vin : 9,43 / 0,78 = 12,09 mL
soit 12 degrés
valeur corrigée
du degré : à 21°C, on doit soustraire 0,19 au degré lu sur l'étiquette.
12 - 0,19 = 11,81
valeur obtenue
par titrage = 12,09
Ces deux valeurs
sont très proches, écart (12,09-11,81) / 12 =0,023 soit 2,3 %)
Le résultat du
dosage est en accord avec la valeur corrigée du degré.
|

