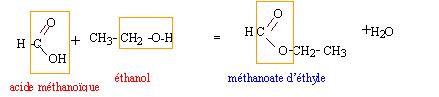|
|
|||||||||||||||||||||
|
|||||||||||||||||||||
|
|
On prépare, en présence de catalyseur, un ester de formule H-COO-C2H5. On chauffe ŕ reflux pendant une heure un mélange initial composé de 0,30 mol d'acide carboxylique, de 0,30 mol d'alcool et de quelques gouttes d'acide sulfurique. Le mélange final contient 0,10 mol d'acide carboxylique. Températures d'ébullition : alcool : 79°C ; acide : 101°C ; ester : 54°C.
Dans l'état final le systčme chimique contient, le catalyseur, encore de l'alcool et de l'acide, mais aussi de l'eau et l'ester.
taux d'avancement final t = xfin /xmax=0,2 / 0,3 = 0,67 ( 67 %) L'acide sulfurique, le catalyseur permet d'atteindre plus rapidement l'équilibre chimique, mais ne modifie pas la composition de cet équilibre. Le taux d'avancement final reste donc inchangé. Le chauffage ŕ reflux permet de travailler ŕ température modérée ( l'équilibre est plus rapidement atteint ), sans perte de matičre par évaporation. Ce type de chauffage est justifié lorsque la réaction est assez lente. Pour obtenir, ŕ partir de 0,30 mol d'acide, 0,30 mol d'ester, il faut éliminer le constituant le plus volatil ( l'ester dans ce cas) au fur et ŕ mesure qu'il se forme par distillation.
|
||||||||||||||||||||
|
|