|
Donneurs,
accepteurs d'ťlectrons.
Donnťes
: ťlectronťgativitť H : 2,2 ; Li : 1,0 ; C : 2,5 ; N : 3,0 ; O : 3,4 ;
Cl : 3,2.
A)
L'ion hydrogŤne H+ est un site accepteur de
doublet d'ťlectrons.
Vrai.
B)
Un alcŤne comporte un site donneur de doublet d'ťlectrons. Vrai.
La double
liaison carbone-carbone.
C)
Une liaison carbone-oxygŤne est plus polarisťe qu'une liaison
carbone-chlore.
Vrai.
L'atome
d'oxygŤne est plus ťlectronťgatif que l'atome de chlore.
D)
La liaison carbone-lithium est polarisťe. Le carbone est alors un site
accepteur de doublet d'ťlectrons.
Faux.
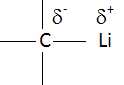
Acide
base.
A) Lorsqu'on dilue une solution acide, le pH augmente. Vrai.
[H3O+] diminue par dilution ; pH =
-log [H3O+] croÓt.
B) L'acide
mťthanoÔque est un acide faible dans l'eau. Vrai.
C) L'ammoniac NH3 est une base au sens de
BrŲnsted. L'ammoniac est la base conjuguťe de l'ion ammonium NH2-.
Faux.
L'ammoniac
est la base conjuguťe de l'ion ammonium NH4+.
D) Une solution tampon est une solution de pH=7.
Faux.
Une solution
tampon modŤre les variations de pH suite ŗ l'ajout modťrť d'acide ou de
base forte, suite ŗ une dilution modťrťe.
Acide
base.
On considŤre la rťaction suivante : C6H5-COO-aq
+ H2O(l) = C6H5-COOH
aq+ HO-aq.
Donnťes
: ŗ 25 įC,le pKa du couple acide / base qui rťagit avec l'eau vaut 4,2.
A l'ťquilibre [H3O+]ťq
= 10-6 mol/L.
A) C'est la forme acide du couple considťrť qui prťdomine. Faux.
pKa
= 4,2 ; pH = 6 ; ŗ pH > pKa, la forme
base conjuguťe C6H5-COO-aq prťdomine.
B) L'ion C6H5-COO-aq
est un acide au sens de BrŲnted. Faux.
L'ion C6H5-COO-aq est une base au sens de
BrŲnted.
C) Au cours de cette rťaction, le pH de la solution augmente. Vrai.
L'un des
produits est l'ion hydroxyde ; [ HO-aq] augmente et le pH croÓt.
D)
[C6H5-COO-aq]ťq
/ [C6H5-COOHaq]ťq=
101,8. Vrai.
pH = pKa +
log( [C6H5-COO-aq]ťq / [C6H5-COOHaq]ťq) ; log( [C6H5-COO-aq]ťq / [C6H5-COOHaq]ťq) =6-4,2 = 1,8.
Dosage.
A) Un dosage par ťtalonnage met en jeu un rťactif titrant et un rťactif
titrť. Faux.
Ce dosage
met en oeuvre une courbe d'ťtalonnage.
B) Un dosage par titrage direct met en jeu une rťaction chimique rapide
et totale. Vrai.
C) Un titrage conductimťtrique permet de trouver la concentration de
l'espŤce dissoute en solution par application de la loi de Kollrausch
stipulant que la conductivitť est proportionnelle ŗ la concentration de
l'espŤce. Vrai.
D). Pour rťaliser le titrage d'une solution incolore et diluťe d'acide
ťthanoÔque, on peut procťder par ťtalonnage avec un conductimŤtre. Faux.
La
concentration de l'ion ťthanoate, base conjuguťe de l'acide ťthanoÔque,
varie par dilution, l'acide ťthanoÔque ťtant faible. La conductivitť de
la solution dťpend de la concentration des ions. Par contre on
peut dťterminer le volume ťquivalent en effectuant
un suivi conductimťtrique.
Titrage
pH-mťtrique.
On considŤre la rťaction de titrage d'une solution d'ťthanoate de
sodium de volume V = 100 mL par une solution d'acide chlorhydrique de
concentration ca = 0,20 mol/L. A l'ťquivalence
on a versť 9,0 mL d'acide chlorhydrique.
A) La rťaction support du titrage est CH3-COO-aq
+ HO-aq --> CH3COOH
aq + H2O(l). Faux.
CH3-COO-aq + H3O+aq --> CH3COOH aq + H2O(l).
B) A l'ťquivalence, les rťactifs ont ťtť introduits en proportions
stoechiomťtriques, le pH ťquivalent est donc ťgal ŗ 7. Faux.
L'acide
faible CH3COOH aq est prťsent ŗ
l'ťquivalence, le pH ŗ l'ťquivalence est infťrieur ŗ 7.
C) La concentration de la solution d'ťthanoate de sodium est c =1,8 10-2
mol/L. Vrai.
A
l'ťquivalence caVťq = cV ; c =caVťq /V = 0,20 *9,0 / 100
= 1,8 10-2 mol/L.
D) Si on continue de verser de l'acide chlorhydrique aprŤs
l'ťquivalence, la solution devient de plus en plus acide et son pH va
se rapprocher de 0,7. Faux.
Il faut
tenir compte de la dilution rťsultant de l'ajout de la solution d'acide
chlorhydrique en excŤs.
|