|
|
La vitamine A (
molťcule 1) est indispensable ŗ la vie animale puisqu'elle intervient
dans de nombreux processus biologiques, dont celui de la vision.
L'homme ťtant incapable de la synthťtiser, son apport se fait par
l'alimentation, principalement sous forme d'esters, dont le principal
est le palmitate de rťtinyle, contenus dans le lait, les laitages, le
jaune d'oeuf, le foie de poisson.
Une fois assimilť, le palmitate de rťtinyle est stockť dans le foie,
avant d'Ítre hydrolysť pour donner de l'acide palmitique ( molťcule 2)
et de la vitamine A qui sera transportťe dans le sang.
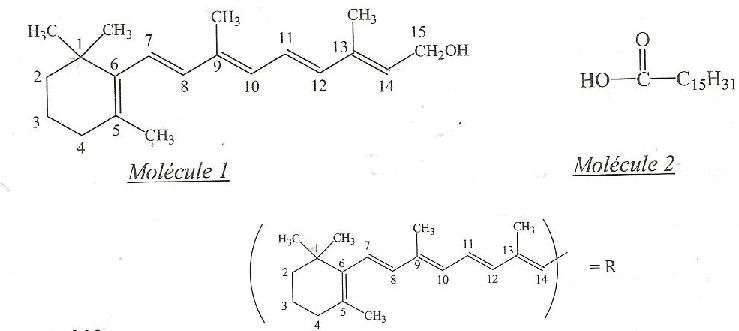
La fonction
caractťristique de la vitamine A est une fonction :
A) Acide carboxylique ; B) Alcool ; C) Aldehyde ; E) Anhydride d'acide
; E) Ester.
R-CH2OH : alcool primaire.
La molťcule 3 est issue de la rťaction entre les molťcules 1 et 2.
A) La formule de la molťcule 3 est : 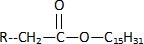 Faux. Faux.
B) La formule de la molťcule 3 est :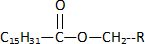 Vrai. Vrai.
C) L'ťquation bilan de la rťaction d'hydrolyse est :
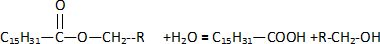 Vrai. Vrai.
D) L'ťquation bilan de la rťaction d'hydrolyse
est :
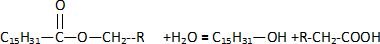 Faux. Faux.
Concernant l'hydrolyse de la molťcule 3 :
A) Il s'agit d'une rťaction totale. Faux.
L'hydrolyse est limitťe
par la rťaction inverse, l'estťrification.
B) Il s'agit d'une rťaction rapide. Faux.
C) Son ťquilibre peut Ítre dťplacť vers la formation du rťtinol par
ťlimination d'eau. Faux.
Par ťlimination d'eau
l'ťquilibre est dťplacť dans le sens indirect.
D) Sa vitesse peut Ítre augmentťe en milieu acide. Vrai.
E) Sa vitesse peut Ítre augmentťe en augmantant la tempťrature. Vrai.
|
.
|
Une fois dans
la circulation sanguine, la vitamine A est transportťe vers les
diffťrents organes, dont les yeux, oý elle s'accumule dans les
b‚tonnets, cellules tapissant la rťtine. Lŗ, sous l'action d'une enzyme
appelťe rťtinol dťshydrogťnase, elle est transformťe par le NAD+
en molťcule 4, selon l'ťquation :
R-CH2OH + NAD+ ---> R-CHO ( molťcule 4 ) +
NADH + H+.
Nommer
le groupe fonctionnel de la molťcule 4. Groupe aldehyde.
Ecrire
la demi-ťquation de transformation de la molťcule 1 en molťcule 4.
R-CH2OH =
R-CHO + 2H+ + 2e-.
Quelle
est, de la molťcule 1 ou de la molťcule 4, l'espŤce oxydante ?
Couple oxydant / rťducteur : R-CHO / R-CH2OH
; R-CHO est la forme oxydante.
Ecrire
la demi-ťquation d'oxydo-rťduction donnant NADH ŗ partir de NAD+.
NAD+ + H+
+ 2e- = NADH.
S'agit-il
d'une oxydation ou d'une rťduction ?
NAD+
gagne des ťlectrons, c'est un oxydant qui se rťduit.
L'humeur aqueuse, liquide biologique de l'intťrieur de l'oeil prťsente
une concentration non nťgligeable en lactate, produit de la rťaction
ci-dessous catalysťe par la lactate dťshydrogťnase (LDH) au niveau du
cristallin.
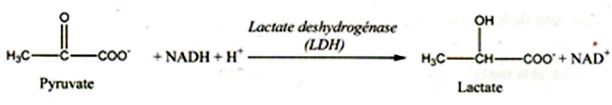
Pour suivre l'ťvolution de la concentration en NADH, on
effectue in vitro un dosage de cette rťaction par spectrophotomťtrie,
dans les conditions de validitť de la loi de Beer-Lambert. NADH et NAD+
possŤdent respectivement le spectre d'absorption suivant :
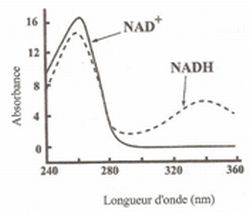
A quelle longueur
d'onde faut-il se placer pour effectuer le suivi cinťtique de cette
rťaction par spectrophotomťtrie ? Justifier.
Il faut qu'une seule espŤce prťsente un maximum d'absorption ŗ la
longueur d'onde choisie. Vers 340 nm, ( domaine U.V ) seule NADH
prťsente un maximum d'absorption.
D'aprŤs
le spectre ci-dessus quelle est la couleur de la solution ? Justifier.
Si les deux espŤces ne prťsentent pas de maximum d'absorption dans le
domaine visible [ 400 nm - 800 nm ], la solution est incolore.
L'acide oxamique est un inhibiteur de la LDH.
Expliquer
briŤvement en quoi la prťsence d'acide oxamique impacte le
fonctionnement des cellules des b‚tonnets de la rťtine.
NADH ne peut plus Ítre rťduit en NAD+ et en absence de ce
dernier, R-CH2OH ne peut Ítre oxydť en R-CHO.
A propos de la mťthode de dosage utilisť :
A) Ce mode opťratoire nťcessite la construction prťalable d'une droite
d'ťtalonnage. Vrai.
B) Cette mťthode de dosage est non destructive. Vrai.
C) On ne peut pas effectuer une mesure ŗ 260 nm ŗ cause de la propriťtť
d'additivitť des absorbances. Vrai.
D) L'absorbance mesurťe est inversement proportionnelle ŗ la
concentration de la solution. Faux.
L'absorbance et la
concentration molaire sont proportionnelles.
E) Pour Ítre dans le domaine de validitť de la loi de Beer-Lambert, il
faut que le spectrophotomŤtre ťmette de la lumiŤre blanche. Faux.
LumiŤre blanche et/ ou
lumiŤre UV pour les mesures quantitatives.
En utilisant une cuve de longueur L=1,0 cm, les mesures d'absorbances
sur 4 solutions de NADH, H+ ont permis d'obtenir les
rťsultats suivants :
[NADH,H+]
(mmol/L)
|
6,0
|
4,0
|
2,0
|
0,5
|
A
|
37,32
|
24,88
|
12,44
|
3,11
|
| A
/ ([NADH,H+] L) ( mmol-1 L cm-1 ) |
37,32
/ (6,0 *1,0) = 6,2
|
24,88
/4 =6,2
|
12,44
/ 2 =6,2
|
6,2
|
On en dťduit que le coefficient d'extinction molaire e de NADH, H+ vaut :
3,1 mol-1L cm-1 ; 6,2 mmol-1L cm-1
; 3,1 mol-1L cm ; 6,2 mol-1L cm-1 ;
6,2 103 mol-1L cm-1 ;
e = 6,2 mmol-1
L cm-1 = 6,2 103 mol-1L cm-1.
A) Le coefficient d'extinction molaire dťpend de la longueur d'onde de
la lumiŤre utilisťe. Vrai.
B) Le coefficient d'extinction molaire est indťpendant de la nature de
la solution. Faux.
C) La loi de Beer n'est pas valide si on utilise de la lumiŤre visible.
Faux.
D) L'absorbance s'exprime en mol-1L cm-1. Faux.
L'absorbance est sans
unitť.
E) La loi de Beer fait intervenir le volume de la cuve traversťe par la
lumiŤre. Faux.
Cette loi fait intervenir
la longueur de la cuve traversťe par la lumiŤre.
|
On mesure la
concentration en acide lactique ( M = 90,0 g/mol) sanguin ( acide
conjugfuť ion lactate ), d'un athlŤte aprŤs une course de 800 m. On
prťlŤve V = 1,0 mL de sang et on en extrait la totalitť de l'acide
lactique. Cet acide est introduit dans une fuiole jaugťe de 50,0 mL
contenant un peu d'eau distillťe. On agite jusqu'ŗ dissolution
complŤte. On complŤte la fiole jaugťe avec de l'eau distillťe jusqu'au
trait de jauge. On appelle S la solution obtenue.
On rťalise le dosage du volume VA = 50,0 mL de la solution S
par une solution aqueuse de soude de concentration molaire cB
= 1,00 10-3 mol/L. L'ťquivalence est atteinte pour un volume
de solution de soude VE = 20,0 mL
La constante d'ťquilibre de la rťaction entre les ions hydroxydes et
'acide lactique vaut K = 1,0 1010 ŗ 25įC.
Que
peut-on dťduire de la valeur de K.
K est trŤs grande, la rťaction est quantitative, totale.
Donner
l'ťquation de la rťaction de titrage en utilisant les formules
semi-dťveloppťes.
HO-aq + CH3-CH(OH)-COOHaq ---> CH3-CH(OH)-COO-aq
+ H2O.
Etablir
l'expression du Ka du couple ( acide lactique / ion lactate) en
fonction de K puis calculer sa valeur.
On note AH l'acide lactique et A- l'ion lactate. Ka
= [A-][H3O+] / [AH] soit [A-] /[AH] = Ka / [H3O+].
K = [A-]/ ([AH][HO-aq]) = Ka / ([H3O+][HO-aq] = Ka /
10-14 ; Ka = 10-14 K =
10-4.
Le pKa du couple ( acide
lactique / ion lactate) vaut : 2 ; 3 ; 4 ; 6 ; 8.
pKa = - log (Ka) = - log 10-4 = 4.
La
concentration molaire en acide lactique dans la solution S vaut :
1,00 10-4 mol/L ; 2,00 10-4 mol/L ; 2,00 10-3 mol/L ; 4,00 10-3 mol/L ; aucune
rťponse juste.
A l'ťquivalence VA[AH] = cB VE ; [AH]
= cB VE / VA = 1,00 10-3
*20 / 50 =4,00 10-4 mol/L.
La
concentration massique en acide lactique dans le prťlevement sanguin
vaut :
9,0 g/L ; 3,6 g/L ; 3,6 mol/L ; 1,8 g/L ; 0,90 g/L.
Dans 50 mL de solution S il y a : VA[AH] = 0,050 *4,00 10-4
= 2,0 10-5 mol d'acide lactique.
Concentration de l'acide lactique dans le sang : c = 2,0 10-5
/ 10-3 =2,0 10-2 mol/L.
c M = 2,0 10-2
*90 = 1,8 g/L.
|
|