|
|
Expliquer le
principe gťnťral de la chromatographie.
La chromatographie est
une mťthode de sťparation et d'identification des constituants d'un
mťlange.
La chromatographie est basťe sur
la diffťrence de solubilitť d'une substance dans deux phases non
miscibles : la phase stationnaire liťe au support et la phase mobile ou
solvant.
Plus une substance est soluble dans la phase mobile, plus elle est
entraÓnťe par cette phase; inversement, une substance peu soluble dans
la phase mobile migre peu.
Un fluide appelť phase mobile parcourt un tube appelť colonne. Cette
colonne peut contenir des "granulťs" poreux (colonne remplie) ou Ítre
recouverte ŗ l'intťrieur d'un film mince (colonne capillaire). Dans les
deux cas, la colonne est appelťe phase stationnaire.
A l'instant initial, le mťlange ŗ sťparer est injectť ŗ l'entrťe de la
colonne oý il se dilue dans la phase mobile qui l'entraÓne ŗ travers la
colonne. Si la phase stationnaire a ťtť bien choisie, les constituants
du mťlange, appelťs gťnťralement les solutťs, sont inťgalement retenus
lors de la traversťe de la colonne.
De ce phťnomŤne appelť rťtention
il rťsulte que les constituants du mťlange injectť se dťplacent tous
moins vite que la phase mobile et que leurs vitesses de dťplacement
sont diffťrentes. Ils sont ainsi ťluťs de la colonne les uns aprŤs les
autres et donc sťparťs.
Un dťtecteur placť ŗ la sortie de la colonne couplť ŗ un enregistreur
permet d'obtenir un tracť appelť chromatogramme. En effet, il dirige
sur un enregistreur un signal constant appelť ligne de base en prťsence
du fluide porteur seul ; au passage de chaque solutť sťparť il conduit
dans le temps ŗ l'enregistrement d'un pic.
Dans des conditions chromatographiques donnťes, le "temps de rťtention"
(temps au bout duquel un composť est ťluť de la colonne et dťtectť),
caractťrise qualitativement une substance. L'amplitude de ces pics, ou
encore l'aire limitťe par ces pics et la prolongation de la ligne de
base permet de mesurer la concentration de chaque solutť dans le
mťlange injectť.
C'est en jouant sur la nature de
l'ťluant (et dans une moindre mesure sur la nature du support) que l'on
parvient ŗ sťparer les constituants d'un mťlange.
Donner le nom de
chaque numťro correspondant ŗ un des constituants du chromatographe en
phase gazeuse.
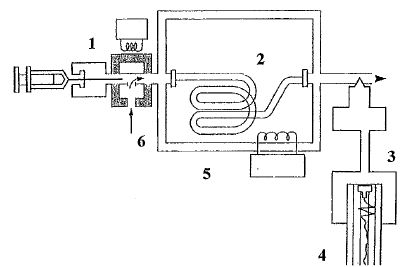
1 : injecteur ; 2 : colonne ; 3 : dťtecteur ; 4 : intťgrateur ou
ordinateur ; 5 : thermostat de colonne ; 6 : gaz vecteur.
Quels
sont les principaux gaz vecteurs utilisables en chromatographie en
phase gazeuxe ?
HydrogŤne, hťlium, azote.
Quelles
sont les prťcautions ŗ prendre vis-ŗ-vis de ces gaz pour ne pas
endommager la colonne ?
Le gaz vecteur doit Ítre pur, inerte (il ne doit pas rťagir avec les
constituants de l'ťchantillon ŗ sťparer) et non miscible possible avec
la phase stationnaire.
|
.
|
Qu'est-ce qu'une
injection en mode "split" ? Quelle est la diffťrence avec une injection
en mode "splitless" ?
Les injecteurs peuvent fonctionner suivant
deux modes, avec ou sans division (encore appelťs split ou splitless).
En
mode split, le gaz vecteur pťnŤtre avec un grand dťbit dans la chambre
de vaporisation ; une vanne de fuite sťpare le courant gazeux en deux
parties : seule la plus petite pťnťtre dans la colonne.
Ce mode est utilisť dans les colonnes capillaires ŗ faible dťbit. Le
mode splitless est utilisť dans le cas d'ťchantillons trŤs diluťs.
Citer
deux dťtecteurs couplťs ŗ la chromatographie en phase gazeuse.
Expliquer briŤvement leur principe de fonctionnement.
Le
spectromŤtre de masse en aval de la colonne capture, ionise,
accťlťre, dťvie et enfin dťtecter les espŤces ionisťes. Le spectromŤtre
de masse casse chaque molťcule en fragments ionisťs et dťtecte ces
fragments en fonction de leur rapport masse sur charge.
Les 4 parties principales d'un
spectromŤtre de masse sont :
Source d'ion : production d'ions en phase gazeuse.
Analyseur m / z : sťparation des ions produits en fonction du rapport
masse / charge ( m / z).
Dťtection : conversion d'un courant ionique en courant ťlectrique.
Traitement du signal : reprťsentation des donnťes sous forme d'un
spectre de masse.
Ces deux appareils utilisťs ensemble, permettent l'identification
d'une substance sans aucune ambiguitť.
Dťtecteur UV-visible : soumis ŗ l'influence
d'un rayonnement lumineux, certains groupements fonctionnels d'une
molťcule peuvent Ítre le siŤge d'une excitation ťlectronique c'est ŗ
dire une absorption d'ťnergie, spťcifiques du groupement fonctionnel.
Les rťsultats des analyses ont permis d'identifier de la propanone dans
le liquide faisant l'objet du scellť.
A quelle famille
chimique appartient la propanone ? Quel est son nom usuel ? Donner le
schťma de Lewis de cette molťcule.
La propanone ou acťtone appartient ŗ la famille des cťtones. 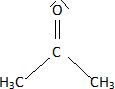
La fiche de sťcuritť de la propanone comporte deux pictogrammes de
danger.

Quelle est la
signification de chaque pictogramme ?
Inflammable pour le
premier et pour le second produits pouvant, selon le cas, entraÓner les
effets suivants : empoisonnement, irritation, allergies cutanťes,
somnolence, vertige.
Les rťsultats des analyses ont permis d'identifier du gasoil dans le
liquide faisant l'objet du scellť nį2. Le gasoil est constituť de
nombreux alcanes linťaire, avec notamment les composťs phytane et
pristane.
Donner
la formule gťnťrale d'un alcane linťaire.
CnH2n+2 avec n entier supťrieur ou ťgal ŗ 1.
Les alcanes peuvent Ítre synthťtisťs ŗ partir d'alcŤnes.
Quel
est le type de rťaction ? Donner un exemple de synthŤse d'un alcane.
Addition de dihydrogŤne en prťsence d'un catalyseur : Nickel de Ranaey
ou de Sabatier.
CnH2n + H2 ---> CnH2n+2.
Le nom officiel du pristane est 2, 6, 10,14-tťtramťthyl-pentadťcane.
Donner
la formule brute du pristane et ťcrire sa formule topologique.
C19H40. 
Quelle
diffťrence y-a-t-il entre le gasoil et le fuel domestique ? Comment
peut-on les diffťrencier chimiquement ?
Chimiquement,
le fioul et le gazole diffŤrent par leur teneur en cťtane.
Le fioul domestique contient un colorant rose-rouge. Le gasoil,
carburant automobile est clair.
|
|
Des tests bandelettes permettent de
mettre en ťvidence de grandes quantitťs d'ion nitrate et potassium.
Citer
une technique analytique qui permettrait de confirmer ce rťsultat ?
Expliquer le principe de cette technique.
Un excŤs connu d'ions Fe2+ rťagit avec les ions nitrates
contenus dans une solution prťparťe ŗ partir d'un engrais liquide. Les
ions Fe2+ qui n'ont pas rťagi sont titrťs par une solution
de dichromate de potassium.
Le photomŤtre de flamme est un appareil qui permet de doser des
solutions d’ions alcalins : la solution d’ions est pulvťrisťe avec un
mťlange d’air et de carburant (propane). La flamme obtenue est colorťe
par l’ion ŗ doser : violet p‚le pour le potassium. Un filtre
isole la longueur d’onde caractťristique de l’ion ťtudiť. Un dispositif
de mesure ( cellule photoťlectrique, amplificateur,
milliampŤremŤtre), donne une valeur proportionnelle au flux lumineux
reÁu. Ce dernier est proportionnel ŗ la concentration de la solution
ionique.
Le
potassium est l'ťlťment chimique de numťro atomique Z = 19.
Donner
la structure ťlectronique de l'atome de potassium dans son ťtat
fondamental.
1s2 2s2 2p6 3s2 3p6
4s1.
Localiser
le potassium dans la clasification pťriodique en justifiant.
La derniŤre couche lectronique compte un seul ťlectron, donc colonne
nį1, famille des alcalins.
Le niveau 4 est en partie occupť, donc 4Ťme ligne.
Ecrire
le schťma de Lewis de l'ion nitrate.
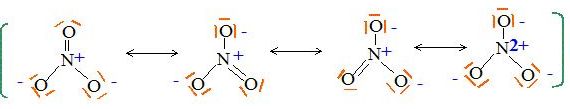
Le
requťrant dťsire connaÓtre la dangerositť des produits chimiques
retrouvťs lors de la perquisition. Quelle rťponse
pouvez-vous lui apporter ?
Voir le site concernant les risques des produits chimiques :
http://www.inrs.fr/accueil/risques.html
A
chaque proposition attribuer, sans justification, la bonne notion
:
Concerne
la dispersion des rťsultats mesurťs sur un mÍme ťchantillon, dans le
mÍme laboratoire, mais avec des analystes diffťrents, des appareils
diffťrents, et des jours diffťrents.
|
Rťplicabilitť
:
|
| Concerne
la dispersion des rťsultats mesurťs sur un mÍme ťchantillon, dans des
laboratoires diffťrents, avec des analystes diffťrents, des appareils
diffťrents, et des jours diffťrents. |
Reproductibilitť
|
Concerne
la proximitť ou le rapprochement entre la valeur mesurťe et une valeur
de rťfťrence considťrťe comme vraie ou rťelle.
|
Justesse.
|
Concerne
la dispersion des rťsultats mesurťs sur un mÍme ťchantillon, dans le
mÍme laboratoire, avec le mÍme analyste, le mÍme appareil et le mÍme
jour.
|
Rťpťtabilitť
|
Concerne
la dispersion des rťsultats mesurťs autour d'une valeur moyenne.
|
Prťcision.
|
Dťfinir "limite de
dťtection" et "limite de quantification".
La limite de dťtection d'une mťthode d'analyse est la plus petite
quantitť d'une espŤce qui peut Ítre dťtectťe mais pas forcťment
quantifiťe avec prťcision.
La limite de quantification est la quantitť la plus faible d’une espŤce
dans un ťchantillon qui peut Ítre dťterminťe quantitativement
avec fidťlitť et exactitude.
|
|