|
|
Elaboration de MoO3.
Le molybdŤne et ses dťrivťs sont extraits de la molybdťnite MoS2.
AprŤs concassage, broyage puis enrichissement par flottation ( pour
ťliminer les concentrťs de cuivre et de tungstŤne ), le minerai est
grillť ŗ l'air dans un rťacteur ( l'eau est ťvaporťe et le soufre est
ťliminť sous forme de SO2 ), selon la rťaction :
MoS2(s) + 3,5 O2(g) = MoO3(s) + 2SO2(g) (1).
Calculer l'enthalpie standard de la rťaction (1) ŗ 298 K et ŗ 700 K.
DrHį = 2DfHį(SO2(g)) + DfHį(MoO3(s)) -3,5 DfHį( O2(g)) - DfHį(MoS2(s)
DrHį298 =2(-296,8) +(-745,1) -3,5 *0 -(-235,1) = -1103,6 kJ mol-1.
On suppose les capacitťs thermiques molaires indťpendantes de la tempťrature sur l'intervalle [298 K - 700 K ].
DrHį700 = DrHį298 + (700-298) (2Cp(SO2(g))+Cp(MoO3(s))-3,5 Cp( O2(g))-Cp(MoS2(s) )
DrHį700 = -1103,6 + 402(2*39,9 +75,0 -3,5 *29,4 -63,5) 10-3 kJ mol-1.
DrHį700 = -1103,6 -4,66 = -1108,3 kJ mol-1.
Cette rťaction de grillage est-elle endo ou exothermique ?
DrHį ťtant nťgative, cette rťaction est exothermique.
L'opťration de grillage est rťalisťe en partant d'un mťlange stoechiomťtrique de MoS2 et d'air ( 20 % de dioxygŤne et 80 % de diazote ), initialement ŗ 298 K.
Quelle est la tempťrature finale TF atteinte par le mťlange, compte tenu de la chaleur dťgagťe par le grillage isobare de MoS2 ŗ 700 K ?
L'ťnergie dťgagťe par la combustion chauffe
les produits formťs et le diazote.
Le systŤme ťtant supposť adiabatique :
DrHį298 + (2Cp(SO2(g))+Cp(MoO3(s)) +14 Cp(N2) )(TF-298) =0
TF =298 -DrHį298 / (2Cp(SO2(g))+Cp(MoO3(s)) +14 Cp(N2) ).
TF =298 +1103,6 103 / (2*39,9 +75 +14 *29 ,1) =2261 K.
L'oxyde MoO3 est ensuite purifiť par voie humide ŗ l'aide de NH4OH
afin d'ťliminer Cu, Ni et W sous forme de sulfures. Comme le procťdť de
dťpŰt ťlectrochimique ultťrieur, ŗ partir d'une phase vapeur, nťcessite
l'utillisation de poudre mťtallique pure de molybdŤne, il convient au
prťalable de rťduire l'oxyde.
La rťduction de l'oxyde MoO3 en mťtal Mo est rťalisťe gr‚ce au dihydrogŤne dans un four. H2 trŤs pur et trŤs sec circule ŗ contre-courant sur des nacelles recouvertes de poudre de MoO3.
L'ensemble est ŗ la pression atmosphťrique. Les opťrations de rťduction
sont rťalisťes entre 700 et 1300 K ( domaine de tempťrature pour lequel
le mťtal et l'oxyde sont solides, non miscibles ) en deux ťtapes
successives.
Vers 800 K, le dihydrogŤne rťduit d'abord MoO3 en MoO2.
Ecrire cette rťaction de rťduction. Calculer la constante d'ťquilibre de cette rťaction ŗ 800 K.
MoO3(s) + H2(g) = MoO2(s) + H2O(g). (2)
DrGį2 = -85600-26,7 T.
DrGį2 = -85600-26,7*800 =-106 960 J mol-1.
DrGį2 = -RT ln K ; ln K = DrGį2 /( -RT) = 106960 / (8,31*800) =16,1 ; K = 9,7 106.
La rťaction est exothermique et sa constante d'ťquilibre est trŤs grande : elle dťmarre instantanťment et sera totale.
|
L'ťtape suivante rťalisťe vers 1000 K, consiste en la rťduction de MoO2 en Mo.
L'enthalpie libre de cette rťaction vaut DrGį3 =105300-98,6 T.
Calculer la constante d'ťquilibre de cette rťaction (3) ŗ 1000 K.
DrGį3 = 105300-98,6*1000 =6700 J mol-1.
DrGį3 = -RT ln K3 ; ln K3 = DrGį3 /( -RT) = 6700 / (8,31*1000) =0,81 ; K3 = 2,2.
Montrer que cette derniŤre rťaction ne peut dťmarrer dŤs la fin de la rťduction de MoO3 en MoO2.
DrGį3 est positive ŗ 1000 K : cette rťaction (3) est thermodynamiquement impossible.
Calculer le nombre de moles n de H2 nťcessaire pour assurer le dťmarrage de cette seconde rťduction ŗ partir de N moles de MoO3 prťsentes au dťpart.
MoO2(s) + 2H2(g) = Mo(s) + 2H2O(g). DrGį doit Ítre nťgative.
Enthalpie libre pour la rťaction : DrGį = DrHį -T DrSį ;
DrHį = N DfHį(Mo(s))+ 2N DfHį(H2O(g))-N DfHį (MoO2(s) -n DfHį (H2(g)).
DrHį3 =0 +2N(-241,8)-N(-588,9) = 105,3 N kJ.
DrSį = N Sį(Mo(s))+ 2N Sį(H2O(g)) -N Sį (MoO2(s) -n Sį (H2(g)) =28,7 N+2*188,8 N -46,3 N -130,6 n = 360 N-130,6 n J K-1.
DrGį = 105,3 N 103 -1000 (360 N-130,6 n ) J.
105,3 N -360 N + 130,6 n < 0 ; 130,6 n < 254,74 N ; n < 1,95 N.
|
Dťterminer, en utilisant par exemple un tableau d'avancement, le nombre de moles de H2 nťcessaire pour rťduire une masse de 3 tonnes de MoO3 dťposť sur les nacelles.
M(MoO3) =95,9 +3*16 =143,9 g/mo l; n(MoO3) = 3 106 / 143.9 =2,085 104 mol.
|
avancement (mol)
|
MoO3(s) |
+3H2(g)
|
= Mo(s)
|
+3H2O(g)
|
initial
|
0
|
2,085 104 |
n
|
0
|
0
|
en cours
|
x
|
2,085 104-x
|
n-3x
|
x
|
3x
|
fin
|
xmax
|
2,085 104-xmax =0
|
n-3xmax =0
|
xmax |
3xmax |
xmax =2,085 104 mol ; n = 3xmax =3*2,085 104=6,254 104 ~6,3 104 mol.
Quel(s) traitement(s) le dihydrogŤne excťdentaire doit-il subir avant d'Ítre injectť ŗ nouveau dans le rťacteur ?
Il faut ťliminer la vapeur d'eau. Le dioxygŤne de l'air doit Ítre
ťgalement ťliminť : le mťlange dihydrogŤne- dioxygŤne ťtant explosif
quasiment en toute sproportions.
Structure de MoO3.
Le trioxyde de molybdŤne prťsente ŗ l'ťtat solide une structure
assimilable ŗ une structure cubique dans laquelle les atomes de
molybdŤne occupent les sommets et ceux d'oxygŤne sont positionnťes au
milieu de chaque arÍte.
Reprťsenter en perspective la maille de MoO3. prťciser le nombre d'atome de chaque espŤce appartenant ŗ cette maille.
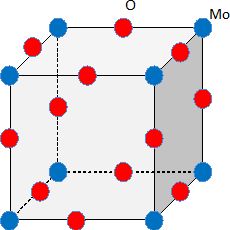
Chaque atome de molybdŤne appartient ŗ 8 mailles et compte pour 0,125 : pour une maille : 8*0,125 = 1 atome Mo en propre.
Chaque atome d'oxygŤne appartient ŗ 4 mailles et compte pour 0,25 : pour une maille :12*0,25 = 3 atomes O en propre.
Calculer le paramŤtre a de la maille, sachant que la masse volumique de MoO3 est Ķ=4690 kg m-3.
Volume de la maille : a3. Masse de la maille :
m =M(MoO3) / NA = 0,1439 / (6,02 1023) =2,39 10-25 kg.
a = (m / Ķ)1/3 =( 2,39 10-25 / 4690)1/3 =3,71 10-10 m = 371 pm.
|
Dťcrire le polyŤdre formť par les atomes d'oxygŤne autour du molybdŤne. Est-il rťgulier ?
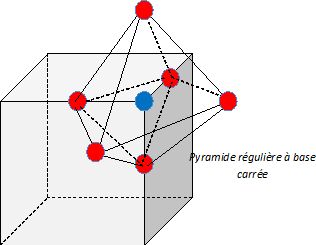
Dťterminer rMo, le rayon de l'atome de molybdŤne en supposant le contact Mo/O rťalisť sur chaque arÍte. rO= 130 pm.
Dans les tables, rMo~ 73 pm. Discuter de la nature de la liaison chimique dans MoO3.
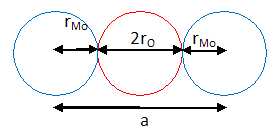
rMo = Ĺa -rO =185-130 = 55 pm.
L'atome d'oxygŤne est bien plus ťlectronťgatif que le molybdŤne. Les liaisons dans MoO3 ont un caractŤre ionique trŤs marquť. Le rayon de l'anion O2- est supťrieur ŗ celui de l'atome d'oxygŤne.
Calculer le rayon maximum rM+ du cation mťtallique de type M+ pouvant s'insťrer, soit en F, le centre d'une face, soit en C, le centre du cube, sans provoquer la dťformation de la maille.
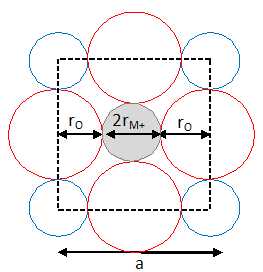 rM+ = Ĺa -rO =185-130 = 55 pm. rM+ = Ĺa -rO =185-130 = 55 pm.
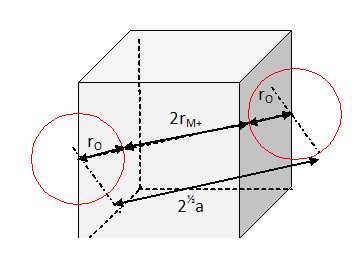 rM+ = Ĺ2Ĺa -rO =185*1,414-130 ~131 pm. rM+ = Ĺ2Ĺa -rO =185*1,414-130 ~131 pm.
Quel est le nombre maximal d'ion lithium Li+, pour lequel rLi+ = 60 pm pouvant s'insťrer dans MoO3 afin de donner une structure dite bronze de molybdŤne, de formule LiMoO3 ?
Sans
dťformation de la maille, un ion lithium peut s'insťrer au centre
du cube. Cet ion est trop gros pour venir s'insťrer au centre d'une
face, sans dťformer la maille.
|
|




