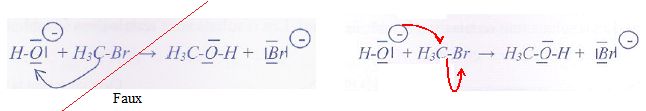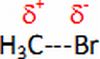|
|
Ester.
Les
esters sont responsables du goűt et de l'odeur agréable de nombreux
fruits et fleurs ainsi que de parfums artificiels. Ainsi l'éthanoate de
benzyle a l'odeur "fleurie" du jasmin.
L'éthanoate de benzyle peut-ętre synthétisé par la réaction suivante:
C6H5-CH2OH(l)+ CH3-COOH(l)
= H20(l) + CH3-COO-CH2-C6H5
(1)
Protocole pour la
synthčse de l'éthanoate de benzyle.
Introduire dans un ballon, avec précaution, 18,0 g d'acide éthanoďque CH3-COOH,
10,8 g d'alcool benzylique C6H5-CH2OH, 3 gouttes d'acide sulfurique concentré et
quelques grains de pierre ponce.
Chauffer le mélange ŕ ébullition douce pendant 30 minutes environ avec
le montage ŕ reflux.
Laisser refroidir le mélange.
Introduire 50 mL environ d'une solution saturée de chlorure de sodium
et mélanger.
Transvaser ce mélange dans une ampoule ŕ décanter. Agiter. Laisser
décanter les deux phases.
Aprčs avoir séparé les phases, introduire dans la phase organique une
pointe de spatule de sulfate de magnésium : un desséchant.
Aprčs filtration, peser la phase organique.
Espčce
chimique
|
acide
éthanoďque
|
Alcool
benzylique
|
Ethanoate
de benzyle
|
eau
|
eau
salée
|
masse
molaire (g/mol)
|
60
|
108
|
150
|
18
|
|
Température
ébullition °C
|
118
|
205
|
215
|
100
|
|
Densité
|
1,05
|
1,04
|
1,06
|
1
|
1,25
|
Solubilité
dans l'eau
|
totale
|
faible
|
faible
|
|
totale
|
Solubilité
dans l'eau salée
|
totale
|
faible
|
nulle
|
totale
|
|
a) L'utilisation du montage ŕ reflux permet de
dire que cette réaction n'est pas totale. Faux.
Cette réaction est lente
: la température est un facteur cinétique.
b) La phase organique dans l'ampoule ŕ décanter se trouve au-dessus.
Vrai.
La phase la plus dense,
l'eau salée, occupe la partie inférieure.
c) L'eau salée facilite la séparation entre les deux phases. Faux.
L'éthanoate de benzyle,
le produit ŕ isoler, est insoluble dans l'eau salée.
Lors d'un essai, la masse obtenue d'éthanoate de benzyle est égale ŕ
7,5 g.
d) Le rendement de cette transformation chimique est égal ŕ 50%. Vrai.
Recherche du réactif
limitant :
n( acide acétique ) =
18/60 =0,3 mol ; n( alcool) = 10,8 / 108 = 0,10 mol ( réactif limitant
).
On peut au mieux obtenir
0,10 mol d'ester soit 0,10 *150 = 15 g.
Rendement 7,5 / 15 = 0,5.
Mécanisme
de réaction :
a) Une flčche courbe correspond au déplacement d'un doublet
d'électrons. Vrai.
b) L'ion hydrogčne est un site donneur de doublet d'électrons. Faux.
H+
présente un défaut d'électron.
Une réaction de substitution peut ętre modélisée par l'équation
suivante:
HO- + CH3Br ---> CH3-OH+ Br-.
Donnée : l'électronégativité du brome est supérieure ŕ celle du carbone.
c) Le mécanisme suivant permet d'expliquer cette réaction de
substitution. Faux.
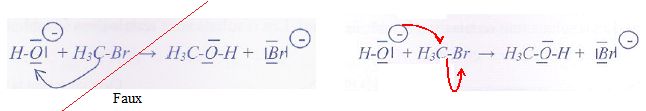
d) L'atome de carbone lié au brome est un site donneur de doublet
d'électrons. Faux.
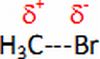
|
.
|
L'acide
acétylsalicylique est le principe actif de l'aspirine. La synthčse de
l'acide acétylsalicylique peut ętre réalisée au laboratoire ŕ partir
d'acide salicylique et d'anhydride éthanoďque. La réaction de synthčse
a pour équation :
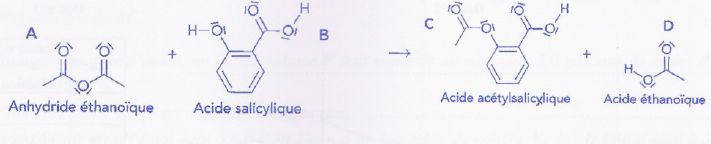
Donnée : l'électronégativité de l'oxygčne est supérieure ŕ celle du
carbone.
a) Le bilan de cette synthčse est une réaction de substitution. Faux.
Réaction d'estérification.
b) L'atome d'oxygčne, désigné par la flčche ci-dessous, est un site
accepteur de doublet d'électrons. Faux.
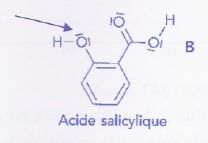
L'atome d'oxygčne
possčdant deux doublets d'électrons libres est donneur d'électrons.
En réalité la réaction de synthčse est un mécanisme qui se fait en
plusieurs étapes dont la premičre étape a pour équation :
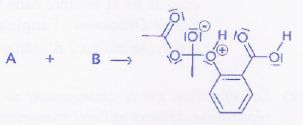
c) La réaction de la premičre étape du mécanisme est une réaction
d'addition. Vrai.
Attaque nucléophile sur
le carbone d'un groupe carbonyle de l'anhydride A.
d) La seconde étape du mécanisme de la réaction de synthčse est une
réaction acido-basique. Vrai.
Mécanisme d'une estérification entre un acide
carboxylique RCOOH et un
alcool primaire R'OH, en milieu acide.
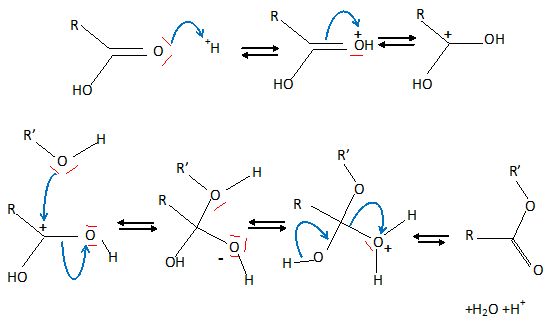
|
|
Lorsque
le raisin est műr, la concentration en saccharose (sucre) atteint ou
dépasse 6,00.10-1 mol par litre de jus de raisin. Les
vendanges peuvent commencer, les grappes de raisin sont ŕ maturité
optimale.
Le maitre de chais sait qu'il faut 18,0 g de sucre par litre de jus
pour obtenir un degré d'alcool. Il utilise la réfractométrie, technique
basée sur la mesure de l'indice de réfraction n d'un milieu transparent
pour trouver la quantité de sucre dans ses jus de raisin et en déduire
le degré d'alcool de son vin.
Dans un premier temps, il mesure l'indice de réfraction ni
de différentes solutions Si de saccharose, de concentrations
massiques Cmi connues, en les plaçant successivement dans
une cuve traversée par un
rayon lumineux Doc n°l. Ses mesures sont rassemblées et permettent de
tracer le graphe ni = f (Cmi) en Doc n°2.
Dans un second temps, il mesure l'indice de réfraction de deux
échantillons A et B de jus de raisin vendangé quelque temps auparavant.
Les résultats sont réunis dans le tableau du Doc n°3.
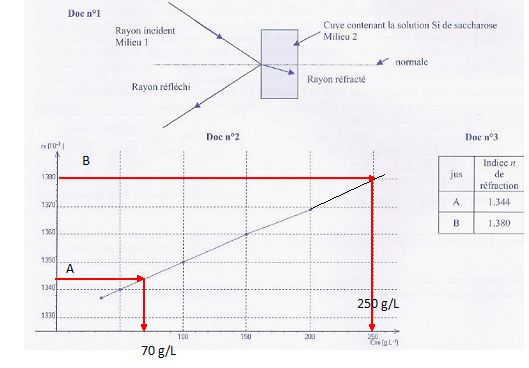
Données : masse molaire du saccharose: 342 g/mol.
L'indice de réfraction n d'un milieu transparent est donné par la
relation n =c / v oů c est lacélérité de la lumičre dans le vide et v
la célérité de la lumičre dans le milieu considéré.
Loi de Descartes : l'angle d'incidence i1 dans le milieu 1
d'indice n1 et l'angle de réfraction i2 dans le
milieu 2 d'indice n2 sont liés par la relation n1
sin i1 = n2 sin i2.
a) La réfraction est le changement de direction d'un rayon lumineux
lorsqu'il traverse la surface de séparation de deux milieux
transparents d'indice différent. Vrai.
b) Le jus B est plus sucré que le jus A. Vrai.
D'aprčs le doc n°2, plus
l'indice est élevé, plus la concentration du saccharose est grande.
c) Le raisin du jus A est műr. Faux.
Lorsque le raisin est műr, la concentration en
saccharose (sucre) atteint ou dépasse 6,00.10-1 mol par
litre de jus de raisin. 0,600
*342 ~205 g/L.
D'aprčs le doc n°2 la
concentration massique du jus en saccharose n'est que de 70 g/L.
d) Lejus B est un jus qui a un degré d'alcool supérieur ŕ 12,5°. Vrai.
Il faut 18,0 g
de sucre par litre de jus pour obtenir un degré d'alcool. 250 / 18 ~14°.
|
|
Le
territoire du Québec possčde de nombreux lacs appelés « lacs acides»
dont le pH est inférieur ou égal ŕ 5,0. Cette acidité d'origine
naturelle ou humaine est survenue au cours des cent derničres années.
Touchés par les pluies acides, émises par les grosses industries, les
résidents du lac des Hauteurs doivent pour contrer l'effet de
l'acidité, épandre de la chaux sur leur terrain et planter des
feuillus. La réduction
des émissions polluantes représente vraisemblablement la meilleure
solution ŕ long terme pour éliminer le problčme des pluies acides.
Toutefois, en attendant ces réductions, il faut parfois recourir ŕ des
solutions
temporaires: le chaulage représente l'une de ces rares alternatives.
Au Québec, le chaulage a été évalué expérimentalement par le ministčre
de l'environnement et de la faune. Une vingtaine de lacs,
principalement dans la région des trois rivičres sont maintenant
chaulés.
Cette technique consiste ŕ augmenter le pH du lac en y versant une base
solide telle que le carbonate de calcium.
La réaction de chaulage considérée comme totale s'écrit :
Ca2+(aq)+ CO32-(aq)+ 2 H30+
~ CO2 (aq)+ Ca2+(aq)+ 3 H2O(l)
Des demandes d'aides financičres sont réclamées car le coűt de la tonne
de carbonate de calcium CaC03(s)se situe aux environs de
1200 euros et ces lacs ont des volumes pouvant atteindre 500 millions
de m3.
De plus, une fois réalisé, le chaulage du plan d'eau permet un retour ŕ
la normale pendant seulement une quinzaine d'années, il faut ensuite
renouveler l'opération.
D'aprčs le ministčre du développement durable de l'environnement et des
parcs.
Données : masse molaire du carbonate de calcium M = 100 g/mol ;
couples acide/base intervenant au cours du chaulage: CO2, H2O
/ HCO3-aq et HCO3-aq
/ CO32-aq. V = 500 millions de m3.
a) Pour ętre qualifié d'acide, un lac de volume V doit contenir au
minimum 5,0 millions de moles d'ions oxonium H30+.
Vrai.
[H30+ ] =n / V =5,0 106
/ (500 109) =10-5
mol/L. Par suite pH = 5.
b) L'ion
carbonate CO32-aq est une espčce
amphotčre. Faux.
c) Pour obtenir un pH final égal ŕ 6,0 dans l'eau d'un lac acide de
volume V, de pH initial égal ŕ 5,0, il faut y déverser environ 23
tonnes de carbonate de calcium. Faux.
Quantité de matičre d'ion H30+
: initiale : 5,0 106 mol ; finale : 5,0 1011* 10-6
=5,0 10-5 mol ; variation : 4,5 106 mol.
n(CaCO3) = 2,25 106 mol
soit 2,25 106
*100 = 2,25 108 g =
225 tonnes.
d) Le
coűt du chaulage pour augmenter d'une unité le pH d'un lac de volume V
dépasse les 200 000 euros. Vrai.
225*1200 =2,7 105 €.
|