|
|
La
sťparation des mťtaux par ťlectrolyse, ŗ partir de leurs ions en
solution, est possible avec de bons rendements. Dans de nombreux cas
l'enregistrement prťalable de courbes intensitť-potentiel dans des
conditions stationnaires est souhaitable. On dispose au laboratoire des
appareils suivants :
- boÓtes de rťsistance, voltmŤtre ŗ forte impťdance, milliampŤremŤtre, potentiostat, cellule conductimťtriques.
- diverses ťlectrodes conductrices ( de platine, de carbone vitreux, d'or ).
- ťlectrode au calomel saturť en KCl, ťlectrode de chlorure d'argent, ťlectrode de verre.
- petites cellules en verre pirex.
Sur le schťma ci-dessous, identifier les diffťrents ťlťments permettant d'enregistrer une courbe intensitť-potentiel.
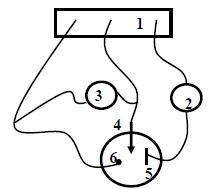
(1)
: potentiostat ; (2) milliampŤremŤtre en sťrie ; (3) voltmŤtre en
parallŤle ; (4) ťlectrode de travail ; (5) ťlectrode auxiliaire en
platine ; (6) ťlectrode de rťfťrence.
On a enregistrť, ŗ l'aide du montage ci-dessus, la courbe de
polarisation d'une ťlectrode de platine plongeant dans une solution
aqueuse de nitrate de sodium ŗ 0,1 mol/L.
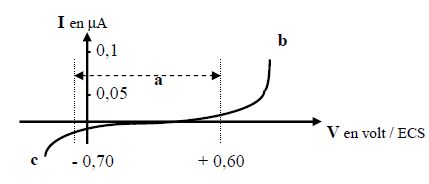
Identifier les parties de la courbe qui correspondent ŗ des ťchanges ťlectrochimiques avec l'ťlectrode.
Les
parties de la courbe qui ne sont pas confondues avec l'axe horizontal
corespondent ŗ des ťchanges d'ťlectrons avec les ťlectrodes.
Identifier les rťactions ťlectrochimiques en cause.
La
partie de la courbe sous l'axe horizontal correspond ŗ une rťduction ;
la partie situťe au dessus de l'axe horizontal correspond ŗ une
oxydation.
On peut enregistrer une courbe de polarisation, dans un montage
ťlectrochimique ŗ trois ťlectrodes, ŗ l'aide d'une ťlectrode solide
tournante. La figure ci-dessous reprťsente la courbe obtenue avec un
disque de platine poli tournant ŗ 2000 tours par minute, pour une
solution constituťe d'un mťlange ťquimolaire de bromure de sodium et de
dibrome de concentration 5 10-3 mol/L dans l'acide sulfurique 1 mol/L. La vitesse de balayage des potentiels est de 2 mV/s.
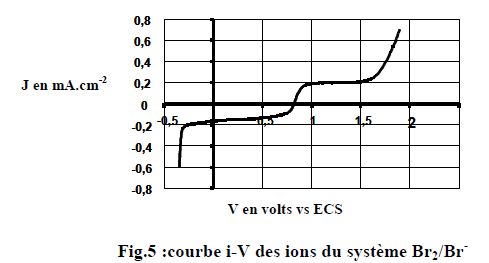
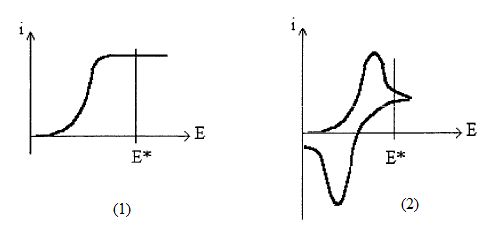
Mise ŗ part les branches correspondant aux parties b et c le courant
observť prťsente l'allure d'une courbe en "S", couramment dťsignťe sous
le vocable de "vague polarographique".
Identifier les rťactions ťlectrochimiques qui correspondent ŗ cette vague polarographique.
Partie infťrieure, rťduction du dibrome : Br2 +2e- = 2 Br-.
Partie supťrieure, oxydation de l'ion bromure : 2 Br- + 2e- = Br2.
Identifier le phťnomŤne responsable de la quasi-onstance du courant entre 1 V et 1,5 V ( i1 ~0,2 mA) et entre 0 et -0,5 V( i2 ~ -0,2 mA).
La concentration des espŤces qui rťagissent aux ťlectrodes diminue au
voisnage des ťlectrodes. Un apport de matiŤre est nťcessaire depuis le
sein de la solution. Ce phťnomŤne de diffusion limite l'intensitť du
courant et on observe des paliers sur la courbe.
Entre ces deux domaines le courant varie rapidement. On appelle potentiel de demi-vague EĹ la valeur du potentiel qui correspond ŗ une valeur du courant demi-somme des deux courants prťcťdents ( j1+j2) / 2.
Evaluer EĹ dans cette expťrience .
( j1+j2) / 2 = 0 et EĹ~0,8 V.
Dťduire de l'allure de la courbe, si le systŤme ťtudiť correspond ŗ des ťchanges ťlectroniques rapide ou lent.
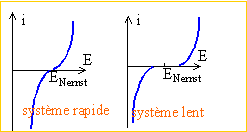
Les ťchanges ťlectroniques peuvent Ítre considťrťs comme rapides.
Pourquoi
place-t-on un flacon laveur contenant de la soude ŗ la sortie du
montage ? Ecrire les rťactions qui s'y produisent.
(1) avec rotation de l'ťlectrode, la vitesse d'apport de matiŤre est constant, indťpendant du temps.
(2) sans convection, la vitesse d'apport de matiŤre n'est pas constante.
|
.
|
Des courbes de polarisation peuvent ťgalement Ítre enregistrťes avec une ťlectrode ŗ goutte de mercure ( polarographie).
On a enregistrť le polarogramme d'une solution 10-3 mol/L de nitrate de cadmium Cd(NO3)2 dans le nitrate de potassium 0,1 mol/L aprŤs 2 minutes de barbotage de diazote.
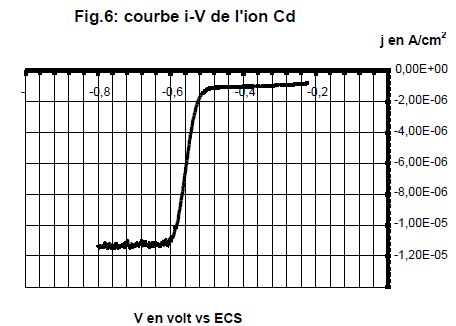
Indiquer l'importance du barbotage de diazote.
Avant chaque analyse,il faut ťliminer l’oxygŤne dissous dans la solution. En effet, celui-ci prťsente deux vagues de rťduction.
O2 + 2e- +2H+ =H2O2.
H2O2 + 2e- +2H+ =2H2O
Les vagues correspondantes se situant dans
l'intervalle potentiel[ -500 mV ; -1200 mV, rendent inutilisable
le polarogramme. Iil est donc nťcessaire de
l’ťliminer par barbotage d’azote dans la solution pendant quelques minutes.
Justifier l'utilisation d'une solution de KNO3.
Si
la solution n’est pas agitťe, le transport des espŤces ťlectroactives
vers l’ťlectrodes’effectue par migration et par diffusion.
On ajoute , le plus souvent, un large excŤs d’ťlectrolyte indiffťrent ťgalement appelť ťlectrolyte support. Dans ce cas :
– La migration des espŤces redox devient nťgligeable et leur transport
dans la solution s’effectue par diffusion.On peut ainsi rťduire sur la
cathode un cation, un anion ou bien une espŤce neutre.
– La force ionique de la solution est imposťe par l’ťlectrolyte support
et les coefficients d’activitť des espŤces redox restent constants.
A quel processus ťlectrolytique correspond la vague observťe ?
Rťduction de l'ion cadmium : Cd2+ + 2e- = Cd(s).
|
|
On a maintenant enregistrť le polarogramme d'un mťlange d'ions Cd2+ / Zn2+, dans les mÍmes conditions expťrimentales qu'ŗ la question prťcťdente.
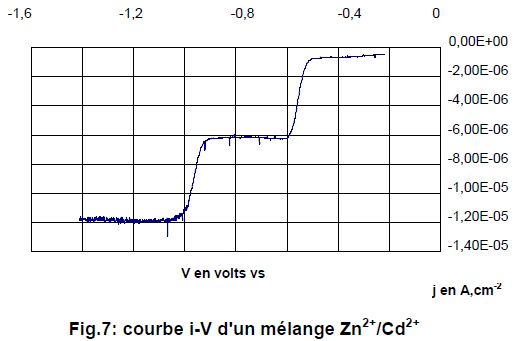
Identifier les processus ťlectrochimiques correspondant aux deux paliers de courants observťs.
Rťduction de l'ion zinc ( palier compris entre -1,4 et -1 V) : Zn2+ + 2e- = Zn(s).
Rťduction de l'ion cadmium pour l'autre palier ( palier compris entre -1 et -0,6 V) : Cd2+ + 2e- = Cd(s).
Estimer le potentiel de demi-vague du zinc dans ces conditions. EĹ ~ -0,95 V.
On souhaite maintenant ťliminer le cadmium prťsent dans un minerai de
zinc. La solution obtenue aprŤs traitement du mťlange d'oxydes par de
l'acide sulfurique est ťlectrolysťe sur cathode d'aluminium pour
laquelle la surtension du dihydrogŤne est similaire ŗ celle du mercure.
Dťfinir le terme de surtension.
La surtension ťlectrochimique ( ŗ intensitť donnťe ), est la diffťrence
entre la valeur expťrimentale du potentiel ŗ appliquer ŗ l’ťlectrode
pour obtenir cette intensitť et celle du potentiel thermodynamique
d’oxydorťduction.
Quel potentiel contrŰlť faut-il appliquer ŗ la cathode pour ne dťposer que le cadmium ? ~ -0,6 V.
Quel est le profil de la courbe j(t) pendant l'ťlectrolyse et ŗ quel moment peut-on considťrer que l'ťlectrolyse est terminťe ?
j(t) ťtant proportionnelle ŗ la concentration en ion cadmium, j(t)
diminue au cours de l'ťlectrolyse. Celle-ci est terminťe lorsque j(t)
s'annule.
On poursuit l'ťlectrolyse avec une nouvelle cathode d'aluminium mais cette fois avec un montage ŗ intensitť imposťe.
Quel est le mťtal rťcupťrť ŗ la cathode ?
L'eau et l'ion zinc peuvent Ítre rťduits ŗ la cathode. On observe un
dťpŰt de zinc ŗ la cathode du fait de la grande surtension du
dihydrogŤne.
L'ampŤremŤtre indique I = 1,5 A et l'ťlectrolyse dure 7 heures.
Quelle est la quantitť de zinc rťcupťrť ?
Q = I t = 1,5*7*3600 = 3,78 104 C.
Quantitť de matiŤre d'ťlectron : n(e-) = Q / 96485 = 3,78 104 /96485 =0,3918 mol.
Le zinc ťtant bivalent n(Zn) = Ĺn(e-) =0,196 mol soit m = n(Zn) M(Zn) =0,196*65,4 = 12,8 g.
|
|