|
|
Quinine et
chloroquine. Extraction de
la quinine.
L'ťcorce de quinquina utilisťe dans la cordiliŤre des Andes comme
antipyrťtique a ťtť apportťe en Europe au dťbut du XVIIe
siŤcle. En 1820, P Pelletier et J Caventou ont extrait la quinine,
reprťsentťe ci-dessous.
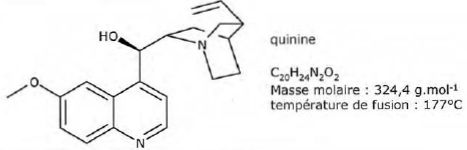
La quinine a ťtť le premier mťdicament efficace contre le paludisme.
Que
signifie le terme "antipyrťtique" ?
Les
antipyrťtiques sont des mťdicaments destinťs ŗ abaisser la
tempťrature du corps ou ŗ diminuer la fiŤvre.
La quinine est une dibase notťe Q dont les couples acido-basiques sont
: QH22+/QH+ ( pKa = 5,1) et
QH+ /Q ( pKa2=9,7).
Identifier sur la
structure les groupes caractťristiques responsables de ces propriťtťs
acido-basiques. On ne demande pas d'attribuer leur pKa.
Ces propriťtťs acido-basiques sont dues aux doublets non liants portťs
par les atomes d'azote engagťs dans les cycles. Ces cycles n'ťtant pas
aromatiques, ces doublets sont assez disponibles.
On propose quelques ťtapes du protocole d'extraction de la quinine ŗ
partir de l'ťcorce de quiquina. ( extrait du BUP mars 2009, vol
103, nį912, p311-320 ).
L'ťcorce est tout d'abord traitťe par de la soude dans l'ťthanol, puis
extraite au dichloromťthane. La solution limpide extraite est alors
soumise au protocole de purification suivant :
- Prťlever 50 mL de la solution de dichloromťthane rťsultant de
l'extraction
- Etape 1 : extraire
la solution de dichloromťthane ŗ l'aide de 2 fois 10 mL de solution
d'acide chlorhydrique de concentration environ 0,1 mol/L. Rťunir les
deux phases aqueuses, les laver ŗ l'aide de 10 mL de dichloromťthane.
Etape 2 :
dans un erlenmeyer, ajouter goutte ŗ goutte une solution de soude de
concentration environ 0,5 mol/L ( vťrifier le pH ŗ l'aide de papier pH
). L'ajout de soude provoque un prťcipitť blanc dans l'erlenmeyer.
Etape 3 :
une fois que le pH est de 12, extraire cette phase aqueuse ŗ l'aide de
deux fois 20 mL de dichloromťthane.
Etape 4 :
rťunir les phases organiques, ajouter une spatule de sulfate de sodium
anhydre, filtrer ŗ l'aide d'un papier filtre plissť. Transvaser le
filtrat dans un ballon tarť et ťvaporer le solvant.
Analyser
soigneusement le protocole afin d'expliquer en quoi les ťtapes 1 ŗ 3
permettent disoler la quinine.
L'extraction double
est plus efficace que l'extraction simple ŗ volume de solvant identique.
Etape 1
: dans le dichloromťthane, phase organique, la quinine se trouve sous
la forme "Q". Lors de l'ajout d'acide chlorhydrique, la quinine se
trouve sous la forme QH2+, soluble dans un solvant
polaire comme l'eau, quasiment insoluble dans le dichloromťthane.
Etapes 2 et 3 : l'ajout de soude
jusqu'ŗ pH= 12 fait passer la quinine sous la forme Q, quasiment
insoluble dans l'eau. La quinine prťcipite. La forme Q de la quinine
ťtant trŤs soluble dans le dichloromťthane, on peut l'extraire gr‚ce ŗ
se solvant.
Identifier
les objectifs de l'ťtape 4.
Eliminer les traces d'eau gr‚ce au sulfate de sodium anhydre, solide
ťliminer ensuite par filtration.
Evaporer le solvant volatil afin de rťcupťrer la quinine.
|
.
|
SynthŤse de la chloroquine.
La chloroquine H est un antipaludťen de synthŤse, mise sur le marchť en
1949. Il prťsente moins d'effets secondairesque la quinine qui peut
provoquer hypoglycťmie, hypotension, vertiges, troubles allergiques...
Sa structure est indiquťe ci-dessous.
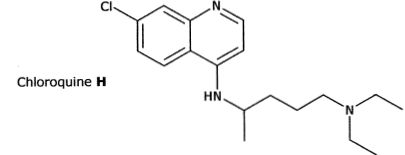
Une synthŤse de la
chloroquine ŗ partir de la 2-chloroaniline a ťtť publiťe en 1946 ( J.
Am. Chem Soc. 1946, 68, 113-116 ). Les ťtapes de la synthŤse sont
schťmatisťes ci-dessous.
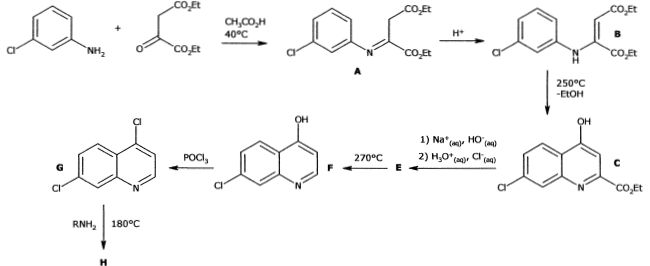
Prťparation de l'imine A.
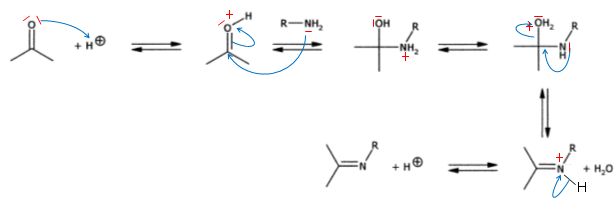
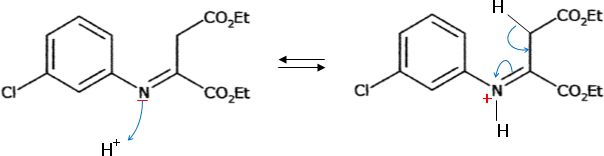
Les diffťrentes ťtapes d'un mťcanisme de la synthŤse d'une imine catalysťe par les ions H+ sont reproduits.
Complťter le mťcanisme.
Indiquer les charges formelles manquantes sur les intermťdiaires
rťactionnels, les doublets d'ťlectrons impliquťs et les flŤches
indiquant leurs dťplacements.
Pourquoi la formation d'une imine est-elle ralentie si le pH est trop faible ?
La
premiŤre ťtape du mťcanisme ci-dessus ( protonation de l'oxygŤne du
carbonyle ) n'a pas lieu. Le carbone du carbonyle est moins activť en
vue d'une attaque par le doublet de l'azote.
Proposer un mťcanisme pour la rťaction, catalysťe par les ions H+, pour passer de l'imine A au composť B.
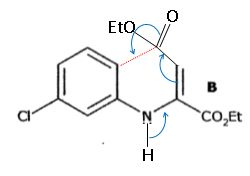
Etape B--> C.
Reproduire la molťcule B en indiquant les atomes qui se lient au cours de la transformation B---> C.
C est en ťquilibre avec la molťcule C' : 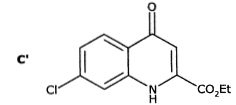
De quel type d'ťquilibre s'agit-il ? Justifier par un argument structural que C est largement majoritaire.
Il s'agit d'un ťquilibre
cťto-ťnolique. Dans la molťcule C, les deux doubles liaisons C=C du
cycle azotť sont conjuguťes avec les 3 doubles liaisons du cycle
aromatique. C est stabilisťe par rťsonance.
La transformation conduit ťgalement ŗ un composť D, un isomŤre de C. Reprťsenter D.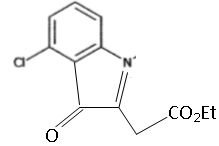
L'isomŤre C est sťparť de l'isomŤre D par recristallisation dans l'acide acťtique glacial.
Que signification le qualiquatif " glacial " dans ce contexte ?
L'acide acťtique pur est ťgalement nommť acide acťtique glacial.
Expliquer le principe de la purification par recristallisation.
Le solide ŗ
purifier est dissout dans un solvant ou dans un mťlange de plusieurs
solvants chaud ; puis on refroidit la solution pour provoquer la cristallisation
du solide que l’on isole par filtration. Quant aux impuretťs, elles doivent
Ítres solubles dans le solvant ŗ chaud comme ŗ froid.
|
|
Etape C--> E.
Quel est le nom de la rťaction mise en oeuvre lors du traitement de C par une solution aqueuse d'hydroxyde de sodium ?
Saponification ou hydrolyse basique d'un ester suivi du passage ŗ l'acide carboxylique en ajoutant de l'acide chlorhydrique.
Donner le mťcanisme de cette rťaction. On pourra utiliser une reprťsentation simplifiťe de C.
Dans le cas gťnťral d'un ester :
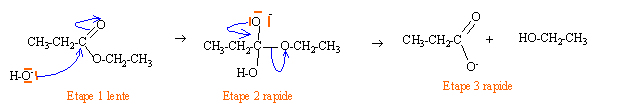
Reprťsenter le produit E obtenu.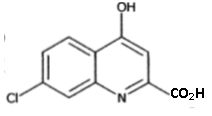
Etape E--> F.
Le composť F est obtenu par simple chauffage de E dans une huile minťrale.
Donner l'ťquation de la rťaction modťlisant le passage de E ŗ F. Comment s'appelle cette rťaction ? Dťcarboxylation d'un acide carboxylique.
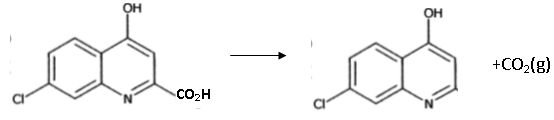
|
|