|
|
Dans
une entreprise de traitement de l'eau, un bidon ancien est retrouvé.
D'aprčs l'étiquette, il contient une solution d'hydroxyde de sodium ( Na+
+ HO-) de pH = 9,7.
Le
technicien désire vérifier la valeur du pH indiqué sur l'étiquette :
pour cela il dose V =200,0 mL de cette solution par une solution
d'acide chlorhydrique de concentration ca = 2,0
10-4 mol/L.Le volume d'acide versé ŕ
l'équivalence vaut VE = 15,8 mL.
Cette solution est-elle ou acide ou basique ? Justifier
.
Une solution de pH supérieur ŕ 7 ŕ 25°C est basique.
On suppose son pH égal ŕ 7. Calculer
les concentrations en ion oxonium et hydroxyde.
[H3O+]=10-9,7
=2,0 10-10 mol/L.
[HO-]=10-14 / [H3O+]=10-14
/ 10-9,7
=10-4,3
=5,0 10-5 mol/L.
Ecrire
l'équation de la réaction de dosage.
H3O+aq + HO-aq
---> 2H2O(l).
Déterminer
la concentration de la solution d'hydroxyde de sodium.
cb = caVE
/ V =2,0 10-4*15,8 / 200 =1,6 10-5
mol/L.
En
déduire la valeur du pH. L'indication de l'étiquette est-elle toujours
correcte ?
pH = 14 + log cb = 14 + log (1,6 10-5)
=9,2.
Ecart relatif : (9,7-9,2) / 9,2 ~0,05 ( 5%).
L'indication est considérée comme correcte ŕ 5 % prčs.
Pour utiliser cette solution, qui reste trop concentrée, le technicien
la dilue dans une grande quantité d'eau.
Comment
évolue le pH ? Vers quelle limite tend-il ?
Par dilution d'une solution basique, le pH diminue et tend vers 7 ŕ
forte dilution. |
.
|
Installation
électrique.
Le réseau triphasé 230 V / 400 V ; 50 Hz, alimente un atelier
comprenant :
- 9 lampes ŕ incandescence identiques purement résistives : 100 W - 230
V ;
- un moteur asynchrone triphasé M1 : Putile
= Pu = 7,5 kW ; rendement h = 0,80 ; facteur
de puissance cos f1
= 0,68.
- un
moteur asynchrone triphasé M2 : Pabsorbée
= PM2 = 3,0 kW ; facteur de puissance cos f2
= 0,75.
Tous ces appareils sont répartis sur les différentes phase de maničre ŕ
ce que le systčme soit équilibré.
Comment
coupler une lampe sur le réseau ? Justifier.
La tension aux bornes d'une lampe doit ętre égale ŕ 230 V, cest ŕ dire
la tension simple.
Une lampe sera donc branchée entre une phase et le neutre.
Compléter
le tableau suivant :
|
9 lampes |
moteur M1 |
moteur M2 |
installation |
| Puissance
active (kW) |
0,9 |
7,5 /
0,8 =9,375 ~9,4 |
3,0 |
P=13,3 |
| Puissance
réactive ( kVAR) |
0 |
9,4 tan f1
=10,13 ~10,1 |
3,0 tan f2=2,65
~2,7 |
Q=12,8 |
Vérifier
que la puissance apparente S de l'installation vaut 18,4 kVA.
S = (P2+Q2)˝
=(13,32 + 12,82)˝
=18,4 kVA.
Calculer
la valeur efficace de l'intensité du courant en ligne.
I= S / (3˝U) =18,4 103
/ (1,732*400) =26,56 ~26,7 A.
Calculer
le facteur de puissance de l'installation.
cos f = P
/ S = 13,3 / 18,4 =0,723 ~0,72.
Quel
est l'intéręt d'avoir un facteur de puissance élévé ? Proposer une
solution pour améliorer le facteur de puissance.
Un facteur de puissance élévé diminue l'intensité en ligne, donc les
pertes par effet Joule.
En branchant des condensateurs en triangle, en amont de l'installation,
on améliore le facteur de puissance.
Etude
du moteur M1.
On donne la plaque signalétique de ce moteur : 230 / 400 V ; cos f1
= 0,68 ; Pu = 7,5 kW ; 1440 tr/min ; 50 Hz ;
rendement : 80 %.
Préciser
la fréquence de synchronisme ns, le
nombre de paires de pôles p et le gissement g.
n = 1440 / 60 = 24 tr/s ou Hz ; ns est un peu
supérieure ŕ n : ns = 25 Hz ou 1500 tr/min.
Nombre de paires de pôles : p = 50 / 25 = 2.
Glissement g = (1500-1440/ / 1500 = 0,04.
Exprimer
puis calculer le moment du couple utile Tu en
fonctionnement nominal.
Pu = 2p
n /60 Tu ; Tu = 60Pu/(2p n)
=60*7500/(6,28*1440)=49,8 Nm.
|
Pompe ŕ chaleur air- air.
Cette machine fonctionne avec une source froide ( extérieur du local ) dont la température est qA = -8°C et une source chaude ( l'intérieur du local ) dont la température est qB = 20°C.
Une quantité de matičred'air n décrit le cycle suivant :
A --> B : compression adiabatique réversible ; la température évolue de qA ŕ qB.
B --> C : compression isotherme.
C --> D : détente adiabatique réversible.
D --> : détente isotherme.
Chaque
état du systčme est caractérisé par sa pression p, son volume V et sa
température T. l'air est considéré comme un gaz parfait.
TA =265 K ; pA = 1,50 105 Pa ; VA = 0,800 m3 ; TB =293 K ; pC = 3,50 105 Pa ; Cv=20,8 J mol-1 K-1 ; g = 1,40. relation de Laplace : TVg-1 = constante.
Montrer que n = 54,5 mol.
n = pAVA / (RTA) =1,50 105 *0,800 / (8,314*265) =54,47 ~54,5 mol.
Montrer que VB = 0,62 m3.
La relation de Laplace s'écrit entre A et B ( adiabatique réversible ) : VA g-1 TA = VB g-1 TB ;
VB g-1 =VA g-1 TA /TB ; VB =VA(TA /TB)1/g-1.
VB = 0,800 (265/293)2,5 =0,6223 ~0,622 m3.
Calculer VC. On donne pB = 2,13 105 Pa.
B---> C : compression isotherme : pB VB = pC VC.
VC = pB VB / pC =2,13 105 0,622 / (3,50 105)=0,379 m3.
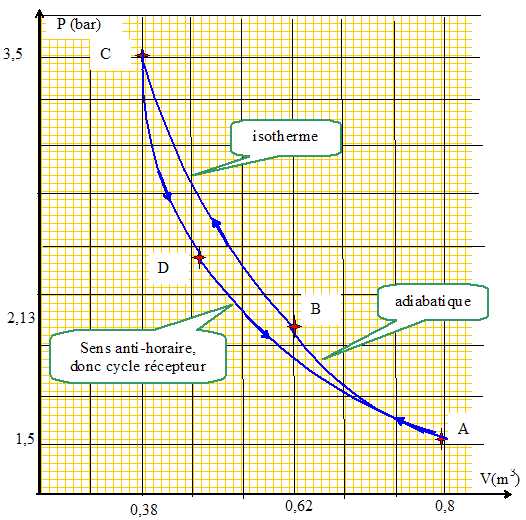
Tracer
l'allure du diagramme de Clapeyron ( p, V) du cycle, en indiquant les
états A, B, C et D ainsi que le sens de parcours du cycle.
La relation de Laplace s'écrit entre C et D ( adiabatique réversible ) : pCVC g =pD VD g = 3,50 105 *0,3791,4 =9,00 104. (1).
Détente isotherme entre D et A : pA VA = pD VD = 1,50 105 *0,800 =1,2 105 (2).
(1) / (2) donne : VD g-1 =9,00 104 / 1,2 105=0,75 ; VD =0,752,5 =0,487 m3.
Par suite : pD =1,2 105/0,487=2,46 105 Pa.
|
|
